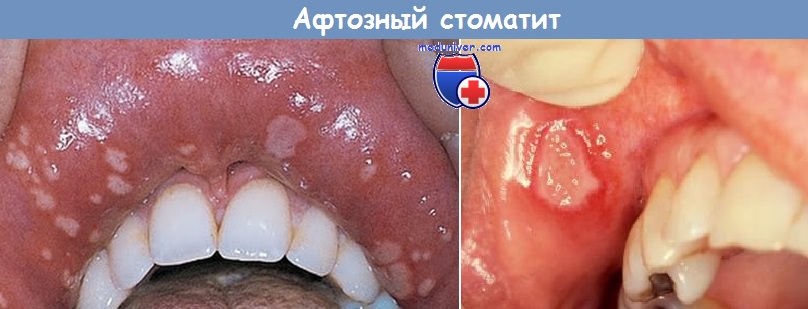
Лейкопенический тест что это
Лейкопеническая проба может быть дополнена тромбоцитопенической пробой, которая основана на том же принципе. Уменьшение количества тромбоцитов крови на 20% косвенно подтверждает сенсибилизирующее действие протеза. Однако следует отметить, что тромбоцитопенический тест бывает положительным реже.
Для гиперчувствительности замедленного типа на протезы из акрилатов и нержавеющей стали характерно уменьшение (лейкопения) количества лейкоцитов в крови. Однако при дифференциальной диагностике аллергических стоматитов мы пользовались результатами клинического анализа периферической крови. Это связано с тем, что в последнее время доказана роль других (кроме лимфоцитов) клеток крови в индуцировании аллергической реакции. Сегментоядерные, т.е. нейтрофильные, лейкоциты — это вспомогательные клетки аллергического воспаления, принимающие участие в антителозависимой цитотоксичности, а также киллеры, уничтожающие клетки с адсорбированным на их мембране аллергеном.
Определение количества моноцитов крови как предшественников макрофагов позволяет косвенно судить об активности этих поглощающих и расщепляющих чужеродные вещества клеток. В периферической крови при аллергическом стоматите появляются и другие изменения: лимфоцитоз, увеличение числа плазматических клеток. По мнению А. Д. Адо (1970), увеличение количества лимфоцитов в крови при аллергии закономерно, так как иммунологическая реактивность реализуется этими клетками при замедленном типе аллергических реакций.
Периферическая кровь изучена нами у 177 больных аллергическим стоматитом. Для примера приводим результаты клинического анализа крови больного аллергическим стоматитом, вызванным протезами из нержавеющей стали.
При аллергическом стоматите, обусловленном металлическими протезами из нержавеющей стали, в крови отмечаются лейкопения, уменьшение содержания сегментоядерных нейтрофилов, относительный лимфоцитоз, моноцитоз. Спустя 3—4 нед после снятия металлических протезов, показатели крови нормализуются. При этом значительно улучшается состояние полости рта (исчезает жжение, сухость, отек слизистых оболочек), нервной системы (улучшается сон, аппетит).
При аллергическом стоматите, вызванном пластмассовыми протезами, в периферической крови отмечается тенденция к лейкопении, лимфоцитозу, моноцитозу, а также уменьшение числа сегментоядерных нейтрофилов, т. е. аналогичная картина как и при аллергическом стоматите к металлам. Для примера приводим показатели крови при проведении экспозиционно-провокационной пробы на акриловый протез.
У 50 больных токсическим стоматитом при проведении экспозиционно-провокационной пробы на акриловый протез в крови нами выявлены лейкоцитоз, увеличение СОЭ, уменьшение количества эритроцитов, гемоглобина, что подтвердило токсическую реакцию на пластмассовые протезы.
Таким образом, клинический анализ крови у больных с непереносимостью акриловых и металлических протезов является дифференциально-диагностическим тестом для установления генеза заболевания при проведении экспозиционно-провокационной гробы.
Наши наблюдения показывают, что комплексная оценка динамики показателей периферической крови имеет большее значение, чем определение только какого-либо одного форменного элемента крови. Клинический анализ крови необходимо проводить у всех больных при непереносимости зубных протезов из пластмассы и металла с целью установления аллергического или токсического генеза этого явления.
Лейкопения
Лейкопения – это снижение уровня лейкоцитов в периферической крови ниже 4000 в 1 мкл. Причиной данного состояния могут быть инфекционные, воспалительные аутоиммунные заболевания, генетические дефекты иммунной системы и пр. Клинически лейкопения проявляется повышенной восприимчивостью организма к различным инфекциям, однако может протекать абсолютно бессимптомно. Уровень лейкоцитов измеряется при заборе венозной либо капиллярной крови утром натощак. Для коррекции данного лабораторного отклонения проводится лечение основного заболевания.
Классификация
Низкий уровень белых кровяных телец может встречаться у абсолютно здоровых лиц – конституциональная безвредная лейкопения отмечается примерно у 2-5% людей. По происхождению патологические лейкопении разделяют на:
По патогенезу (механизму развития) различают лейкопении, возникшие вследствие:
В зависимости от типа клеток лейкоцитарного ряда выделяют следующие разновидности лейкопении:
Причины лейкопении
Инфекции
Одна из наиболее распространенных причин лейкопении – вирусные и генерализованные бактериальные инфекции. Патогенез снижения уровня лейкоцитов может быть различным – непосредственное повреждение клеток лимфотропными вирусами (ВИЧ, Варицелла-Зостер, корь), подавление образования в костном мозге, усиленная их потеря с экссудацией.
Прием лекарственных препаратов
К развитию лейкопении способен привести широкий спектр лекарственных средств. Известно два основных механизма лекарственно-индуцированной лейкопении: токсическое повреждение костного мозга, ведущее за собой нарушение кроветворения, и образование иммунных комплексов, в результате чего вырабатываются антитела, атакующие собственные лейкоциты макроорганизма.
Лейкопения возникает в среднем на 15 сутки от начала приема лекарства. Степень тяжести может быть самой различной – от незначительного снижения количества белых кровяных клеток до агранулоцитоза. В связи с поражением всех 3-х ростков гемопоэза часто встречается сочетание с анемией и тромбоцитопенией (панцитопения). В большинстве случаев достаточно отмены лекарственного препарата. При развитии агранулоцитоза может потребоваться применение колониестимулирующих факторов. Медикаменты, наиболее часто вызывающие лейкопению:
Аутоиммунные воспалительные заболевания
Причиной лейкопении могут быть аутоиммунные заболевания. В этих случаях преимущественно снижаются лимфоциты и нейтрофилы. Существует два основных патогенетических механизма аутоиммунной лейкопении – образование антилейкоцитарных антител и снижение экспрессии на мембранах иммунных клеток специальных белков (CD55, CD59), которые защищают клетки от цитолиза. Лейкопения обычно умеренная, регрессирует во время ремиссии или под влиянием патогенетического лечения. Лейкопенический синдром характерен для следующих патологий:
Болезни крови
Механизмов лейкопении при гематологических патологиях несколько – замещение кроветворной ткани злокачественными клетками, фиброзной или жировой тканью, синтез антилейкоцитарных антител, дефицит некоторых химических элементов для гранулоцитопоэза (железа, цианкобаламина, фолиевой кислоты):
Лучевая болезнь
Действие ионизирующей радиации неблагоприятно сказывается на всем организме человека. В первую очередь и сильнее всего страдают органы с высокой скоростью клеточного обновления, к которым относится костный мозг. Под влиянием гамма-лучей, имеющих высокую проникающую способность, гемопоэтические стволовые клетки утрачивают митотическую активность.
Это неизбежно приводит к падению в крови уровня лейкоцитов, а также тромбоцитов и эритроцитов. При острой лучевой болезни лейкопения наступает быстро, через 48-96 суток после облучения, при хронической – постепенно, в течение 1 года. Тяжесть лейкопении напрямую зависит от полученной дозы облучения. Восстановление числа кровяных клеток происходит медленно либо вовсе не наступает.
Наследственные формы лейкопений
К первичным лейкопениям относятся генетические заболевания, обусловленные мутациями генов, регулирующих созревание или дифференцировку лейкоцитов. Некоторые мутации приводят к изменению структуры лейкоцитарных антигенов, из-за чего они подвергаются аутоиммунному разрушению. В подавляющем большинстве случаев встречаются первичные нейтропении.
Дебют наступает с первых лет жизни. Часть из этих болезней имеет доброкачественную природу (циклическая нейтропения, первичная иммунная нейтропения, синдром «ленивых лейкоцитов», синдром Генслена), снижение количества нейтрофилов при них незначительное, присоединяющиеся инфекции протекают в легкой форме, лейкопения регрессирует самостоятельно.
Другие наследственные лейкопении часто сопровождаются инфекционными осложнениями, которые зачастую становятся фатальными уже в детском возрасте: болезнь Костмана (генетически детерминированный агранулоцитоз), первичные иммунодефициты (синдром Ди Джорджи, Вискотта-Олдрича), синдром Чедиака-Хегаси. При этих болезнях для восстановления нормальных значений лейкоцитов требуется специфическое лечение.
Другие причины
Диагностика
Лейкопения выявляется при клиническом исследовании крови. Ввиду многообразия этиологических факторов данного отклонения при его обнаружении следует обратиться к врачу-терапевту для тщательного сбора анамнеза, физикального осмотра, назначения дополнительного обследования:
Коррекция
Конституциональная лейкопения не требует никакого вмешательства. Если причиной развития данного отклонения стал лекарственный препарат, необходима срочная его отмена. При выраженном снижении лейкоцитов или агранулоцитозе прибегают к введению гранулоцитарного колониестимулирующего фактора (Г-КСФ) или инфузии донорских гранулоцитов. Главное условие успешности терапии – лечение основной патологии:
Прогноз
Некоторые формы первичных лейкопений характеризуются высоким уровнем смертности (50-90%) среди детей от инфекционных осложнений. При вторичных лейкопениях прогноз в большей степени зависит от основного заболевания. Поэтому при любом уровне снижения лейкоцитов в крови показано тщательное обследование, направленное на выяснение причины и своевременное начало лечения.
ТЕСТ НА ЛЕКАРСТВЕННУЮ НЕПЕРЕНОСИМОСТЬ (тест на активацию базофилов, CAST)
Опубликовано 23 Май 2018 пользователем admin
Горизонтальные табы
ОПИСАНИЕ:
Аллергия на лекарства является проблемой, которая актуальна как для врачей, так и для их пациентов. Именно на врачах лежит ответственность за назначение того или иного лекарственного препарата, а предвидеть развитие аллергических реакций на конкретное лекарство у конкретного человека можно не всегда.
В большинстве случаев пациенты сами принимают лекарства, активно рекламируемые по телевидению и отпускаемые в аптеках без рецепта врача. Именно эти лекарства представляют наибольшую опасность.
Так, у 90 % людей, страдающих лекарственной аллергией, её вызывают либо аспирин, либо сульфаниламидные препараты (триметоприм, септрин, бисептол), либо антибиотики (пенициллин, цефуроксим). Оценить истинную частоту встречаемости аллергических реакций трудно. Однако известно, что четверо из каждых десяти обычно перестраховываются, отвечая на вопрос о лекарственной аллергии, или путают аллергические реакции с какими-либо другими.
Аллергические реакции на лекарственные препараты по времени возникновения разделяют на два типа.
1. Немедленные, возникающие сразу после приема или введения лекарства. К ним относят анафилактический шок, крапивницу, аллергические отёки.
2. Замедленные, развивающиеся спустя несколько дней. Проявляются повышением температуры, крапивницей, болями в области суставов.
На сегодняшний день для диагностики лекарственной аллергии используются кожные или провокационные тесты, которые могут давать ложноположительный или ложноотрицательный результат. Именно для выявления лекарственной аллергии предназначен тест на активацию базофилов (CAST) с лекарственными препаратами пациентов.
ПОКАЗАНИЯ:
— для диагностики IgE-зависимой аллергии и псевдоаллергии, особенно лекарственной непереносимости, в случаях противоречивых или отрицательных результатов кожных тестов;
— для диагностики аллергической реакции на рентгенконтрастные вещества (коронарография, экскреторная урография и.т.д. манипуляции при которых используются рентгенконтрастные вещества).
ИНТЕРПРЕТАЦИЯ РЕЗУЛЬТАТОВ:
Положительно:
— повышение уровня индекса активации свыше 1,05, говорит о лекарственной непереносимости на данный препарат;
Отрицательно:
— отсутствие лекарственной непереносимости на конкретный препарат.
Провокационные тесты в аллергологии
В последние годы отмечается значительный рост аллергических заболеваний, особенно среди населения крупных индустриальных центров и мегаполисов, что диктует необходимость постоянного поиска новых диагностических приемов и методов лечения аллергии. Диагно
В последние годы отмечается значительный рост аллергических заболеваний, особенно среди населения крупных индустриальных центров и мегаполисов, что диктует необходимость постоянного поиска новых диагностических приемов и методов лечения аллергии.
Диагноз ставится на основании физикальных, а также лабораторных, инструментальных и других методов общеклинического и аллергологического обследования.
Особое место среди методов специфического аллергологического обследования занимают так называемые провокационные тесты, направленные на выявление ответной реакции на специфический раздражитель — аллерген.
Условия проведения аллергологического тестирования
Провокационные тесты с использованием аллергенов может проводить исключительно специалист — аллерголог-иммунолог, владеющий практическими навыками проведения подобных исследований, способный быстро и грамотно провести лечебные мероприятия при возникновении системных реакций.
Возможность развития системных реакций при проведении такого тестирования делает данную процедуру опасной, поэтому ее следует осуществлять только в условиях специализированного кабинета или стационара, оборудованных всем, что необходимо для купирования системных реакций. Провокационные тесты имеют свои показания и противопоказания, которые нужно учитывать при назначении подобных методов диагностики.
Наиболее распространенные методы аллергологического тестирования
Для проведения специфического провокационного тестирования используются стандартизированные лечебно-диагностические аллергены, прошедшие регистрацию в России и допущенные к применению. Основные группы лечебно-диагностических аллергенов, применяемых на данный момент в России для диагностики немедленной аллергии, следующие: пыльцевые аллергены; аллергены домашней и библиотечной пыли; аллергены клещей домашней пыли; аллергены эпидермиса животных; аллергены из пера и пуха птиц; пищевые аллергены; инсектные аллергены; бактериальные и грибковые аллергены.
Основная цель провокационных тестов — выявить наличие гиперчувствительности к тому или иному аллергену, установить ее степень, а также подобрать спектр аллергенов для дальнейшего проведения аллерген-специфической иммунотерапии.
При проведении тестирования производится нанесение на кожу или слизистые конъюнктив либо дыхательного тракта одного или нескольких разведений аллергена, после чего оценивается выраженность реакции в ответ на этот раздражитель. Основные методы провокационного аллергологического тестирования: кожный (в том числе аппликационный); назальный; конъюнктивальный; ингаляционный; сублингвальный.
Кожное тестирование
Кожное тестирование — наиболее доступный и высокоспецифичный метод выявления гиперчувствительности как немедленного, так и замедленного типа.
Данный метод тестирования имеет противопоказания, которые также необходимо учитывать и при применении других провокационных тестов.
Противопоказания к проведению кожного тестирования: обострение основного заболевания; тяжелое, нескомпенсированное течение бронхиальной астмы; острые интеркуррентные инфекции (ОРЗ, ангина, пневмония и др.); декомпенсация заболеваний внутренних органов (печени, почек, сердечно-сосудистой системы, эндокринной системы, крови и др.); обострение очагов хронической инфекции. Активная фаза хронических инфекционных заболеваний (туберкулеза, сифилиса, бруцеллеза и др.); аутоиммунные заболевания (СКВ, склеродермия, ревматоидный артрит, дерматомиозит и др.); злокачественные новообразования; психические заболевания; беременность и лактация; синдром приобретенного иммунодефицита.
С целью диагностики одной из самых распространенных форм немедленной аллергии — атопии — применяют скарификационные и prick-методы кожного тестирования. Для диагностики гиперчувствительности замедленного типа (ГЗТ) используют внутрикожные тесты с бактериальными и грибковыми аллергенами, для общей оценки ГЗТ возможно проведение кожных тестов с туберкулином и бруцеллином. Реакция оценивается через 24—48 ч. И в том и в другом случае используется тест-контрольная жидкость как отрицательный и раствор гистамина как положительный контроль.
Кожное тестирование с определенной долей вероятности может быть неинформативным (ложноположительные или ложноотрицательные результаты) по целому ряду причин — неправильное хранение аллергенов, снижение кожной реактивности, нарушения техники проведения кожного тестирования и др. Поэтому, как и другие виды провокационного тестирования, кожные тесты можно рассматривать в качестве уточняющего метода диагностики. При этом необходимо также учитывать, что по результатам кожного тестирования можно установить лишь наличие сенсибилизации (повышенной чувствительности организма к определенному аллергену). Для того чтобы поставить заключительный диагноз, необходимо установить четкую связь между наличием данной сенсибилизации и клиническими проявлениями заболевания, т. е. подтвердить, что именно этот аллерген ответственен за появление симптомов аллергии.
Для оценки степени чувствительности пациента к данному аллергену (а также с целью подбора начальной дозы лечебного аллергена для проведения аллерген-специфической иммунотерапии) проводится аллергометрическое титрование, т. е. тестирование с разными разведениями аллергена. Исследование осуществляют путем постановки кожных проб с различными разведениями аллергенов.
Кожные тесты можно проводить только с использованием специально разработанных диагностических аллергенов. Тесты с нанесением лекарственного препарата на кожу, внутрикожным или подкожным его введением с целью выявления лекарственной аллергии использовать не рекомендуется. Во-первых, это создает опасность возникновения системной реакции, а во-вторых, есть риск развития неспецифической местной воспалительной реакции, которая не может достоверно указывать на наличие или отсутствие аллергии.
Методика постановки кожных аллергологических проб
На кожу предплечья, предварительно обработанную спиртом, наносят каплю тест-контрольной жидкости, каплю 0,01% раствора гистамина, а также каплю аллергена (аллергенов). Раствор с гистамином является положительным контролем, а с тест-жидкостью — отрицательным. Расстояние между местами нанесения капель не менее 2,5-3 см. После этого производится повреждение эпидермиса в области каждой капли. При этом используют разные скарификаторы. Скарификацию также можно выполнять ланцетами — специальными скарификаторами с фиксированными на них аллергенами. При проведении prick-тестирования повреждение наносится посредством укола, при проведении скарификации — поверхностной царапины эпидермиса (при проведении этой процедуры важно не повредить кровеносные сосуды!). Реакции оценивают через 10–20 мин. Оценка скарификационных и prick-тестов по степени выраженности реакции приведена в таблицах 1 и 2.
Аппликационные кожные тесты
Аппликационные кожные тесты (patch-tests) применяются для диагностики контактного аллергического дерматита и фотодерматита. Для проведения тестирования используются стандартизированные диагностикумы для выполнения аппликационных тестов: медикаменты местного действия, металлы, компоненты резины, клеящие вещества, антимикробные средства, ароматизаторы и другие вещества. Реакция оценивается через 48–72 ч.
Назальный тест
Назальный тест применяют для диагностики аллергического ринита. В один носовой ход закапывают 1 каплю тест-контрольной жидкости. При отсутствии какой-либо реакции в другой носовой ход последовательно закапывают по 1 капле десятикратного разведения аллергена (1:100, 1:10), затем цельный аллерген. Интервал между закапыванием аллергена с более высокой концентрацией должен составлять не менее 20–30 мин. Увеличение концентрации аллергена производится только при отсутствии реакции на предыдущее разведение. Тест считается положительным при появлении симптомов ринита. Проявления ринита также можно зафиксировать при передней риноскопии.
Конъюнктивальный тест
Конъюнктивальный тест используют для диагностики аллергического конъюнктивита. В нижний конъюнктивальный мешок глаза закапывают тест-контрольную жидкость. При отсутствии реакции в другой конъюнктивальный мешок последовательно закапывают по 1 капле аллергена в двукратных разведениях (1:2048, 1:1024, 1:512 и т. д., до 1:2). Интервал между нанесениями аллергена с разными концентрациями не менее 20–30 мин. Увеличение концентрации аллергена производится только при отсутствии реакции на предыдущую концентрацию. Тест считается положительным при появлении симптомов конъюнктивита.
Ингаляционный тест
Ингаляционный тест применяют для диагностики бронхиальной астмы и проводят только в условиях стационара. Сначала оценивают показатели функции внешнего дыхания — ОФВ1 (первоначально не менее 70% от должных величин). Затем ингалируют контрольную жидкость. Ингаляции можно проводить с помощью дозирующего струйного ингалятора. При отсутствии реакции производятся ингаляции аллергена в двукратных разведениях (1:1024, 1:512, 1:256 и т. д., до 1:16). Через каждые 10 мин после очередной ингаляции регистрируется ОФВ1. При снижении показателя более чем на 20% тест считается положительным. После проведения теста пациент должен оставаться под наблюдением врача 24 ч. В течение одних суток возможно проведение ингаляционного теста только с одним аллергеном.
Сублингвальный тест
Сублингвальный тест применяют для диагностики лекарственной и пищевой аллергии. При наличии в анамнезе пациента тяжелых реакций, предположительно связанных с исследуемым препаратом или пищевым продуктом, предпочтительнее использовать лабораторные методы исследования. Перед началом тестирования измеряют ЧСС, АД, осматривают полость рта. Затем 1/8 (1/4) таблетки (или 2-3 капли растворенного лекарственного препарата) или натуральный пищевой продукт в разведении 1:10 помещают под язык пациента на 5–15 мин. Тест считается положительным при возникновении местной воспалительной реакции на слизистой оболочке полости рта или системной реакции. После тестирования больной должен находиться под наблюдением врача в течение суток. За этот период времени врач проводит мониторинг состояния сердечно-сосудистой и дыхательной систем пациента.
Реакции при проведении аллергологического тестирования
Возникновение местной аллергической реакции при проведении аллергологического тестирования является ожидаемой, однако, учитывая наличие провокации, подобный метод обследования сопряжен и с опасностью появления системных реакций, которые требуют принятия немедленных мер. Возникновение подобных осложнений при проведении тестирования возможно как в первые секунды (минуты), так и часы, а в некоторых случаях — и сутки.
Легкие признаки системной реакции: боли в суставах, головная боль, ощущение дискомфорта.
Умеренные признаки системной реакции: легкие проявления ринита, конъюнктивита или бронхиальной астмы (пиковая скорость выдоха не ниже 60% от должных величин или от показателя пациентов в период ремиссии). Симптомы хорошо контролируются соответствующими лекарственными препаратами (Н1-блокаторами или ингаляционными β2-агонистами).
Выраженные признаки системной реакции: крапивница, отек Квинке, нарушение бронхиальной проводимости (с показателем пиковой скорости выдоха ниже 60% от должной величины или от показателя пациента в период ремиссии), симптомы контролируются соответствующим лечением.
Угрожающие жизни состояния — анафилактический шок, отек жизненно важных органов (отек гортани) — требуют интенсивной терапии.
Основными причинами развития подобных реакций могут быть: несоблюдение требований, предъявляемых в отношении противопоказаний к провокационному тестированию; использование нестандартизированных аллергенов или препаратов, которые хранились без соблюдения соответствующих требований; нарушения технологии проведения тестирования; высокая индивидуальная чувствительность пациента.
Объем терапевтической помощи при возникновении системных реакций зависит от ее выраженности.
Во всех случаях возникновения системных реакций при проведении аллергологического тестирования необходима госпитализация для стационарного наблюдения и лечения пациента. Лечение тяжелых системных реакций необходимо проводить в условиях отделения реанимации и интенсивной терапии.
При возникновении системных реакций первое, что необходимо сделать,— прекратить введение (аппликацию, ингаляцию и т. д.) аллергенов. После этого следует начать проведение терапии, направленной на купирование реакции: введение системных антигистаминных препаратов (Н1-блокаторов), а также системных глюкокортикостероидов парентерально. В случае возникновения бронхообструктивного синдрома применяются β2-агонисты, холинолитики (ингаляционно), парентеральное введение метилксантинов, системных ГКС с учетом степени выраженности реакции.
Анафилактический шок — одно из самых серьезных проявлений аллергической реакции немедленного типа, сопровождающееся рядом системных нарушений и требующее оказания немедленной врачебной помощи. Время развития — от нескольких секунд до нескольких часов. Анафилактический шок может развиваться по разным сценариям. Клинические симптомы обусловлены сокращением гладких мышц, увеличением сосудистой проницаемости, дисфункцией эндокринных желез, нарушением свертываемости крови. Ведущими в клинической картине анафилактического шока являются кардиоваскулярные и респираторные нарушения, одно из которых может превалировать над другим.
В более легких случаях анафилактический шок начинается с появления предвестников — чувства тревоги, страха, слабости, ощущения жара. Могут появляться кожный зуд, высыпания по типу крапивницы, эритема, отек Квинке, осиплость голоса (вплоть до афонии), затруднение глотания, головокружение, головная боль, шум в ушах, онемение и покалывание пальцев, языка и губ, симптомы ринита и конъюнктивита, боли в животе, пояснице и в области сердца. При осмотре — бледность кожных покровов, иногда с синюшным оттенком. Наблюдаются одышка, стридорозное дыхание, хрипы; рвота, непроизвольная дефекация и мочеиспускание. Снижение АД на 30–50 мм рт. ст., тоны сердца глухие, пульс нитевидный. Тахикардия, тахиаритмия. Потеря сознания отмечается не сразу или вовсе не происходит.
При анафилактическом шоке средней степени тяжести указанные выше симптомы носят более выраженный характер. Потеря сознания происходит быстро, нередко отмечаются тонические и клонические судороги, холодный липкий пот, цианоз губ, расширение зрачков. Тоны сердца глухие, сердечный ритм неправильный, нитевидный, АД не определяется.
При тяжелом течении — развитие стремительное. Потеря сознания немедленная. Тоны сердца не выслушиваются, АД не определяется. Дыхание не выслушивается из-за полной обструкции дыхательных путей.
Лечебные мероприятия при возникновении анафилактического шока
Лечебные мероприятия при возникновении анафилактического шока должны проводиться незамедлительно. Ввести подкожно 0,3–0,5 мл 0,1% раствор адреналина. Место нанесения аллергена (по возможности) обколоть 0,1% раствором адреналина или норадреналина в дозе 0,1–0,3 мл с 4–5 мл физиологического раствора. Можно приложить лед. Необходимо начать внутривенное капельное введение: 300 мл 5% раствора глюкозы + 1 мл 0,1% раствора норадреналина. Альтернативно: введение допамина (от 300–700 мкг/мл, но не более 1500 мкг/мл) с постепенным снижением. При необходимости можно продолжать введение прессорных аминов (0,1% раствор адреналина подкожно) с интервалами 5–10 мин. Длительность введения определяется гемодинамическими показателями. Внутривенное капельное введение системных ГКС-препаратов: гидрокортизона 250 мг, или преднизолона 90–120 мг, или дексаметазона 8–32 мг. При возникновении бронхообструктивного синдрома ввести эуфиллин 10,0 мл 2,4% раствора в/в на физиологическом растворе. При отеке легких дозу ГКС можно увеличить, а также ввести в/в 0,5 мл 0,5% строфантина с 10 мл 40% глюкозы. При необходимости проводится: интубация или трахеостомия и перевод на ИВЛ, оксигенация — ингаляция увлажненного кислорода с помощью носового катетера (скорость — 5–10 л/мин). Применение диуретиков показано только при нормализации АД. При систолическом АД выше 90 мм рт. ст. могут быть введены антигистаминные препараты: тавегил — 2,0 мл. Осуществляется введение плазмозамещающих препаратов, жидкости в/в капельно или струйно. Возможно введение декстранов. Введение ГКС и антигистаминных препаратов продолжить до улучшения состояния пациента. Отмена вышеуказанных препаратов производится постепенно и сообразно объективным признакам стабилизации. Необходим постоянный мониторинг функции дыхательной и сердечно-сосудистой систем. Возможно развитие осложнений (инфаркт миокарда, отек легких, отек мозга и проч.).
Длительность лечения варьирует от нескольких часов до нескольких суток.
Таким образом, провокационное тестирование с использованием диагностических аллергенов продолжает оставаться важной, а в ряде случаев незаменимой частью специфического аллергологического обследования. Провокационные методы позволяют оценить аллергологический статус пациента, проводить подбор и оценку эффективности терапии, осуществлять динамическое наблюдение за состоянием пациента.
В последнее время во всем мире проводится работа, направленная на создание новых диагностических препаратов на основе аллергенов. Однако основной принцип подобной диагностики остается неизменным: назначение, проведение и оценка результатов провокационного аллергологического тестирования должны производиться исключительно специалистом — аллергологом-иммунологом.
Е. Н. Медуницына, кандидат медицинских наук НИИ аллергологии и иммунологии, Москва