Остеолиз
Полезное
Смотреть что такое «Остеолиз» в других словарях:
остеолиз — сущ., кол во синонимов: 3 • акроостеолиз (1) • остеоклазия (3) • размягчение (19) … Словарь синонимов
остеолиз — (osteolysis; остео + греч. lysis разложение, растворение) рассасывание ограниченного участка кости без последующего замещения другой тканью … Большой медицинский словарь
остеолиз травматический массивный — (osteolysis traumatica massiva; син.: Горхема болезнь, кость исчезающая, кость фантомная) обширный остеолиз в области перелома кости, возникающий как его осложнение … Большой медицинский словарь
Остеолиз (Osteolysis), Остеоклазия (Osteoclasia) — размягчение и разрушение кости в результате какого либо заболевания (чаще всего инфекционного) или нарушения кровоснабжения кости (ишемии). В случае акроостеолиза (acroosteolysis) поражаются концевые фаланги пальцев рук и ног:данный симптом… … Медицинские термины
ОСТЕОЛИЗ, ОСТЕОКЛАЗИЯ — (osteoclasia) размягчение и разрушение кости в результате какого либо заболевания (чаще всего инфекционного) или нарушения кровоснабжения кости (ишемии). В случае акроостеолиза (acroosteolysis) поражаются концевые фаланги пальцев рук и ног:данный … Толковый словарь по медицине
Ко́стная киста́ — (синоним киста кости) заболевание, характеризующееся образованием полости в костной ткани. В его основе лежит локальное нарушение внутрикостного кровообращения, активация лизосомных ферментов, которая приводит к деструкции глюкозаминогликанов,… … Медицинская энциклопедия
ОПУХОЛИ КОСТЕЙ МЕТАСТАТИЧЕСКИЕ — мед. Костные метастазы различных опухолей возникают гораздо чаще, чем первичные костные опухоли. Наиболее часто в кости метастазируют карциномы молочной железы, лёгкого, предстательной железы, мочевого пузыря, щитовидной железы, почек. 80%… … Справочник по болезням
СКЛЕРОДЕРМИЯ СИСТЕМНАЯ — мед. Системная склеродермия (СС) диффузное заболевание соединительной ткани, возникающее вследствие системной прогрессирующей дезорганизации соединительной ткани с преобладанием фиброзно атрофических изменений кожи и внутренних органов, а также… … Справочник по болезням
Остео́лиз прогресси́рующий — (спонтанное рассасывание костей, спонтанная абсорбция, злокачественная абсорбция костей, болезнь фантомной кости, болезнь исчезающей кости, эссенциальный остеолиз) редкое заболевание, характеризующееся спонтанным прогрессирующим рассасыванием… … Медицинская энциклопедия
Бондронат — Действующее вещество ›› Ибандроновая кислота* (Ibandronic acid*) Латинское название Bondronat АТХ: ›› M05BA06 Ибандроновая кислота Фармакологическая группа: Корректоры метаболизма костной и хрящевой ткани Нозологическая классификация (МКБ 10)… … Словарь медицинских препаратов
Лизис костной ткани что это
Дегенеративно-дистрофическая деструкция. При ней замещающим субстратом является фиброзная, неполноценная остеоидная ткань с участками кровоизлияний и некроза, окрашенными в темно-коричневый цвет (бурая опухоль). К этой группе деструкции относятся: киста, гиганто-клеточная опухоль (остеобластокластома) и множественные кисты при болезни Реклингаузена. Рентгенологическая картина при этих процессах проявляется наличием деструктивного симптомокомплекса.
При солитарной кисте выявляется единичный круглый очаг или фокус деструкции округлой формы, окаймленный со всех сторон склеротизированной костной каемкой, иногда имеющей крупноячеистый рисунок из-за наличия внутренних перекладин.
Отличие болезни Реклингаузена от солитарной кисты только в том, что первая имеет множественность поражений и в деструктивных очагах чаще не бывает перекладин, т. е. полости большей частью с однородным рисунком.
При гигантоклеточной опухоли (остеобластокластоме) будет выявляться одиночный крупный фокус деструкции в метаэпифизарном отделе кости с множественными крупными ячейками (в виде мыльных пузырей) — ячеистая форма; или в виде краевого деструктивного дефекта с четко ограниченными контурами — литическая форма остеобластокластом.
Деструкция от вытеснения. При ксантоматозе, главным образом в плоских костях, особено в черепе, будут выявляться множественные очаги деструкции в виде сплошных дефектов с изъязвленными контурами различной формы и величины без признаков периостальной реакции.
Рентгенологическая картина остеолиза такая же, как и при деструкции, она проявляется просветлениями различной формы и величины. Характерная особенность остеолиза в его локализации, т. к. остеолизу подвергаются самые периферические и свободные участки скелета: ногтевые отростки, суставные концы костей, а деструкция располагается в любом отделе кости. При остеолизе рассасывается вся кость: корковый слой, губчатая кость и субхондральная пластина.
Патоморфологической основой остеонекроза является гибель костных клеток при сохранении плотного промежуточного вещества, в связи с чем плотные элементы в некротическом участке преобладают, и на единицу веса мертвой кости минерального остатка приходится больше, чем живой. Некроз участка кости наступает в результате недостаточного или полного прекращения кровоснабжения, а живая костная ткань, окружающая омертвевший участок, обычно гиперемирована и процессы всасывания в ней усилены по сравнению с нормой.
Различают септический и асептический остеонекрозы. Асептические некрозы наблюдаются при остеохондропатиях или деформирующих артрозах, при тромбозах и эмболиях, возникающих у работников определенных профессий (кессонщиков, водолазов, высотников).
Лизис костной ткани что это
Родовые повреждения головы, несмотря на то, что они сопровождают человечество на протяжении всей его истории, по-прежнему относятся к одной из главных причин детской смертности и инвалидности. Наиболее частым маркером повреждения головки ребенка в родах является кефалогематома [5].
Кефалогематома (поднадкостничная гематома, ПНГ) – скопление крови в пространстве, сформированном кровью между костью и отслоенной от нее надкостницей. По различным данным, встречается у 0,2–3 % новорожденных. Своеобразие проблемы родовой травмы головы обусловливают анатомо-физиологические особенности новорожденного. К моменту родов голова плода является наибольшей по окружности частью его тела. Например, у доношенного новорожденного она составляет 33–37,5 см, что на 1–2 см больше окружности грудной клетки. Именно голова плода чаще всего формирует родовой канал. Поэтому даже во время физиологических родов она подвергается максимальному механическому воздействию со стороны естественных сил изгнания и сопротивления родового канала [3]. Основным механизмом образования кефалогематомы у новорожденного является смещение кожи и надкостницы головы во время продвижения плода по родовым путям и его обратного хода между схватками. В период «изгнания» плода голова совершает не только движения вперед и назад, но и вращательное движение, что является наиболее травматичным. Источником кровотечения являются сосуды поднадкостничного пространства, реже внутрикостные сосуды в области переломов костей черепа, которые встречаются у 10–25 % детей с ПНГ.
К основным факторам патогенеза образования кефалогематом относятся:
– Механический фактор: он обозначен преобладанием сцепления надкостницы с тканями родового канала над связями периоста и кости головы плода. Механическое повреждающее действие на плод оказывают чрезмерная сила маточных сокращений, затяжные роды, поступательное и вращательное движения головки плода во время прохождения ее по родовым путям.
– Гидравлический фактор: включает в себя раннее отхождение околоплодных вод, являющихся амортизатором, защищающим голову плода.
– Разница атмосферного и внутриматочного давлений оказывает присасывающее действие на кровь и тканевую жидкость, что усугубляется при операции кесарева сечения, вакуумной экстракции, стремительных родах.
– Анатомический фактор: включает в себя застой крови в результате патологии пуповины (короткая пуповина, перегиб или натяжение пуповины, обвитие шейки плода) [1].
Внешне ПНГ проявляются в виде локальной выпуклости чаще в теменной области с четкими границами по краю кости. Сначала ПНГ плотная, в дальнейшем определяется флюктуация и пальпируется валик по периферии ПНГ, что часто создает ложное впечатление о наличии вдавленного перелома в этой зоне. По данным авторов, около 80 % ПНГ значительно уменьшаются в первую неделю жизни ребенка и рассасываются обычно в течение 2–3 недель [2]. Если же этого не происходит, кефалогематома начинает оссифицироваться. Обычно через 4 недели после рождения кефалогематома, которая или совершенно не уменьшилась в размерах, или уменьшилась незначительно, начинает по периферии покрываться костной плотности капсулой и в конце концов полностью инкапсулируется.
Наиболее благоприятный вариант, когда образуется гиперостоз на месте окостеневшей кефалогематомы. С внутренней поверхности надкостницы остеобласты образуют сначала остеоидную капсулу. Затем начинается прорастание соединительной ткани в полость кефалогематомы и где есть еще жидкая кровь или фибриновые сгустки, с постепенной рубцовой организацией кефалогематомы и в отдельных случаях – окостенением.
В ряде случаев параллельно процессу инкапсуляции идет резорбция подлежащей кости с образованием в ней сквозных дырчатых дефектов. В некоторых случаях, где-то в возрасте около года, эта капсула постепенно рассасывается и остается сквозной дефект в черепе.
По данным различных авторов, оссификация кефалогематом колеблется в диапазоне от 7,3 до 50 %. При этом в 48,3 % наблюдений под оссифицированной гематомой выявляются дефекты кости до твердой оболочки мозга [4].
Спорным остается вопрос о тактике лечения ПНГ. По мнению ряда авторов, в подавляющем большинстве случаев кефалогематомы требуют лишь консервативного лечения. Хирургическое лечение – пункционное удаление – оправдано только у тех новорожденных, у которых гематомы сопровождаются грубым косметическим дефектом (распространение на лицевую часть головы и/или очень большие ее размеры – «обезображивающие» кефалогематомы, без тенденции к уменьшению ее размеров к 10 дню жизни. Ряд авторов призывает к более активному хирургическому лечению кефалогематом в остром периоде, причем пункцию целесообразно выполнять после первой недели жизни, когда проходит «физиологическая» подверженность кровотечениям.
Несмотря на большую распространенность кефалогематом, отсутствует единое представление и единая схема в определении показаний к хирургическому (пункционному) лечению.
Иллюстрацией одного из вариантов клинического течения кефалогематом может служить следующее наблюдение.
Девочка К.Е., 28 дней, находилась на стационарном лечении в отделении нейрохирургии БУЗОО ГДКБ № 3 г. Омска с диагнозом: кефалогематома правой теменной области. При обращении родители высказывали жалобы на наличие у ребенка большой припухлости на голове справа. Из анамнеза известно, что ребенок от первой беременности, протекавшей на фоне анемии беременной. Роды естественные, в сроке 40 недель, закричала сразу. Околоплодные воды светлые. Масса при рождении – 3350 г, рост – 51 см. К груди приложена в родзале, сосала активно. При рождении констатирована кефалогематома, которая со слов матери в течение первых трех дней увеличивалась. Из роддома выписана на 5 сутки. Участковый педиатр рекомендовала выжидательную тактику.
В возрасте 21 дня родители обратили внимание, что кефалогематома стала плотноватой, размеры ее с момента родов не уменьшились. Ребенок был направлен на консультацию к нейрохирургу. При осмотре: в соматическом и неврологическом статусе патологических проявлений не выявлено. В правой теменной области визуализируется обширная кефалогематома, размерами 10×12×4 см, поверхность которой пальпаторно плотная с ощущением эластической упругой мембраны по типу «пергаментного треска», выраженным валиком оссификации по периферии. Окружность головы 37 см.
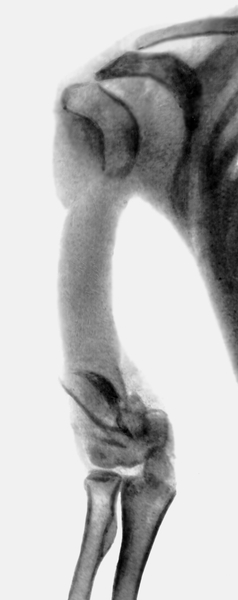
Перед пункционным лечением проведен обязательный диагностический минимум: общий анализ крови, общий анализ мочи – в пределах возрастной нормы. Нейросонография – на момент исследования срединные структуры мозга не смещены, ликворная система не расширена, УЗ-данных в пользу внутричерепной гематомы не получено. В правой теменной области визуализируется кефалогематома максимальной толщиной 20 мм, эхоструктура ее жидкостная, неоднородная. В прилежащей костной структуре кортикальный слой неровный. Рентгенография черепа в двух проекциях – справа в теменной области мягкотканая тень, справа покровная кость истончена, разволокнена с неровными контурами, структура кости разряжена, неравномерная по плотности с неровным внутренним контуром. Дважды с интервалом в один день, под местной анестезией проведена пункция кефалогематомы, удалено соответственно 15 и 8 мл жидкой лизированной крови. Процедуры ребенок перенес удовлетворительно. После серии пункций напряжение и размеры кефалогематомы значительно уменьшились, поверхность приобрела волнистый, кратерообразный вид. Через 2 недели при контрольном осмотре констатировано некоторое сглаживание бугристой поверхности кефалогематомы. В соматическом и неврологическом статусе патологических изменений не обнаружено. Проведена нейросонография – вещество головного мозга без структурных изменений, в теменной области справа в мягких тканях визуализируется жидкостное образование 40×6 мм, в прилежащей костной структуре кортикальный слой неровный, прерывистый от 4 до 11 мм (остеомаляция?). Проведена мультиспиральная компьютерная томография – в правой теменной кости определяется локальное истончение кости с неправильной формы дефектом, поперечным размером 16 мм и продольным размером 40 мм. Над этой зоной в мягких тканях волосистой части головы определяется уплотнение, примыкающее к кости, расположенное под подкожно-жировой клетчаткой, размерами до 43×21×3 мм, плотностью 78 ед. Н – кефалогематома.
Отмечено расширение субарахноидальных пространств больших полушарий головного мозга. Объем желудочков мозга не изменен. Смещения срединных структур нет.
Контрольный осмотр ребенка в возрасте 2 месяцев. Активно жалоб мать не предъявляет. В соматическом статусе без особенностей. В неврологическом статусе: взгляд фиксирует, за игрушками следит, на звуковые раздражения реагирует. Зрачки равновеликие, реакция на свет живая. Активные движения в конечностях сохранены. Сухожильные и периостальные рефлексы с рук средней живости, с ног оживлены. Рефлекс Бабинского с обеих сторон. Местно: окружность головы 40 см, большой родничок 1,5×1,5 см, мягкий, пульсацию мозга передает. Кефалогематома практически не визуализируется, в правой теменной области при пальпации определятся участок вдавления кости 1,1×1,5 см. Проведена нейросонография – структурных изменений вещества головного мозга нет, в правой теменной области в костной структуре кортикальный слой неровный, прерывистый от 3 до 7 мм, остеомаляция.
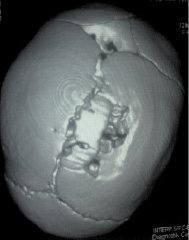
Рис. 1. МСКТ в режиме 3D костной реконструкции. Просматривается дефект в правой теменной кости
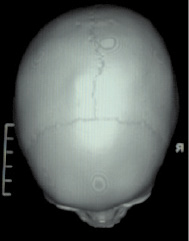
Рис. 2. МСКТ в режиме 3D костной реконструкции (контроль через год). Дефект в правой теменной кости не просматривается, костной деструкции нет
В течение года проводилось динамическое наблюдение за ребенком, проводилась нейросонография. В неврологическом статусе изменений выявлено не было. Через один год проведена контрольная МСКТ – кости свода и основания черепа не изменены, дефекта правой теменной кости не определяется. Срединные структуры не смещены. Локальное расширение субарахноидального пространства конвекситально справа до 2–3 мм, боковые желудочки симметричные, не расширены. Третий, четвертый желудочки не изменены. Зон патологической плотности в веществе головного мозга и его оболочках не найдено.
Таким образом, костный дефект после кефалогематомы оссифицировался самостоятельно, не требуя пластического закрытия.
Противоречивость точек зрения на выбор методик лечения кефалогематом во многом объясняется отсутствием общепринятой универсальной классификации этого заболевания и, естественно, сопряженных с ней алгоритмов лечебных действий. Неудаленная кефалогематома больших размеров влияет не только на местном уровне, рассасывая подлежащую черепную кость, но воздействует и на общее состояние новорожденного. Помимо локальных костных изменений поднадкостничная гематома может осложнять течение раннего перинатального периода и приводить к отдаленным последствиям. К наиболее частым осложнениям относят развитие желтухи у новорожденных в раннем неонатальном периоде, формирование анемизации, вследствие скопления значительного объема крови в кефалогематоме. Описаны различные формы гнойно-септической инфекции, развившиеся из-за инфицирования кефалогематомы. Ряд авторов считают, что кефалогематома может быть одним из косвенных признаков родовой травмы центральной нервной системы. Ее наличие сопряжено с нарушением гемодинамики не только в покровах черепа, но и в головном мозге новорожденного, что не может не отразиться на его состоянии. Достаточно часто кефалогематома сочетается с другими родовыми повреждениями: внутричерепные кровоизлияния, переломы черепа, переломы ключицы, повреждения шейного отдела позвоночника [6].
В настоящее время становится все более очевидным, что оставлять кефалогематому нельзя – она должна быть эвакуирована с наложением давящей повязки. Современные методы диагностики доказывают оправданность активной хирургической тактики в отношении детей с кефалогематомами. Пункционная аспирация содержимого кефалогематомы имеет лечебную и в большей степени профилактическую направленность, так как предсказать естественную эволюцию кефалогематомы у каждого больного довольно трудно.
Рецензенты:
Бочарников Е.С., д.м.н., профессор кафедры детской хирургии, ГБОУ ВПО ОмГМА, г. Омск;
Чернышев А.К., д.м.н., профессор кафедры детской хирургии, ГБОУ ВПО ОмГМА, г. Омск.
Боль в костях при остеопорозе
Поделиться:
Остеопороз — заболевание, приводящее к разрушению костной ткани, первым признаком которого является боль в костях. Его причина — нарушения обмена веществ, поэтому при костных болях неясного происхождения можно уточнить диагноз при помощи анализов крови.
Куда девается кальций
Кость состоит из сетчатого белкового «скелета», в ячейки которого откладываются соли кальция и фосфора. Именно этим объясняется ее прочность: если бы кость была просто твердой, она оказалась бы хрупкой, как фарфор, но белковая основа сообщает ей необходимую гибкость. В процессе развития человека — начиная еще с внутриутробного периода — формируется сперва гибкая «матрица» будущей кости, а кальцием она наполняется уже позже. Уровень насыщенности кости кальцием различается в разные периоды жизни. Отчего это зависит?
Дело в том, что обеспечение твердости нашего скелета — не единственная забота кальция. Он необходим для сокращения мышц — в том числе и сердечной. Поэтому понижение уровня кальция в крови ниже некоего «прожиточного минимума» совершенно справедливо рассматривается организмом как ситуация, угрожающая жизни. А скелет — это огромный «запас» кальция, из которого его при необходимости можно брать.
Читайте также:
Психогенная боль в спине
Костный «индикатор»
Регуляцией уровня кальция в крови занимаются два гормона: кальцитонин (его выделяет щитовидная железа) и паратгормон (продукт паращитовидных желез — маленьких образований на задней поверхности щитовидной железы). Если кальция в крови достаточно, кальцитонин «загоняет» его в кости. Но если уровень этого металла в крови падает, паратгормон «вытаскивает» его из костной ткани, чтоб не остановилось сердце.
Очевидно, что при нарушениях в выработке этих гормонов непременно возникнут симптомы со стороны костей, причем зачастую они бывают одними из первых. В зависимости от характера гормональных нарушений выделяют следующие виды остеопороза.
Тиреоидный остеопороз
Тут все несложно. Гипофункция щитовидной железы — недостаток кальцитонина: кальция много в крови, а в кости он не попадает, развивается остеопороз. Кроме ноющих неясных болей в костях снижение функции нашего «щита» проявляется и другими симптомами: вялость, слабость, ощущение общей заторможенности, сухость и бледность кожи, ломкость волос, отечность лица, урежение пульса, снижение иммунитета. Уточнить диагноз поможет анализ крови на тиреотропный гормон (ТТГ) в комплексе с кальцитонином. ТТГ изменяется и в случае понижения, и в случае повышения функции щитовидной железы, поэтому начинать обследование нужно именно с него, а не с визуализационных методов (УЗИ).
Паратиреоидный остеопороз
Здесь все наоборот. Паратгормон, как мы помним, «выгоняет» кальций из костей в кровь. При гиперфункции паращитовидных желез паратгормона слишком много, он действует очень активно, что опять способствует развитию остеопороза. Однако избыток кальция в крови тоже ни к чему хорошему не приводит. Чрезмерно длительные сокращения — спазмы — гладкой мускулатуры кишечника вызывают запоры и боли в животе. Почки, пытаясь вывести избыток кальция, работают «на износ», в них могут появляться камни-кальцинаты, мочевыделение увеличивается и ощущается сильная жажда. Разобраться в такой ситуации помогут анализ крови на кальций и фосфаты и определение кальция в суточной моче.
Эстрогензависимый остеопороз
Опосредованно на уровень кальция влияют также женские половые гормоны — эстрогены. Именно поэтому их снижение в перименопаузальном периоде может приводить к развитию остеопороза.
Воздействие эстрогенов на костную ткань — сложный многоступенчатый процесс. Интересно, что эти гормоны влияют не только на обмен кальция, но и на общее состояние «белкового скелета». С точки зрения природы все довольно логично: юная девушка (с высоким уровнем эстрогенов) должна быстро залечивать любые травмы, а вот немолодой, которая уже выполнила репродуктивную функцию, такая способность как бы уже не обязательна. Против природы не пойдешь, однако нам не хочется соглашаться с природными механизмами.
Поэтому всем женщинам, вступающим в пременопаузу, рекомендуется обсудить со своим гинекологом вопрос профилактики остеопороза — она куда эффективнее лечения. Основные анализы, которые может назначить врач: определение в крови кальция и костной фракции щелочной фосфатазы и количество кальция в суточной моче.
Любые подозрения на остеопороз должны быть подтверждены денситометрией — измерением плотности костной ткани. Наиболее точным вариантом является двуэнергетическая рентген-денситометрия. Как любой рентгеновский метод, она не совсем безвредна, однако существует альтернатива — УЗ-денситометрия. Так что поставит диагноз в любом случае несложно — главное сделать это вовремя.
Научная электронная библиотека
1.1. Особенности метаболизма костной ткани
В филогенетическом аспекте кость является самой молодой тканью. Она до сих пор находится в периоде адаптации к существованию в условиях гравитации. Кроме того, скелет человека подвержен воздействию такого фактора, как прямохождение, а в последние столетия претерпевает изменения, связанные с гипокинезией и различными вынужденными положениями.
В морфофункциональном отношении кость является одной из наиболее сложных и биологически активных тканей. По многим показателям она превосходит другие системы организма и является наиболее массивной, многофункциональной, обладает высокой метаболической и репаративной активностью. Костная ткань в разных участках на 20–25 % состоит из органического матрикса. Около 60–65 % массы сухого деминерализованного матрикса приходится на коллаген и 17–18 % на неколлагеновые белки, по своей структуре, являющиеся гликопротеинами. В состав стромы костного мозга входят недифференцированные стволовые мезенхимальные клетки – ретикулярные, соединительнотканные, эндостальные фибробластоподобные, эндотелиальные клетки, адипоциты, дифференцированные костные клетки (остеобласты, остеокласты, остеоциты), межклеточное вещество, клетки эндоста и периоста, костный мозг, сосудистые, лимфатические и нервные образования, интимно связанные с окружающими мягкими тканями [13, 28, 36, 52].
В костной ткани постоянно протекают два противоположно направленных процесса – резорбция и новообразование. Соотношение этих процессов зависит от различных факторов, в том числе от физических нагрузок на кость и возраста. Считается, что остеогенез происходит за счет клеток эндоста, периоста и костного мозга. Процесс физиологического ремоделирования губчатой костной ткани проходит несколько фаз, в каждую из которых ведущую роль выполняют те или иные клетки. Первоначально участок костной ткани, подлежащий резорбции, «помечается» остеоцитами при помощи специфических цитокинов (активация), разрушается протективный слой на костном матриксе. К оголенной поверхности кости мигрируют предшественники остеокластов и сливаются в многоядерную структуру – симпласт – зрелый остеокласт. Затем остеокласт деминерализует костный матрикс (резорбция), уступает место макрофагам, которые завершают разрушение органической матрицы межклеточного вещества кости и подготавливают поверхность к адгезии остеобластов (реверсия). На последнем этапе в зону разрушения прибывают предшественники, дифференцирующиеся в остеобласты, они синтезируют и минерализуют матрикс в соответствии с новыми условиями статической и динамической нагрузки на кость (формирование) [9, 14, 19, 45].
Регуляция остеогенеза имеет три уровня: локальный (местный), системный и генетический. Это обстоятельство в конечном итоге обеспечивает высокий уровень метаболизма костной ткани.
Локальную регуляцию осуществляет микроокружение посредством различных цитокинов, большим количеством факторов роста, рядом полипептидов, ферментов, межклеточных контактов.
Системная нейроэндокринная регуляция осуществляется гормонами и веществами с гормоноподобным действием. Наиболее изученными являются паратиреоидный гормон, половые гормоны, метаболиты вит. D, кальцитонин, глюкокортикоиды, тиреоидные гормоны [9, 52]. Морфофункциональная связь остеогенеза и кровообращения осуществляются не только анатомически, но и тесно функционально. Это подтверждено многочисленными исследованиями связей внутрикостной и внекостной системы артериального, венозного, лимфатического русла, нервной регуляции с остеорецепцией.
Красный костный мозг является депо крови, органом кроветворения, высокочувствительной рефлексогенной зоной, центральным звеном иммунной системы. Красный костный мозг – это источник практически неистощаемого пула мезенхимальных стволовых фибробластоподобных клеток – предшественников остеобластов, способных не только потенцировать остеогенез, но и строить кроветворное микроокружение и регулировать собственно кроветворение [49].
Нарушение процесса остеогенеза приводит к патологии. Исследования В.М. Чепоя (1978) с применением радиоактивного пирофосфата технеция показали, что при межпозвонковом остеохондрозе в телах позвонков отмечается значительное ослабление фибробластических процессов и усиление остеокластических изменений. Кость становится разреженной и хрупкой, как в старческом возрасте, т.е. развивается остеопороз. По мнению McMahon et al. (2002) дефицит в остеогенезе карбоангидразы-2 приводит к появлению симптомов остеосклероза.
По данным С.В. Либенсона (1989) при гипокинезии происходят существенные изменения в системе регуляции остеогенеза, выражающиеся в гипокальцемии, увеличении содержания паратгормина и кальцитонина в крови, гиперэкскреции с мочой минеральных и органических компонентов, участвующих в остеогенезе. Подобные же изменения автор наблюдал и при хроническом болевом синдроме.
Репаративная регенерация – это восстановление ткани после повреждения. Механизмы физиологической и репаративной регенерации костной ткани качественно едины, осуществляются на основе общих закономерностей. Репаративная регенерация – есть в той или иной мере усиленная физиологическая [34]. Одними из индукторов репаративной регенерации костной ткани и усиления метаболизма являются ее травматическое повреждение [10, 34], а также метод аутотрансплантации красного костного мозга, как источника мезенхимальных стволовых клеток – предшественников фибробластов.
Многие исследователи указывают на возможность локально возбуждать репаративную регенерацию костной ткани, тем самым изменять ее метаболизм, методом остеотомии, трепанации, туннелизации или перфорации в необходимых участках кости. Локализованная и дозированная альтерация костной ткани применяется, как средство терапевтического воздействия и приводит к купированию дегенеративно-дистрофических нарушений. Лечебный эффект проявляется местно в зоне стимуляции и регионарно в сегментарных областях за счет интенсификации гемоциркуляции [10, 32, 34].
Микротравматическое повреждение костной ткани приводит к возникновению остеоиндуктивного сигнала, который осуществляется морфогенетическим белком-2, при этом, как в костной ткани, так и в кровеносной системе, происходит стремительная активация ростовых факторов (инсулиноподобного фактора роста, фактора роста фибробластов, колониестимулирующего фактора, фактора некроза опухоли-α и т.д.) [6].
Индуцированный фактор некроза опухоли человека (hTNF)-α стимулирует образование одноядерных преостеокластоподобных клеток (POCs), увеличивает число мРНК рецепторов кальцитонина (CTR) в POCs, формирует образование колонийстимулирующего фактора макрофагов (M-CSF) и экспрессирует образование мРНК активатора ядерного фактора Каппа В лиганда (RANKL). Совместное влияние стволовых клеток красного костного мозга и hTNF-α с растворимым RANKL увеличивают образование многоядерных остеокластоподобных клеток (MNC-s) из макрофагов, осуществляя лизис и резорбцию перелома. RANKL не только участвует в сигнальной трансдукции преостеокластов и остеокластов, но и в резорбтивной функции и выживании зрелых остеокластов [50]. Сигнальные механизмы RANKL распространяются и на активируемые митогенами протеинкиназы – нейроэндокринный уровень регуляции [50]. HTNF-α, простагландин Е2 (PGE2), паратгормон (PNG), 1, 25 (ОН) 2 витамин D3 индуцируют образование интерлейкина 11 (IL-11), интерлейкина 11R (IL-11R) и гликопротеина (gp 130) остеобластами за счет мРНК.
Основной фактор роста фибробластов (bFGF) увеличивает в ККМ количество остеобластов и стимулирует образование белкового матрикса, ускоряя минерализацию и снижая уровень свободного фосфата.
При повреждении кости в красном костном мозге, так же экспрессируется мРНК фактора роста эндотелия сосудов (VEGF) с рецепторами. Ангиобласты способствуют окружению поврежденной зоны капиллярами. Действие механического повреждения может быть потенцировано введением аутологичных стволовых клеток костного мозга [36].
Особый интерес вызывают работы о применении внутрикостной трансплантации аллогенного костного мозга для лечения экспериментального сенильного остеопороза. В этом случае остеоиндуктивный сигнал осуществляется морфогенетическим белком-2 и макрофагами [25, 50]. Аденозинтрифосфат (АТФ) так же участвует в передаче сигналов факторов роста ККМ за счет повышения активности протеинкиназ. Таким образом, существенно усиливается метаболическая активность костной ткани.
Янковский Г.А. (1982) привел результаты лечения 135 больных пояснично-крестцовым радикулитом методом введения 1 мл изотонического раствора натрия хлорида в остистые отростки нижних поясничных позвонков. У 122 пациентов автор отметил значительный регресс неврологической симптоматики и в течение последующих 2-х лет у этих больных поясничные боли не отмечались. При рентгенденситометрии у данных пациентов было выявлено увеличении плотности костной ткани. Автор сделал вывод, что внутрикостная пункция остистого отростка вследствие общности кровообращения обуславливает улучшение трофики тела позвонка и, соответственно, межпозвонкового диска.
При гистологическом исследовании костной ткани И.Н. Атясовым (2000) после проведения внутрикостного введения 10 мл различных жидкостей или крови в 1 сутки определялось разрушение костных трабекул, повреждение стромы и паренхимы костномозговой ткани, нарушение кровообращения в очаге деструкции, что являлось следствием механического повреждения в момент внедрения иглы в кость.
Через 3 суток на месте внутрикостного вливания 10 мл жидкости наблюдалось разрастание нежноволокнистой ткани и гиперплазия эндостальных элементов в виде окружения близлежащих к очагу деструкции костных трабекул остеобластами, а в некоторых опытах (после внутрикостного введения лекарственных жидкостей вместе с аутологичным костным мозгом) – уже было видно образование и разрастание остеоидных балочек.
Через 5 суток разросшаяся нежноволокнистая ткань почти полностью замещала очаг кровоизлияний, определялась резко выраженная гиперплазия соединительнотканных и эндостальных элементов в виде разрастания множества остеоидных балочек и напластования остеоидных масс на окружающие зрелые костные балки.
По истечении 7 суток в месте введения жидкости определялась нежно-волокнистая ткань, полностью замещающая очаг кровоизлияний.
Через 15 суток в нежно-волокнистой соединительной ткани определялись скопления лимфоидных и жировых клеток, множество зрелых костных балок с явлениями активной перестройки с помощью остеобластов и остеокластов.
На 18–20 сутки определялись участки фиброза.
В последующие 30–60 суток в месте введения иглы в кость отмечалась разросшаяся фибринозная ткань неравномерной плотности, окруженная костными балками, находящимися в стадии дальнейшей перестройки.
К 60 суткам костная и костномозговая ткани полностью восстанавливали свою клеточную структуру [2, 3].
Костная ткань – это главное депо минеральных солей в организме, по своей химической структуре представляет собой кристаллы гидроксиапатита, поэтому обладает физическими свойствами пьезоэлектрика. При одноостных сжатиях, изгибах или кручениях постоянно изменяется пьезоэлектрический потенциал как всей кости, так и отдельных ее составляющих элементов. В основополагающих работах Фукады и Ясуды (1957) было показано, что поляризация линейно связана с механическим напряжением и деформацией. В состоянии покоя на поверхности кости нет связанных поляризационных зарядов, вызванных собственными механическими напряжениями, т.к. они компенсируются ионами электролита. Механическая деформация кости определенным образом изменяет пьезоэлектрические потенциалы.
Так, на вогнутой поверхности образуется отрицательный, а на выпуклой – положительный заряд. Сочетание положительных и отрицательных потенциалов так же существенно влияет на процессы активации остеокластов, остеобластов и других клеток кости и костного мозга, на движение ионов и заряженных молекул по кровеносным сосудам.
На вогнутой поверхности стимулируется костеобразование, а на выпуклой – резорбция кости. Кроме того, кровотоком создается электрохимический потенциал. Совокупность электропотенциалов распределена в кости таким образом, что венулы заряжены преимущественно положительно, что, по-видимому, является биологически оправданным механизмом предотвращения зарастания костных каналов, в которых они проходят.
Однако при недостаточных механических нагрузках на кость, незначительном внутрикостном кровотоке, венозном застое изменяется соотношение разнополярных потенциалов. Положительный заряд венул уменьшается или превращается в отрицательный. Это способствует костеобразованию в месте их выхода. Уменьшается диаметр отверстия, в котором проходит венула, что ограничивает возможности резервного оттока, усиливает отек, замедляет отток крови от кости. Таким образом, замыкается патологический круг.




 Читайте также:
Читайте также: