Заместительная гормональная терапия для мужчин с возрастным андрогенным дефицитом
Специализация: урология, андрология
Синдром возрастного андрогенодефицита у мужчин — это нарушение биохимического баланса, возникающее в зрелом возрасте по причине недостаточности андрогенов в сыворотке крови, нередко сопровождающейся снижением чувствительности организма к андрогенам. Как правило, это приводит к значительному ухудшению качества жизни и неблагоприятно сказывается на функциях практически всех систем организма. Естественно, что огромный интерес вызывают вопросы терапии андрогенного дефицита, поскольку именно она ставит сложную задачу перед врачом-клиницистом: выбрать из широкого арсенала методов и препаратов гормональной терапии наиболее оптимальный, сочетающий в себе качество, эффективность, а также удобство в применении.
В настоящее время врачи-урологи и андрологи наиболее часто применяют заместительную терапию тестостероном. Данный метод позволяет решить целый ряд задач: снизить симптомы возрастного андрогенодефицита путем повышения либидо, общей сексуальной удовлетворенности, уменьшить выраженность либо полностью ликвидировать вегетососудистые и психические расстройства. Кроме того, если заместительная терапия тестостероном применяется более 1 года, у пациентов наблюдается повышение плотности костной массы, снижение выраженности висцерального ожирения, а также нарастание мышечной массы. Также после длительного курса лечения нормализуются лабораторные параметры: наблюдается повышение уровня гемоглобина или количества эритроцитов, снижение уровня ЛПОНП (липопротеинов очень низкой плотности) и ЛПНП (липопротеинов низкой плотности) при неизмененном уровне ЛПВП (липопротеинов высокой плотности). Многие авторы считают, что такого эффекта можно достичь, добившись восстановления концентрации тестостерона в крови до нормального уровня (10–35 нмоль/л). Следует также учитывать, что *17α-алкилированные препараты тестостерона флуоксиместеролон и метилтестостерон обладают выраженной гепатотоксичностью, оказывая токсическое и канцерогенное влияние на печень, а также отрицательно воздействуют на липидный спектр крови (резкое повышение уровня атерогенных и снижение уровня антиатерогенных липопротеидов). Поэтому применение этих производных тестостерона в клинической практике было прекращено.
В настоящее время из пероральных препаратов предпочтение отдается тестостерону ундеканоату (Андриол). Указанный эфир тестостерона не подвергается первичному печеночному метаболизму, так как всасывается в лимфатическую систему, минуя печень. После гидролиза тестостерона ундеканоата в лимфатической системе в системный кровоток поступает тестостерон, который оказывает лечебное действие как сам по себе, так и через свои основные метаболиты – дигидротестостерон (ДГТ) и эстрадиол, обусловливающие полный спектр андрогенной активности тестостерона. Таким образом, тестостерона ундеканоат сохраняет свою активность при пероральном применении. Вместе с этим, минуя систему воротной вены и прохождение через печень, тестостерона ундеканоат не оказывает гепатотоксического и гепатоканцерогенного действия. Период полувыведения препарата из плазмы составляет 3–4 часа. В связи с этим режимом дозировки тестостерона ундеканоата является 2-кратный прием в течение суток, это не всегда удобно для пациентов. Исходя из собственного опыта, мы считаем, что Андриол является достаточно мягким препаратом и помогает только в случаях начальных и минимальных проявлений возрастного андрогенного дефицита.
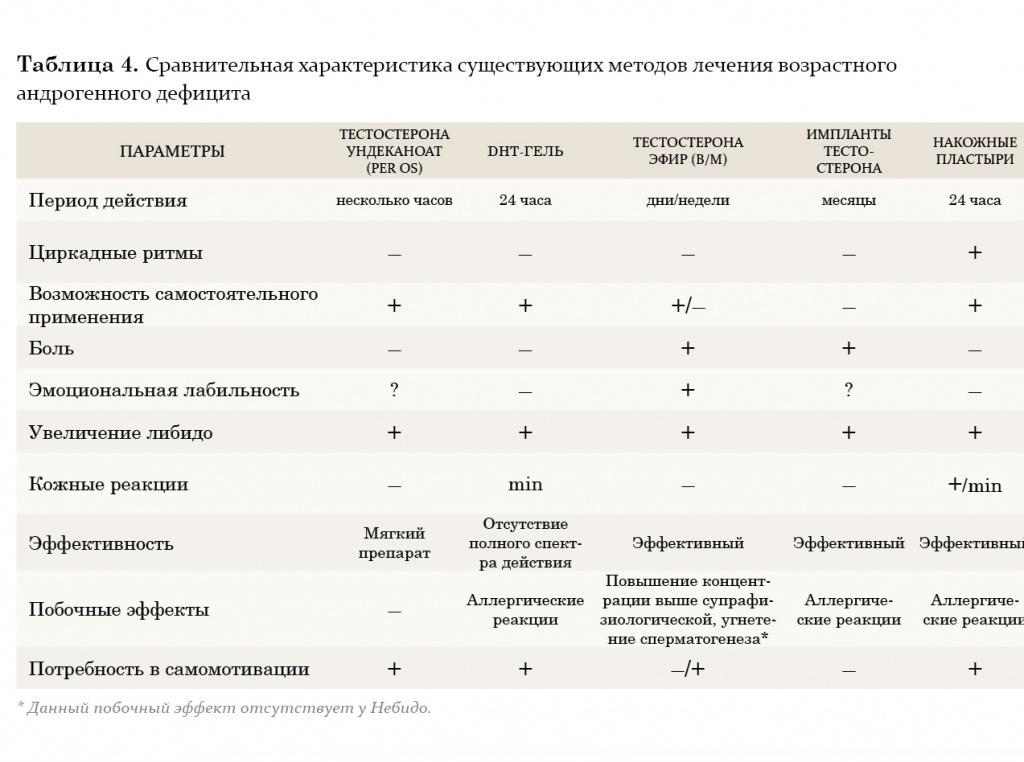
Внутримышечные инъекции пролонгированных эфиров тестостерона также являются широко применяемым методом заместительной терапии у мужчин с гипогонадизмом. Два наиболее известных эфира тестостерона – тестостерона ципионат и тестостерона энантат, имеют похожую фармакокинетику. При внутримышечном введении этих препаратов создается депо, из которого препарат высвобождается в кровеносное русло. В течение первых 2–3 дней после введения уровень тестостерона повышается до супрафизиологических цифр, а затем медленно снижается на протяжении последующих 2 недель до субнормальных значений. Положительной стороной этих препаратов является длительность терапевтического действия. Тем не менее резкие изменения в уровне тестостерона, зачастую ощущаемые самим пациентом в виде подъемов и снижения либидо, общего самочувствия, эмоционального статуса, являются нежелательными качествами данных препаратов. В связи с этим большие надежды возлагаются на новый препарат Небидо (Шеринг), фармакокинетика которого значительно отличается от других эфиров тестостерона. Небидо представляет собой тестостерона ундеканоат и является препаратом, не обладающим пиком повышения концентрации.
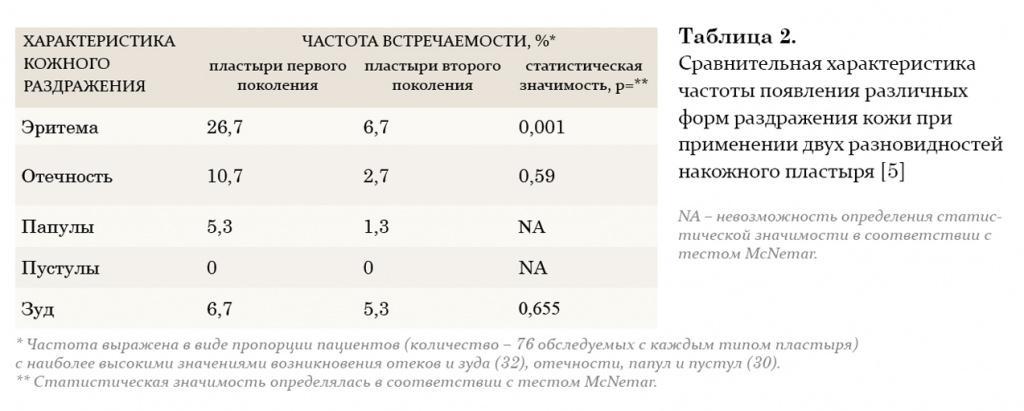
На протяжении двух последних десятилетий большое внимание уделяется исследованию преимуществ трансдермального применения препаратов тестостерона. Мошоночные пластыри обладают эффективным действием, и некоторые пациенты считают их наиболее удобным методом лечения. Накожные пластыри наиболее хорошо воспринимаются пациентами и дают эффективный уровень тестостерона в сыворотке крови. Тем не менее существуют некоторые различия между этими двумя разновидностями пластырей относительно их аллергогенного потенциала: при применении накожных пластырей отмечается гораздо большая частота возникновения аллергических реакций и раздражения кожи, чем при применении мошоночных пластырей.
Гель тестостерона обладает всеми преимуществами пластырей и не вызывает развития кожных реакций. Единственный его недостаток заключается в наличии возможности контакта геля с партнершей и недостаточном количестве долговременных исследований по его применению.
Трансдермальный путь введения тестостерона позволяет избежать его первичного метаболизма в печени и инактивации, как это происходит при применении пероральных андрогенных препаратов, а также позволяет имитировать циркадные ритмы высвобождения физиологического немодифицированного тестостерона и его естественных метаболитов, эстрадиола и ДГТ. К тому же терапию с использованием пластырей и геля в случае необходимости можно легко прервать. К положительным моментам этого метода лечения также относится низкий риск возникновения лекарственной зависимости.
Европейский препарат 5-α-дигидротестостерон-гель (ДГТ) хотя и признан эффективным, однако неизвестно, оказывает ли изолированное применение неароматизированного андрогена, каким является ДГТ, такое же действие, как тестостерон, в связи с тем, что метаболиты тестостерона включают эстрадиол. По мнению многих авторов, применение препарата не рекомендуется, так как ДГТ вследствие невозможности превращения в эстрадиол не обладает полным спектром терапевтических свойств тестостерона (например, влиянием на костную ткань и сердечно-сосудистую систему).
Некоторые из препаратов заместительной терапии, такие как тестостерона ундеканоат, ДГТ-гель и мошоночные пластыри, вызывают существенное увеличение концентрации ДГТ в сыворотке крови. ДГТ известен как главный андроген простаты, и в связи с этим проводилось много дискуссий по поводу способности его вызывать заболевания предстательной железы. Однако, несмотря на эти предположения, в последнее 10-летие не зафиксировано данных в пользу увеличения частоты возникновения патологии простаты при назначении препаратов ДГТ.
Таким образом, существует множество препаратов заместительной андрогенотерапии, однако все они имеют те или иные побочные эффекты, а также обладают угнетающим действием на сперматогенез. В последнее время появляется все больше работ, демонстрирующих вторичный характер возрастного андрогенного дефицита. Согласно материалам ВОЗ, получены данные о сохранении секретирующей функции клетками Лейдига у пожилых мужчин, что позволило ученым предложить принципиально новый подход в лечении возрастного андрогенного дефицита, основанный на стимуляции синтеза эндогенного тестостерона.
Однако не стоит забывать, что наряду с абсолютными противопоказаниями для заместительной терапии андрогенами (рак грудной и предстательной желез) существуют и дополнительные (доброкачественная гиперплазия предстательной железы с выраженной обструкцией, пролактинома, полицитемия). К относительным противопоказаниям относятся нарушения сна в виде апноэ, обструктивные заболевания легких, интенсивное курение.
К побочным эффектам андрогенов относятся усиление ночного апноэ, полицитемия, гинекомастия, приапизм, задержка жидкости, повышение АД, отеки, увеличение размеров простаты, торможение сперматогенеза.
То есть сегодня существуют методы лечения возрастного андрогенного дефицита, которые можно разделить на две группы, принципиально различающиеся по механизму действия:
заместительная терапия экзогенными андрогенными препаратами; терапия, стимулирующая синтез эндогенного тестостерона.
Таким образом, можно сказать, что оптимального для всех средства для лечения возрастного андрогенного дефицита у мужчин не существует. И к выбору препарата следует подходить строго индивидуально, учитывая возраст пациента, индекс массы тела, необходимость сохранения сперматогенеза, показатели гематокрита и сопутствующие заболевания.
Тестостерона пропионат : инструкция по применению
Состав
Действующее вещество: testostеrone propionate;
1 мл тестостерона пропионата в пересчете на 100% вещество 10 мг или 50 мг
Вспомогательные вещества: этилолеат.
Лекарственная форма
Раствор для инъекций.
Фармакологическая группа
Показания
Заместительная терапия при первичном и вторичном гипогонадизме, евнухоидизме; импотенция эндокринного генеза, посткастрационный синдром, мужской климакс; бесплодие вследствие нарушения сперматогенеза, олигоспермия; остеопороз, вызванный недостаточностью андрогенов; рак молочной железы; климактерические расстройства у женщин (в сочетании с эстрогенами); дисфункциональные маточные кровотечения при гиперэстрогенизме; мастопатии, сопровождающиеся предменструальным мучительным напряжением молочных желез; эндометриоз, миомы матки.
Противопоказания
Индивидуальная непереносимость препарата, рак предстательной железы или рак молочной железы у мужчин, гиперплазия предстательной железы, нарушения мочеиспускания, гинекомастия, нарушение функции печени и почек, гиперкальциемия, сердечная недостаточность, инфаркт миокарда, отеки, сахарный диабет, выраженная астенизация больных, пожилой возраст мужчин, период беременности и кормления грудью.
Способ применения и дозы
Мужчинам при евнухоидизме, врожденном недоразвитии половых желез, удалении их хирургическим путем или в результате травмы назначают внутримышечно ¢ внутримышечно или подкожно по 25-50 мг через день или через 2 дня. Продолжительность курса лечения зависит от эффективности терапии и характера заболевания. После улучшения клинической картины Тестостерона пропионат вводят в поддерживающих дозах по 5-10 мг ежедневно или через день. При импотенции эндокринного генеза, а также при мужском климаксе, сопровождающемся сосудистыми и нервными расстройствами, Тестотерона пропионат назначают по 10 мг ежедневно или по 25 мг 2-3 раза в неделю в течение 1-2 месяцев. Для лечения мужского бесплодия препарат применяют в дозе 10 мг 2 раза в неделю в течение 4-6 месяцев или по 50 мг через день в течение 10 дней. При патологическом мужском климаксе назначают по 25 мг 2 раза в неделю в течение 2 месяцев с месячным перерывом. На начальных стадиях гипертрофии предстательной железы вводят по 10 мг один раз в 2 дня в течение 1-2 месяцев.
Женщинам старше 45 лет при дисфункциональных маточных кровотечениях назначают по 10-25 мг через день в течение 20-30 дней до прекращения кровотечения и появления атрофических клеток в влагалищных мазках.
Побочные реакции
со стороны дыхательной системы: респираторные нарушения, апноэ во сне;
со стороны костно-мышечной системы: боль в ногах, артралгия, судороги мышц;
желудочно-кишечные и гепатобилиарной системы: диарея, тошнота, холестатическая желтуха, повышение уровня аминотрансфераз;
Со стороны системы крови и лимфатической системы: единичные случаи полицитемии, склонность к тромбозам;
со стороны кожи и ее производных : различные кожные реакции, включая акне, себорею, облысение, зуд
метаболические и алиментарные нарушения: увеличение массы тела
неврологические нарушения: головокружение, повышенное потоотделение, головная боль, нервозность, депрессия
общие нарушения и состояние места инъекции боль в месте инъекции, подкожная гематома в месте инъекции; длительное лечение тестостероном или его применение в высоких дозах иногда может приводить к повышению частоты случаев задержки жидкости и отеков; реакции гиперчувствительности.
Передозировка
При применении препарата в повышенных дозах или в течение длительного времени могут развиваться побочные эффекты, описанные в соответствующем разделе. В этом случае препарат отменяют, а после исчезновения андроген побочных эффектов продолжают в уменьшенных дозах. В случае необходимости проводят симптоматическое лечение.
Передозировка препарата может привести к прекращению менструации.
Применение в период беременности или кормления грудью
В связи с возможным тератогенным эффектом андрогенов назначать в период беременности (особенно в I триместре) и кормления грудью противопоказано.
Безопасность и эффективность применения у детей не изучались, поэтому не рекомендуется применять в педиатрической практике.
Особенности применения
Как и все масляные растворы, Тестостерона пропионат вводится внутримышечно. Необходимо тщательно следить за тем, чтобы вещество, которое вводится, не попала в сосуд. При очень медленном введении раствора можно избежать появления кратковременных реакций, иногда наблюдаются во время или сразу после инъекции масляного раствора (позывы к кашлю, приступы кашля, угнетение дыхания).
В процессе лечения необходимо контролировать состояние больных с сердечной недостаточностью, артериальной гипертензией, эпилепсией, мигренью, нарушением функции почек.
Перед началом лечения у мужчин необходимо исключить диагноз рака предстательной железы, поскольку при применении препарата андрогены повышают риск развития гиперплазии предстательной железы.
С профилактической целью рекомендуется проводить регулярные обследования простаты.
Применение Тестостерона детям вместе с маскулинизацией может стать причиной ускоренного роста и созревания костной ткани, а также преждевременного закрытия зоны роста эпифиза, вследствие чего приведет к снижению окончательного роста. Возможно появление обычных угрей.
В связи с возможной склонностью к тромбообразованию с осторожностью следует назначать мужчинам после недавно перенесенной операции или травмы.
Злоупотребление препаратом или привыкания. Андрогены нельзя применять для усиления развития мышц у здоровых людей и для повышения физических способностей.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами
Во время приема препарата следует воздержаться от управления автотранспортом и работы с механизмами.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий
При комбинированном применении с веществами, являющимися индукторами микросомальных ферментов печени (барбитуратами, рифампицином, карбамазепином, фенилбутазоном, фенитоином), эффект Тестостерона может ослабляться. При резко выраженном гипогонадизме Тестостерона пропионат можно комбинировать с препаратами, стимулирующими функцию щитовидной железы, эстрогенами. Усиливает действие анаболических средств, витаминов, препаратов, содержащих кальций, фосфор, замедляет элиминацию циклоспорина.
Андрогены могут усилить гипогликемизирующий эффект инсулина, поэтому может возникнуть необходимость в снижении дозы гипогликемизирующего препарата.
Андрогены могут влиять на метаболизм других лекарственных средств (наблюдается рост сывороточных концентраций оксифенбутазона). Кроме того, сообщалось, что Тестостерон и его производные повышают активность пероральных антикоагулянтов, что может потребовать корректировки дозы. Независимо от того факта, следует всегда соблюдать ограничения, касающиеся инъекций, пациентам с приобретенными или наследственными нарушениями свертываемости крови.
Одновременное применение Тестостерона и адренокортикотропного гормона или кортикостероидов может увеличить риск появления отеков.
Барбитураты и алкоголь снижают активность тестостерона.
Фармакологические свойства
Фармакокинетика. После внутримышечного или подкожного введения медленно абсорбируется из места инъекции. Тестостерон, циркулирующий в крови, попадает в органы-мишени, где восстанавливается до 5-a-дигидротестостерона, который взаимодействует с рецепторами клеточной мембраны и проникает в ядро клетки. До 98% препарата в плазме крови связывается с белками, в основном с глобулинами. Метаболизируется в печени до малоактивных и неактивных метаболитов, которые выводятся из организма с мочой. Примерно 6% выводится кишечником в неизмененном виде.
Основные физико-химические свойства
Маслянистая жидкость светло-зеленого или светло-желтого цвета, со специфическим запахом.
Пролонгированные формы тестостерона в лечении гипогонадизма
Определение и классификация Гипогонадизм — клинический синдром, обусловленный невозможностью обеспечить физиологический уровень тестостерона, связанный с нарушением функции одного из звеньев гипоталамо-гипофизарно-гонадной (ГТГ) системы при нормальном к
Определение и классификация
Гипогонадизм — клинический синдром, обусловленный невозможностью обеспечить физиологический уровень тестостерона, связанный с нарушением функции одного из звеньев гипоталамо-гипофизарно-гонадной (ГТГ) системы при нормальном количестве сперматозоидов.
Различают первичную и вторичную тестикулярную недостаточность.
Первичная тестикулярная недостаточность — заболевание яичек, проявляющееся низким уровнем тестостерона, нарушением сперматогенеза и повышением уровня гонадотропных гормонов.
Вторичная тестикулярная недостаточность — нарушение на центральном уровне в гипоталамусе и гипофизе, характеризуется низким или нормальным уровнем гонадотропных гормонов и низким уровнем тестостерона.
Данная классификация имеет значение для выбора тактики лечения, так как при вторичном гипогонадизме, в отличие от первичного, фертильность можно восстановить при проведении соответствующей гормональной стимуляции. У мужчин с первичной тестикулярной недостаточностью деторождение чаще всего невозможно. При дальнейшем обследовании пациентов со вторичным гипогонадизмом выявляются опухоли гипофиза или системные заболевания.
Поздний гипогонадизм — это связанный с возрастом синдром, характеризующийся типичными клиническими симптомами, обусловленными низким уровнем тестостерона в крови. Наличие позднего гипогонадизма ухудшает качество жизни больного и приводит к нарушению функции многих органов и систем. Данный термин включает такие понятия, как андропауза, андрогенная недостаточность в пожилом возрасте, частичный андрогенный дефицит стареющих мужчин. Возрастное снижение уровня тестостерона связано с нарушением функции как яичек, так и гипоталамо-гипофизарной системы. При этом уровень тестостерона с возрастом уменьшается у мужчин в среднем на 1—2 в год, хотя меньшая концентрация тестостерона по сравнению с нижней границей нормы для здорового молодого мужчины наблюдается лишь у части пациентов пожилого возраста.
Реже гипогонадизм может служить одним из проявлений патологии ГГГ-системы у мужчин с мутацией гена DAX-1, гемохроматозом, серповидно-клеточной анемией, талассемией, при лечении глюкокортикостероидами, алкоголизме.
Клиническая картина гипогонадизма
Диагностика дефицита андрогенов у мужчин представляет определенные трудности. Клинические симптомы гипогонадизма неспецифичны и зависят от возраста, сопутствующих заболеваний, тяжести и длительности нарушения, различной чувствительности к андрогенам и предшествующей терапии тестостероном.
Перечислим симптомы и признаки, указывающие на наличие дефицита андрогенов у мужчин.
Вышеперечисленные клинические симптомы и признаки установлены на основании изучения врачами популяции пациентов, находящихся на лечении в клинике, имеющих, вероятно, более выраженный дефицит андрогенов; наблюдения за мужчинами с классическим дефицитом андрогенов в общей популяции не проводились.
Пороговое значение концентрации тестостерона, ниже которой проявляются симптомы дефицита андрогенов и развиваются неблагоприятные последствия для здоровья, остается неизвестным и, возможно, зависит от возраста. Более того, концентрация тестостерона, при которой назначение препарата является эффективным, остается неизвестной и может различаться в зависимости от индивидуальных особенностей пациента и органа-мишени.
К менее специфичным симптомам и признакам, встречающимся при дефиците андрогенов, относятся следующие.
Таким образом, имеющиеся на сегодня данные свидетельствуют об отсутствии четкого порогового уровня тестостерона, при котором более низкие показатели говорили бы о клинических симптомах дефицита андрогенов и который являлся бы критерием диагностики гипогонадизма у всех пациентов.
Лабораторная диагностика
Определение уровня тестостерона. Необходимо отметить, что определение уровня тестостерона показано только пациентам с клиническими признаками дефицита андрогенов. Наиболее важными параметрами в выявлении гипогонадизма являются общий и расчетный свободный тестостерон, который определяется путем вычислений уровня общего тестостерона и глобулина, связывающего половой гормон (ГСПГ). Важным является определение тестостерона в период с 7 до 11 ч утра, когда его уровень наиболее высок.
Считается, что минимальный пороговый уровень тестостерона не является постоянным и зависит от географических и этнических факторов. Однако в настоящее время официально определено минимальное значение тестостерона, при котором не требуется гормонозаместительная терапия. Так, нижней границей нормы является уровень общего тестостерона 12 нмоль/л (346 нг/дл) и свободного тестостерона 250 пмоль/л (72 пг/мл). Также определено, что при уровне общего тестостерона 8 нмоль/л (231 пг/мл) и свободного тестостерона 180 пмоль/л (52 пг/мл) показана гормонозаместительная терапия. При промежуточных значениях тестостерона и наличии симптомов гипогонадизма показанием к проведению гормональной терапии является исключение других причин заболевания.
Необходимо помнить, что в 30% случаев при повторном анализе выявляется нормальный уровень тестостерона. Кроме того, у 15% здоровых молодых мужчин в течение 24 ч возможно снижение уровня тестостерона по сравнению с нормальными значениями. Поэтому в случае выявления несоответствия клинической картины данным лабораторной диагностики анализы лучше повторить.
Обследование пациента с дефицитом андрогенов должно включать общую оценку состояния здоровья для исключения системных заболеваний, выяснение данных о применении некоторых медикаментов (например, опиатов или высоких доз глюкокортикоидов) и рекреационных препаратов, влияющих на продукцию и метаболизм тестостерона, нарушениях питания и избыточных физических нагрузках, так как при этих состояниях может наблюдаться транзиторное снижение уровня тестостерона. Диагноз дефицита андрогенов не должен выставляться во время острого периода вирусного респираторного заболевания.
Ниже перечислены группы пациентов, у которых часто выявляется низкий уровень тестостерона. Всем им показано определение уровня андрогенов.
Состояния, при которых рекомендуется определение содержания тестостерона в крови:
Таким образом, диагностика дефицита андрогенов у определенных групп больных позволяет выявить пациентов с заболеваниями, казалось бы не связанными с дефицитом андрогенов. Для них терапия тестостероном также показана и может оказаться полезной для лечения основного заболевания.
Определение ФСГ, ЛГ и дополнительные обследования. После выявления андрогендефицита для дифференциальной диагностики первичного (тестикулярного) и вторичного (гипоталамо-гипофизарного) гипрогонадизма показано определение уровня лютеинизирующего гормона (ЛГ) и фолликулстимулирующего гормона (ФСГ) в плазме крови. У мужчин с первичной тестикулярной недостаточностью неизвестной этиологии мы советуем провести исследование кариотипа для исключения синдрома Клайнфельтера. У пациентов с подозрением на вторичный гипогонадизм необходимо проведение дополнительных обследований для исключения опухоли гипофиза, гиперпролактинемии, гемохроматоза и других инфильтративных процессов, синдрома обструктивного ночного апноэ и генетических нарушений, связанных с дефицитом гонадотропинов.
Терапия тестостероном может быть связана с повышением риска возникновения серьезных нежелательных эффектов у мужчин при ряде состояний. Метастазирующий рак предстательной железы и рак молочной железы являются гормонально зависимыми опухолями, рост которых может стимулироваться под влиянием терапии тестостероном; тестостерон не должен назначаться мужчинам с данными видами опухолей. Существует мнение о возможности назначения заместительной терапии тестостероном на основе индивидуального подхода к пациентам с низким уровнем тестостерона после радикальной простатэктомии при отсутствии признаков заболевания в течение двух и более лет и при невозможности выявить PSA в крови, однако в связи с отсутствием рандомизированных исследований такой подход не должен рассматриваться в качестве рекомендации для всех пациентов.
Наличие узлового образования или индуративного процесса в предстательной железе, а также повышение уровня PSA иногда свидетельствуют о невыявленном раке предстательной железы. Кроме того, терапия тестостероном может способствовать ухудшению состояния у мужчин с эритроцитозом, синдромом обструктивного ночного апноэ при отсутствии лечения, при выраженных симптомах обструкции нижних мочевыводящих путей, при тяжелой сердечной недостаточности.
В открытых исследованиях у молодых мужчин с гипогонадизмом была показана низкая частота развития побочных эффектов при заместительной терапии тестостероном. Частыми специфическими побочными эффектами тестостерона являются повышение уровня гематокрита, возникновение акне, увеличение жирности кожи, чувство напряжения в молочных железах.
Литература
И. А. Данилов, кандидат медицинских наук
П. А. Щеплев, доктор медицинских наук, профессор
КБ Управления делами Президента РФ, Москва/p>




