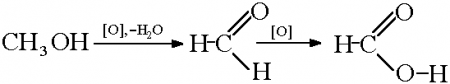
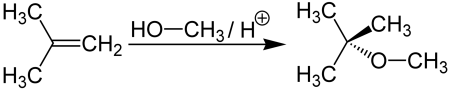
Пить нельзя – нюхать можно: о безопасности метаноловой «омывайки»
Скоро 15 лет, как незамерзающая жидкость на основе метанола находится вне закона, и мы вынуждены пользоваться дорогим и пахучим изопропилом. Разбираемся, в чем причина запрета и какую жидкость лучше выбрать.
Для начала вспомним про основные компоненты незамерзающих жидкостей для омывателя. Это вода, поверхностно-активные вещества (ПАВ), которые отвечают за очистку стекла, красители, «отдушки»-ароматизаторы и температурные модификаторы — этиловый, метиловый или изопропиловый спирты, а также моноэтиленгликоль, не дающие жидкости замерзнуть и отвердеть.
Наилучший термомодификатор — этиловый спирт, он же этанол, он же «пищевой» или «водочный» спирт. По всем показателям (безопасность, себестоимость, температура замерзания) он превосходит метиловый и изопропиловый, но в России акцизный сбор на его использование столь велик, что отечественные производители «незамерзаек» от него отказались. Как исключение иногда в продаже встречаются «премиальные» этаноловые «незамерзайки» по цене порядка 1 500 рублей за 5-литровую канистру.
Опасный метанол?
Немногим уступает этанолу по техническим критериям метиловый спирт, он же метанол, он же древесный спирт. Метанол в РФ не облагается акцизами и по оптовой стоимости относительно дешев (от 12 до 17 тысяч рублей за тонну, в зависимости от производителя и условий поставок), имеет низкую температуру замерзания (— 97,8°С) и, в отличие от изопропилового спирта, не имеет ярко выраженного запаха.
Однако в России с 2007 года метанол для использования в качестве компонента автомобильных жидкостей запрещен — такие составы нельзя ни производить, ни импортировать в РФ. Между тем в странах ЕС, в частности, близких нам Финляндии и Эстонии, метаноловые «незамерзайки» производятся и продаются без ограничений.
Правда, в оправдание запрета у нас ссылаются не на европейский опыт, а на некие «отечественные реалии» и «определенные слои общества», употребляющие суррогаты алкоголя и способные по неведению и привычке из 90-х выпить стеклоочиститель, не зная, что в них метанол.
Однако токсичность паров у метанола одинакова с легальным изопропиловым спиртом. Предельно допустимая концентрация метанола в воздухе рабочей зоны равна 5 мг/куб.м, у изопропилового спирта 10 мг/куб.м, а у этилового спирта, для сравнения, этот показатель равен 1000 мг/куб.м. По классификации, и изопропиловый спирт, и метанол относятся к третьему классу опасности (самый опасный — первый, наименее опасный — четвертый).
Если у вас остались сомнения, предлагаем вашему вниманию цитату из официального постановления Минздрава 14-летней давности:
. Использование стеклоомывающих жидкостей по назначению не оказывает вредного воздействия на здоровье человека, что подтверждается многолетней практикой применения их за рубежом и отсутствием отравлений в нашей стране.
Вместе с тем, учитывая низкий уровень культуры и гигиенического образования части населения, пренебрежение к факторам, наносящим вред здоровью, и соблюдению санитарных требований в области гигиены труда, увеличение в последнее время «социально сниженных лиц» без определенного места жительства и руководствуясь статьей 51 Федерального закона «О санитарно-эпидемиологическом благополучии населения», постановляю:
1. Организациям и предприятиям запретить с 01.07.2000 производство и реализацию стеклоомывающих жидкостей, содержащих метанол.
Главный санитарный врач РФ Г. Г. Онищенко
Постановление Минздрава РФ от 23.05.2000 N 4
Тем не менее во многих публикациях в Сети нагнетаются страх и истерия по поводу содержащих метанол «незамерзаек», говорится о «крайней опасности вдыхания непахнущих ядовитых паров» и предлагается выбирать «незамерзайку» по запаху — чем он сильнее, тем метанола меньше. Оставим эти советы на совести авторов, а читателям со всей авторитетностью заявляем, что если метаноловую жидкость использовать по ее прямому назначению, никакого вреда она не нанесет.
Впрочем, советовать покупать контрафакт на улицах и подпольно ввозить его через границу из Финляндии не будем. Чисто теоретически, если у вас в багажнике найдут канистру с метаноловой «незамерзайкой», вас могут осудить по статье 238 УК РФ «Производство, хранение, перевозка либо сбыт товаров и продукции, не отвечающих требованиям безопасности». Товар есть? Есть. Перевозка осуществляется? Да. Тем не менее на практике автомобилистов, предпочитающих не ограничивать себя из-за алкогольных пристрастий маргиналов, полиция не трогает. А уж какие у них взаимоотношения с продавцами метанола, остается только догадываться.
Немного конспирологии
Есть мнение, что запрет на производство метилового спирта в России — это результат работы нефтяного лобби. Сторонники данной теории говорят, что изопропиловый спирт в промышленной химии получают методом сернокислотной гидратации пропилена. А вот пропилен, в свою очередь, является побочным продуктом нефтепереработки.
И теория выглядела бы стройно, если бы не любопытный факт: основным сырьем для производства метанола является синтез-газ, который добывают путем пиролиза природного газа. Конечно, от экспорта нефти российский бюджет получил в прошлом году 191 млрд долларов, а от газа — лишь 28 млрд… Но всё равно запрет метаноловой «незамерзайки» как результат победы «Роснефти» над «Газпромом» выглядит как-то странно. Пожалуй, что дело всё-таки в привычках люмпенов, массовый падеж которых государству не нужен.
Легальная вонючка
Сейчас в РФ можно законно производить и импортировать в страну только «незамерзайки» на основе изопропилового спирта. С технической, экономической и потребительской точек зрения он наихудший из всех спиртов, используемых для «незамерзаек». Изопропил имеет самую высокую температуру замерзания (— 89° С) и для получения жидкости с порогом в — 30° С его доля должна быть 50%, то есть половина от объема канистры.
При этом изопропил имеет достаточно высокую оптовую стоимость — примерно в пять раз дороже метилового. Себестоимость «честной» изопропиловой «незамерзайки», таким образом, оказывается достаточно высока, при том что кроме спирта тут к стоимости добавляются различные присадки-ароматизаторы, призванные перебить присущий изопропилу резкий запах. Кстати, безопасность для здоровья этих «отдушек» — тоже под большим вопросом.
По магазинам
Благодаря нашему законодательству, на российском рынке «незамерзаек» образовалось как бы два полюса. На одном — дорогие изопропиловые жидкости стоимостью 400-600 рублей, реализуемые на АЗС, в престижных супермаркетах, дилерских автосервисах и т. п. На другом — продаваемые на рынках, трассах или через Интернет дешевые «незамерзайки» на метаноле ценой 100-200 рублей, производимые фактически подпольно.
Таким образом, выложив 500 рублей за 5-литровую канистру — 30° С потребитель получает полностью легальный продукт, где относительно гарантируется соблюдение порога застывания жидкости и применение в ней качественных ПАВ и красителей, которые не будут разъедать пластики и резину в магистралях стеклоомывателя. Но всё равно дышать придется пахучим изопропиловым «лимоном» или «сосной».
С другой стороны, у содержимого подпольно сделанной метаноловой баклажки за 150 рублей никакого едкого запаха не будет. Но какие ядреные ПАВ намешали туда и водой из какой канавы разбавляли — этого не знает никто. Не гарантируется и соблюдение порога замерзания.
Кстати заметим, что замерзание жидкости раньше заявленной температуры — это одна из самых неприятных «засад». Зимние «омывайки» достаточно редко замерзают в лед и рвут магистрали (если только совсем «паленка»), однако получившаяся снегообразная масса хоть и не выведет систему из строя, но и пользоваться омывателем тоже не даст. Особенно долго растворяется такой «снег» в длинных магистралях омывателей фар и стекла задней двери.
Метанол (метиловый спирт). Справка
Группа российских туристов отравилась, предположительно, некачественным алкоголем на популярном турецком курорте Бодрум во время яхт-тура в ночь на 27 мая. Трое россиянок скончались после госпитализации с отравлением метиловым спиртом.
Девушка, отравившаяся вместе с группой российских туристов некачественным алкоголем в Турции, скончалась в московской больнице.
Метиловый спирт (метанол, карбинол, древесный спирт) СН3ОН – бесцветная, легкоподвижная жидкость с запахом, аналогичным запаху этилового спирта. Сырьем для производства метилового спирта служат главным образом природный газ и отходы нефтепереработки, а также коксующийся уголь, газы производства ацетилена пиролизом природного газа и др.
Метанол получают в промышленности восстановлением монооксида углерода при 400° С под давлением 20-30 МПа (мегапаскаль) в присутствии катализатора, состоящего из оксидов меди, хрома, и алюминия.
Метиловый спирт смешивается во всех соотношениях с водой, спиртами, ацетоном, бензолом; образует азеотропные смеси (смеси жидкостей, которые кипят при постоянной температуре и перегоняются без изменения состава) с ацетоном, бензолом, сероуглеродом, тетрахлорид углеродом и мн. др. соединениями.
До 1960-х гг. метиловый спирт синтезировали только на цинкхромовом катализаторе при 300-400°С и давлении 25-40 МПа. Впоследствии распространение получил синтез метилового спирта на медьсодержащих катализаторах (медьцинкалюмохромовом, медь‑цинкалюминиевом или др.) при 200-300°С и давлении 4-15 МПа.
Впервые метиловый спирт был выделен из продуктов сухой перегонки древесины Жаном Батистом Дюма и Эженом Пелиго, которые, сопоставив его свойства со свойствами винного спирта, дали первые представления о классе спиртов (1835). В 1857 г. французский химик Марселен Бертло синтезировал метиловый спирт омылением метилхлорида. Синтетический метиловый спирт начали получать с 1923 г.
Метанол используют как растворитель, а также в производстве формальдегида, применяемого для получения фенолформальдегидных смол. Большие объемы метанола используют при добыче и транспорте природного газа.
Его используют также для получения лекарственных веществ, как добавку к бензину и для получения бензина в целях экономии нефтяного сырья. Разрабатываются процессы получения из метилового спирта уксусного ангидрида, винилацетата, этанола, ацетальдегида, этиленгликоля и др. многотоннажных нефтехимических продуктов.
Метанол – наиболее токсичное соединение среди всех спиртов. Он окисляется в организме человека значительно медленнее, чем этиловый спирт, и в ходе его окисления образуются различные ядовитые вещества.
Метиловый спирт быстро всасывается в желудке и тонком кишечнике. Почти весь метанол (90%) метаболизируется в печени при помощи фермента алкогольдегидрогеназы, в результате чего образуются формальдегид и муравьиная кислота, обладающие высокой токсичностью. Метаболиты метанола удаляются почками, а меньшая часть (15%) в неизменном виде выделяется через легкие.
Метанол является сильным ядом преимущественно нервного и сердечно-сосудистого действия с выраженными кумулятивными свойствами. Токсическое действие метанола связано с угнетением центральной нервной системы, развитием тяжелого метаболического ацидоза (изменение кислотно-щелочного баланса организма), поражением сетчатки глаза и дистрофией зрительного нерва.
Диагноз подтверждается обнаружением в моче муравьиной кислоты.
Хронические отравления характеризуются головокружением, головной болью, бессонницей, повышенной утомляемостью, желудочно-кишечными расстройствами, болями в области сердца и печени, нарушением функции зрения, прежде всего цветного.
Материал подготовлен на основе информации открытых источников
Метанол ГОСТ 2222-95
| Метанол | |
|---|---|
 | |
 | |
 | |
| Систематическое наименование | Метанол |
| Традиционные названия | Метиловый спирт, древесный спирт, карбинол, метилгидрат, гидроксид метила |
| Хим. формула | СН3OH |
| Состояние | жидкость |
| Молярная масса | 32,04 г/моль |
| Плотность | 0,7918 г/см³ |
| Динамическая вязкость | 5.9×10 −4 Па·с |
| Энергия ионизации | 10,84 ± 0,01 эВ |
| Т. плав. | -97 °C |
| Т. кип. | 64,7 °C |
| Т. разл. | 320-380 °C |
| Т. всп. | 6 °C |
| Т. воспл. | 13 °C |
| Т. свспл. | 440 °C |
| Пр. взрв. | 6,98-35,5 % |
| Тройная точка | 175,45 K (−97,7°C) |
| Кр. точка | 513,15 K (240 °C), 7,85 МПа |
| Энтальпия образования | -238 кДж/моль |
| Энтальпия сгорания | 726 000 Дж/моль |
| Энтальпия плавления | 3167,29 ± 0,01 Дж/моль |
| Энтальпия кипения | 37 400 Дж/моль |
| Удельная теплота испарения | 37,4 кДж/моль |
| Давление пара | 11,8 кПа (при 20 °С) |
| pKa | 15,5 |
| Дипольный момент | 1,65 Д |
| ГОСТ | ГОСТ 2222-95 ГОСТ 6995-77 |
| Рег. номер CAS | 67-56-1 |
| PubChem | 887 |
| Рег. номер EINECS | 200-659-6 |
| SMILES | |
| RTECS | PC1400000 |
| ChEBI | 17790 |
| Номер ООН | 1230 |
| ChemSpider | 864 |
| Токсичность | умеренно-токсичен для мелких животных, высокотоксичен для крупных животных и человека, поражает зрительный нерв   |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
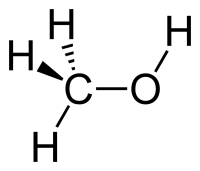
Метанол (метиловый спирт, древесный спирт, карбинол, метилгидрат, гидроксид метила) — CH3OH, простейший одноатомный спирт, бесцветная ядовитая жидкость, контаминант. Метанол — это первый представитель гомологического ряда одноатомных спиртов.
С воздухом в объёмных концентрациях 6,98—35,5 % образует взрывоопасные смеси (температура вспышки 8 °C). Метанол смешивается в любых соотношениях с водой и большинством органических растворителей.
Содержание
История
Метанол был впервые обнаружен Бойлем в 1661 году в продуктах сухой перегонки древесины. Через два столетия, в 1834 году, его выделили в чистом виде Ж. Б. Дюма и Э. М. Пелиго. Тогда же была установлена химическая формула метанола. В 1857 году Бертло получил метанол омылением метилхлорида.
Получение
Известно несколько способов получения метанола: сухая перегонка древесины и лигнина, термическое разложение солей муравьиной кислоты, синтез из метана через метилхлорид с последующим омылением, неполное окисление метана и получение из синтез-газа. Первоначально в промышленности был освоен метод получения метанола сухой перегонкой древесины, но впоследствии он потерял своё промышленное значение. Современное производство метанола из монооксида углерода и водорода впервые было осуществлено в Германии компанией BASF в 1923 году. Процесс проводился под давлением 10—35 МПа на цинк-хромовом катализаторе (ZnO/Cr2O3) при температуре 320—450 °C. Впоследствии распространение получил синтез метанола на медьсодержащих катализаторах, промотированных цинком, хромом и др., при 200—300 °C и давлении 5-10 МПа, разработанный в Англии.
Современный промышленный метод получения — синтез из оксида углерода(II) и водорода на медь-цинковом оксидном катализаторе при следующих условиях:
Схема механизма каталитического получения метанола сложна и суммарно может быть представлена в виде реакции:
До промышленного освоения каталитического способа получения метанол получали при сухой перегонке дерева (отсюда его название «древесный спирт»). В настоящее время этот способ неактуален.
Молекулярная формула — CH4O или CH3—OH
Производство метанола (в тыс. тонн):
| год | США | Германия | Мир | Цена продажи($/т) |
|---|---|---|---|---|
| 1928 | 24 | 18 | 140 | 84,7 |
| 1936 | 97 | 93 | 305 | 88,9 |
| 1950 | 360 | 120 | 349 | 83,1 |
| 1960 | 892 | 297 | 3930 | 99,7 |
| 1970 | 2238 | нет данных | 5000 | 89,7 |
| 1980 | 3176 | 870 | 15000 | 236,1 |
| 2004 | 3700 | 2000 | 32000 | 270 |
Применение
В органической химии метанол используется в качестве растворителя.
Метанол используется в газовой промышленности для борьбы с образованием гидратов (из-за низкой температуры замерзания и хорошей растворимости). В органическом синтезе метанол применяют для выпуска формальдегида, формалина, уксусной кислоты и ряда эфиров (например, МТБЭ и ДМЭ), изопрена и др.
Наибольшее его количество идёт на производство формальдегида, который используется для производства карбамидоформальдегидных и фенолформальдегидных смол. Значительные количества CH3OH используют в лакокрасочной промышленности для изготовления растворителей при производстве лаков. Кроме того, его применяют (ограниченно из-за гигроскопичности и отслаивания) как добавку к жидкому топливу для двигателей внутреннего сгорания.
Благодаря высокому октановому числу, позволяещему увеличить степень сжатия до 16, увеличивая тем самым удельную мощность двигателя; метанол используется для заправки гоночных мотоциклов и автомобилей. Метанол горит в воздушной среде, и при его окислении образуется двуокись углерода и вода:
Для получения биодизеля растительное масло переэтерифицируется метанолом при температуре 60 °C и нормальном давлении приблизительно так: 1 т масла + 200 кг метанола + гидроксид калия или натрия.
Во многих странах метанол применяется в качестве денатурирующей добавки к этанолу при производстве парфюмерии. В России использование метанола в потребительских товарах запрещено. В России запрещено использование метилового спирта в средствах по уходу за автотранспортом, а также продажа населению указанных средств, содержащих метанол.
Используется в топливных элементах. Работа топливных элементов основана на реакции окисления метанола на катализаторе в диоксид углерода. Вода выделяется на катоде. Протоны (H + ) проходят через протонообменную мембрану к катоду где они реагируют с кислородом и образуют воду. Электроны проходят через внешнюю цепь от анода к катоду снабжая энергией внешнюю нагрузку.
Общая для топливного элемента:
Получение муравьиной кислоты окислением метанола:
Получение диметилового эфира дегидратацией метанола при 300—400 °C и 2-3 МПа в присутствии гетерогенных катализаторов — алюмосиликатов — степень превращения метанола в диметиловый эфир — 60 % или цеолитов — селективность процесса близка к 100 %. Диметиловый эфир (C2H6O) — экологически чистое топливо без содержания серы, содержание оксидов азота в выхлопных газах на 90 % меньше, чем у бензина. Цетановое число диметилового дизеля более 55, при том что у классического нефтяного 38-53.
Метил-трет-бутиловый эфир получается при взаимодействии метанола с изобутиленом в присутствии кислых катализаторов (например, ионообменных смол):
Метил-трет-бутиловый эфир (C5H12O) применяется в качестве добавки к моторным топливам, повышающей октановое число бензинов (антидетонатор). Максимальное законодательное содержание МТБЭ в бензинах Европейского союза — 15 %, в Польше — 5 %. В России в среднем составе бензинов содержание МТБЭ составляет до 12 % для АИ92 и до 15 % для АИ95, АИ98.
Отдельным направлением является использование метанола для переэтерификации жиров в производстве биодизеля.
Гомологизация метанола
Гомологизация, то есть превращение органического соединения в свой гомолог путём внедрения одной или нескольких метиленовых групп, для спиртов была впервые осуществлена в 1940 году — на основе метанола каталитическим путём под воздействием высокого давления был синтезирован этанол:
Реакция гомологизации по своему механизму близка реакции гидроформилирования алкенов и в настоящее время с помощью модифицированных катализаторов кобальта и рутения и добавления йодид-ионов в качестве промоторов удаётся добиться 90 % выхода по этанолу.
Исходный метанол также получают из окиси углерода (катализаторы на основе оксидов меди и цинка, давление 5—10 МПа, температура 250 °C), так что общая схема выглядит следующим образом:
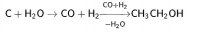
Побочными продуктами реакции в случае синтеза этанола будут ацетальдегид, этилен и диэтиловый эфир.
В 1940 году впервые была осуществлена катализируемая оксидом кобальта при давлении 600 атм реакция метанола с синтез-газом с образованием в качестве основного продукта этанола… Впоследствии эта реакция, названная гомологизацией, вызвала огромный интерес у химиков. Её привлекательность связана с возможностью получения этилена из угольного сырья Применение в качестве катализаторов карбонила кобальта Со2(СО)8 позволило понизить давление до 250 атм, при этом степень превращения метанола составила 70 %, а основной продукт — этанол образовывался с селективностью 40 %. В дальнейшем были предложены более селективные катализаторы на основе соединений кобальта и рутения с добавками фосфиновых лигандов и было установлено, что реакцию можно ускорить с помощью введения промоторов — иодид-ионов. В настоящее время удалось достичь селективности по этанолу 90 %. Хотя механизм гомологизации до конца не установлен, можно считать, что он близок к механизму карбонилирования метанола.
Биометанол
Промышленное культивирование и биотехнологическая конверсия морского фитопланктона рассматривается как одно из наиболее перспективных направлений в области получения биотоплива.
В начале 80-х рядом европейских стран совместно разрабатывался проект, ориентированный на создание промышленных систем с использованием прибрежных пустынных районов. Осуществлению этого проекта помешало общемировое снижение цен на нефть.
Первичное производство биомассы осуществляется путём культивирования фитопланктона в искусственных водоёмах, создаваемых на морском побережье.
Вторичные процессы представляют собой метановое брожение биомассы и последующее гидроксилирование метана с получением метанола.
Основными доводами в пользу использования микроскопических водорослей являются следующие:
С точки зрения получения энергии данная биосистема имеет существенные экономические преимущества по сравнению с другими способами преобразования солнечной энергии.
Метанол в качестве топлива
При применении метанола в качестве топлива следует отметить, что объёмная и массовая энергоёмкость (теплота сгорания) метанола (удельная теплота сгорания = 22,7 МДж/кг) на 40—50 % меньше, чем бензина, однако при этом теплопроизводительность спиртовоздушных и бензиновых топливовоздушных смесей при их сгорании в двигателе различается незначительно по той причине, что высокое значение теплоты испарения метанола способствует улучшению наполнения цилиндров двигателя и снижению его теплонапряженности, что приводит к повышению полноты сгорания спиртовоздушной смеси. В результате этого мощность двигателя повышается на 7—9 %, а крутящий момент на 10—15 %. Двигатели гоночных автомобилей, работающих на метаноле с более высоким октановым числом, чем бензин, имеют степень сжатия, превышающую 15:1, в то время как в обычном ДВС с искровым зажиганием степень сжатия для неэтилированного бензина как правило, не превышает 11,5:1. Метанол может использоваться как в классических двигателях внутреннего сгорания, так и в специальных топливных элементах для получения электричества.
Отдельно следует отметить увеличение индикаторного КПД при работе классического ДВС на метаноле по сравнению с его работой на бензине. Такой прирост вызван снижением тепловых потерь и может достигать единиц процентов.
| Топливо | Плотность энергии | Смесь воздуха с топливом | Удельная энергия смеси воздуха | Удельная теплота испарения | Октановое число (RON) | Октановое число (MON) |
|---|---|---|---|---|---|---|
| Бензин | 32 МДж/л | 14,6 | 2,9 МДж/кг воздух | 0,36 МДж/кг | 91—99 | 81—89 |
| Бутанол-1 | 29,2 МДж/л | 11,1 | 3,2 МДж/кг воздух | 0,43 МДж/кг | 96 | 78 |
| Этанол | 19,6 МДж/л | 9,0 | 3,0 МДж/кг воздух | 0,92 МДж/кг | 132 | 89 |
| Метанол | 16 МДж/л | 6,4 | 3,1 МДж/кг воздух | 1,2 МДж/кг | 156 | 92 |
Низкий уровень примесей метанола может быть использован в топливе существующих транспортных средств с использованием надлежащих ингибиторов коррозии. Т. н. европейская директива качества топлива (European Fuel Quality Directive) позволяет использовать до 3 % метанола с равным количеством присадок в бензине, продаваемом в Европе. Сегодня в Китае используется более 1000 млн галлонов метанола в год в качестве транспортного топлива в смесях низкого уровня, используемых в существующих транспортных средств, а также высокоуровневые смеси в транспортных средствах, предназначенных для использования метанола в качестве топлива.
Помимо применения метанола в качестве альтернативы бензина существует технология применения метанола для создания на его базе угольной суспензии, которая в США имеет коммерческое наименование «метакол» (methacoal). Такое топливо предлагается как альтернатива мазута, широко используемого для отопления зданий (Топочный мазут). Такая суспензия в отличие от водоуглеродного топлива не требует специальных котлов и имеет более высокую энергоемкость. С экологической точки зрения такое топливо имеет меньший «углеродный след», чем традиционные варианты синтетического топлива получаемого из угля с использованием процессов, где часть угля сжигается во время производства жидкого топлива.
Свойства метанола и его реакции
Метанол — бесцветная жидкость с алкогольным запахом (запах этилового спирта). Температура кипения +64,7 °C.
Удельный вес при 0°/0° = 0,8142 (Копп); при 15°/15° = 0,79726; при 25°/25° = 0,78941 (Perkin); при 64,8°/4° = 0,7476 (Шифф); при 0°/4° = 0,81015; при 15,56°/4° = 0,79589 (Dittmar и Fawsitt). Капиллярная постоянная при температуре кипения a ² =5,107 (Шифф); Критическая температура 241,9° (Шмидт). Упругость пара при 15° = 72,4 мм; при 29,3° = 153,4 мм; при 43° = 292,4 мм; при 53° = 470,3 мм; при 65,4° = 756,6 мм (Д. Коновалов). Теплота горения равна 170,6, теплота образования 61,4 (Штоман, Клебер и Лангбейн).
Метанол смешивается во всех отношениях с водой, этиловым спиртом и эфиром; при смешении с водой происходит сжатие и разогревание. Горит синеватым пламенем. Подобно этиловому спирту — сильный растворитель, вследствие чего во многих случаях может заменять этиловый спирт. Безводный метанол, растворяя небольшое количество медного купороса, приобретает голубовато-зеленое окрашивание, поэтому безводным медным купоросом нельзя пользоваться для открытия следов воды в метаноле; но он не растворяет CuSO4∙7H2O (Клепль).
Метанол (в отличие от этанола) с водой не образует азеотропной смеси, в результате чего смеси вода-метанол могут быть разделены ректификационной перегонкой. Температура кипения водных растворов метанола:
| Молярная доля метанола % | Т кип. °C, 760 мм. рт. ст. |
|---|---|
| 0 | 100 |
| 5 | 92,8 |
| 10 | 88,3 |
| 15 | 84,8 |
| 20 | 82 |
| 25 | 80,1 |
| 30 | 78,2 |
| 35 | 76,8 |
| 40 | 75,6 |
| 45 | 74,5 |
| 50 | 73,5 |
| 55 | 72,4 |
| 60 | 71,6 |
| 65 | 70,7 |
| 70 | 69,8 |
| 75 | 68,9 |
| 80 | 68 |
| 85 | 67,1 |
| 90 | 66,3 |
| 95 | 65,4 |
| 100 | 64,6 |
Метанол дает со многими солями соединения, подобные кристаллогидратам (сольваты), например: CuSO4 ∙ 2CH3OH; LiCl ∙ 3CH3OH; MgCl2 ∙ 6CH3OH; CaCl2 ∙ 4CH3OH представляет собой шестисторонние кристаллы, разлагаемые водой, но не разрушаемые нагреванием до 100° (Kane). Соединение BaO ∙ 2CH3OH ∙ 2H2O получается в виде блестящих призм при растворении BaO в водном метаноле и испарении на холоде полученной жидкости при комнатной температуре (Форкранд).
С едкими щелочами метанол образует соединения 5NaOH ∙ 6CH3OH; 3KOH ∙ 5CH3OH (Геттиг). При действии металлических калия и натрия легко даёт алкоголяты, присоединяющие к себе кристаллизационный метанол и иногда воду.
При пропускании паров метанола через докрасна накалённую трубку получается C2H2 и другие продукты (Бертло). При пропускании паров метанола над накалённым цинком получается окись углерода, водород и небольшие количества болотного газа (Jahn). Медленное окисление паров метанола при помощи раскаленной платиновой или медной проволоки представляет лучшее средство для получения больших количеств формальдегида: 2CH3OH+O2=2HCHO+2H2O. При действии хлористого цинка и высокой температуры метанол даёт воду и алканы, а также небольшие количества гексаметилбензола (Лебедь и Грин). Метанол, нагретый с нашатырём в запаянной трубке до 300°, даёт моно-, ди- и триметиламины (Бертло).
При пропускании паров метанола над KOH при высокой температуре выделяется водород и образуются последовательно формиат, ацетат и, наконец, карбонат калия.
Концентрированная серная кислота даёт метилсерную кислоту CH3HSO4, которая при дальнейшем нагревании с метанолом даёт метиловый эфир. При перегонке метанола с избытком серной кислоты в отгон переходит диметилсерная кислота (CH3)2SO4. При действии серного ангидрида SO3 получается CH(OH)(SO3H)2 и CH2(SO3H)2 (см. Метилен).
Метанол при действии соляной кислоты, пятихлористого фосфора и хлористой серы даёт хлористый метил CH3Cl. Действием HBr и H2SO4 получают бромистый метил. Подкисленный 5%-й серной кислотой и подвергнутый электролизу, метанол даёт CO2, СО, муравьинометиловый эфир, метилсерную кислоту и метилаль CH2(OCH3)2 (Ренар). При нагревании метанола с хлористо-водородными солями ароматических оснований (анилином, ксилидином, пиперидином) легко происходит замещение водорода в бензольном ядре метилом (Гофман, Ладенбург); реакция имеет большое техническое значение при приготовлении метилрозанилина и других искусственных пигментов.
Нахождение в природе
В свободном состоянии метиловый спирт встречается в природе лишь изредка и в очень небольших количествах (например в эфирных маслах), но производные его распространены довольно широко. Так, например, многие растительные масла содержат сложные эфиры метилового спирта: масла гаултерии — метиловый эфир салициловой кислоты C6H4(OH)COOCH3, масло жасмина — метиловый эфир антраниловой кислоты C6H4(NH2)COOCH3. Простые эфиры метилового спирта чрезвычайно часто встречаются среди природных веществ, например природных красителей, алкалоидов и т. п.
В промышленности метиловый спирт раньше получали исключительно путём сухой перегонки дерева. В жидких погонах, так называемом «древесном уксусе», наряду с уксусной кислотой (10 %), ацетоном (до 0,5 %), ацетальдегидом, аллиловым спиртом, метилацетатом, аммиаком и аминами содержится также 1,5—3 % метилового спирта. Для отделения уксусной кислоты продукты сухой перегонки пропускают через горячий раствор известкового молока, задерживающий её в виде уксуснокислого кальция. Значительно труднее отделить метиловый спирт от ацетона, так как температуры кипения их очень близки (ацетон, т.кип. 56,5°; метиловый спирт, т.кип. 64,7°). Все же путём тщательной ректификации на соответствующих колоннах в технике удается почти полностью отделить метиловый спирт от сопутствующего ему ацетона. Неочищенный метиловый спирт называется также «древесным спиртом».
Токсичность
В США максимальное допустимое суточное употребление метанола (референтная доза), подразумевая несвязанное с какими-либо эффектами на здоровье, установлено в размере 2 мг на кг веса тела (с 1988 года).
Предельно допустимая концентрация метанола в воздухе рабочей зоны равна 5 мг/м³ (у изопропилового спирта 10 мг/м³, у этанола — 1000 мг/м³), ПДК в воздухе населенных мест равна 1,0 мг/м³ (у изопропилового спирта 0,6 мг/м³, у этанола — 5 мг/м³).
Наиболее легкая форма отравления характеризуется наличием головной боли, общей слабостью, недомоганием, ознобом, тошнотой, рвотой.
Токсичность метанола состоит в том, что при попадании в организм он с течением времени окисляется до ядовитого формальдегида, который вызывает слепоту, вредно влияет на нервную систему, вступает в реакции с белками. Происходит так называемый летальный синтез.
Особая опасность метанола связана с тем, что по запаху и вкусу он неотличим от этилового спирта, из-за чего и происходят случаи его употребления внутрь. Йодоформная реакция: с этиловым спиртом выпадет йодоформ жёлтого цвета, а с метанолом ничего не выпадает (реакция не подходит для определения содержания метанола в растворе этанола).
Как указано в руководстве для врача скорой медицинской помощи, при отравлении метанолом антидотом является этанол, который вводится внутривенно в форме 10 % раствора капельно или 30—40 % раствора перорально из расчёта 1—2 грамма раствора на 1 кг веса в сутки. Полезный эффект в этом случае обеспечивается отвлечением фермента АДГ I на окисление экзогенного этанола.
Следует учесть, что при недостаточно точном диагнозе за отравление метанолом можно принять алкогольную интоксикацию, отравление 1,2-дихлорэтаном или четырёххлористым углеродом — в этом случае введение дополнительного количества этилового спирта опасно.
Отравления метанолом довольно часты. Так, в США в течение 2013 года зафиксировано 1747 случаев.
Массовые отравления метанолом
Известно множество массовых отравлений метанолом. Источником метанола могут быть фальсифицированные незамерзающие жидкости для автомобилей, контрафактный алкоголь, метанол, выдаваемый за этиловый спирт.