ascus цитология что делать
Что такое дисплазия шейки матки? Причины возникновения, диагностику и методы лечения разберем в статье доктора Игнатенко Т. А., гинеколога со стажем в 13 лет.
Определение болезни. Причины заболевания
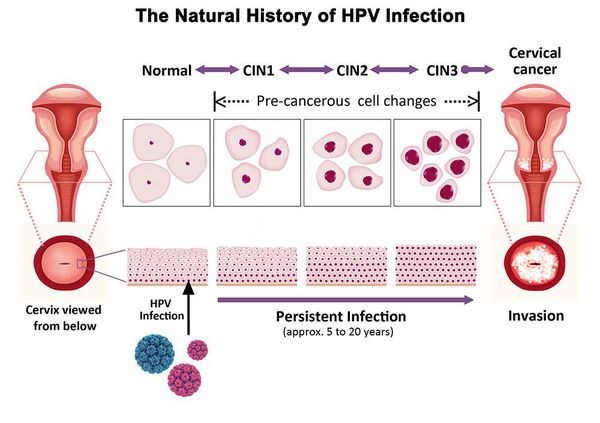
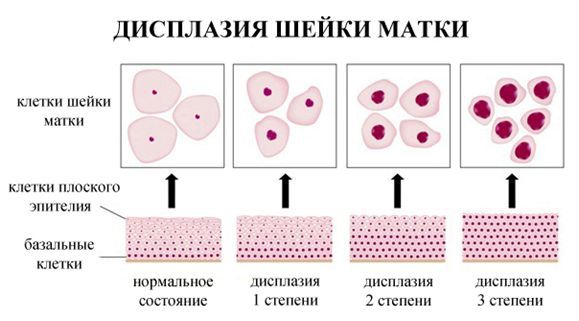
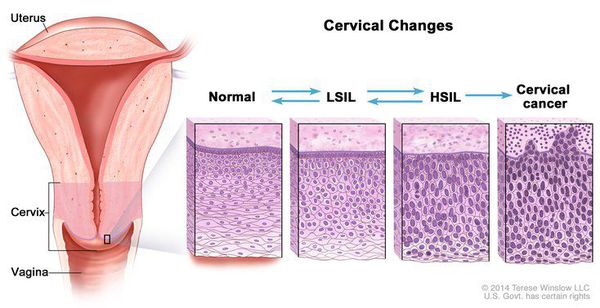
Дисплазия шейки матки, или цервикальная интраэпителиальная неоплазия (ЦИН), или Cervical Intraepithelial neoplasia (CIN) — это патологический процесс, при котором в толще клеток, покрывающих шейку матки, появляются клетки с различной степенью атипии (неправильного строения, размера, формы).
Основной фактор развития дисплазии и рака шейки матки — папилломавирусная инфекция (ПВИ), причем длительное персистирование именно ВПЧ высокого канцерогенного риска. У женщин с риском развития цервикальной неоплазии распространенность онкогенных типов ВПЧ чрезвычайно велика. ВПЧ становится причиной CIN 2-3 и рака шейки матки в 91,8% и 94,5% случаев соответственно. [1]
Риск цервикальной CIN 2 особенно высок у женщин, которые до этого имели опыт пересадки органов, у них выявлена ВИЧ-инфекция или они принимают иммунодепрессанты. [2]
Кроме того, была выявлена связь между пассивным курением среди некурящих и повышенным риском возникновения CIN 1. [3]
Симптомы дисплазии шейки матки
Дисплазия шейки матки, как правило, имеет бессимптомное течение, поэтому пациентки не предъявляют никаких специфических жалоб.
Патогенез дисплазии шейки матки
Критический фактор развития цервикальной интраэпителиальной неоплазии — инфицирование вирусом папилломы человека. Во многих случаях цервикальная интраэпителиальная неоплазия легкой степени отражает временную реакцию организма на папиломавирусную инфекцию и без лечения исчезает в течение полугода-года наблюдения. При цервикальной интраэпителиальной неоплазии умеренной и тяжелой степени высока вероятность встраивания вируса папилломы человека в клеточный геном. Инфицированные клетки начинают продуцировать вирусные белки E6 и Е7, которые продлевают жизнь клетки, сохраняя ее способность к неограниченному делению. Неизбежно формирующиеся на этом фоне мутации клеток ведут к формированию предрака (дисплазии) и рака шейки матки, влагалища и вульвы.
Онкогенные белки ВПЧ (Е6, Е7) взаимодействуют с регуляторными белками клеток шейки матки, приводя к повышению активности онкомаркера p16INK4A, что свидетельствует о неконтролируемом размножении клеток шейки матки. Таким образом, сверхэкспрессия p16INK4A, определяемая в материале шейки матки, который получают при биопсии, является биомаркером интеграции вируса папилломы человека высокого риска в геном и трансформации эпителиальных клеток под действием вируса, что делает эту информацию полезной при оценке прогноза развития предраковых и злокачественных поражений, связанных с инфицированием генитального тракта вирусом папилломы человека. [5]
Классификация и стадии развития дисплазии шейки матки
Для постановки цитологического диагноза (по результатам цитологического исследования соскобов шейки матки и цервикального канала с окрашиванием по Папаниколау (Рар-тест) или жидкостной цитологии) используется классификация Бетесда (The Bethesda System, 2014), основанная на термине SIL (Squamous Intraepithelial Lesion) – плоскоклеточное интраэпителиальное поражение. [10]
Выделяют три вида результатов соскобов с поверхности шейки матки (экзоцервикса):
Классификация Папаниколау
Существуют также гистологические классификации для оценки материала, полученного при биопсии.
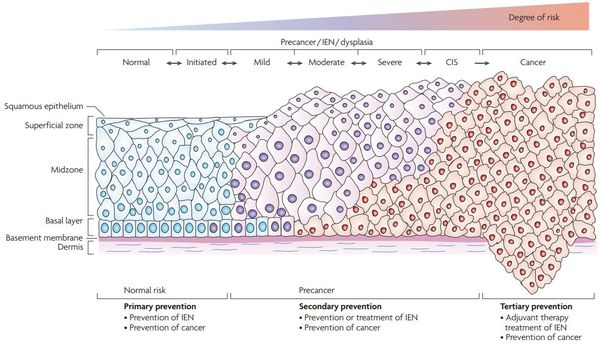
По классификации R. M. Richart (1968) в зависимости от глубины поражения поверхностного клеточного слоя шейки матки выделяют:
В приведенной ниже таблице даны соотношения классификаций предраковых поражений шейки матки. [9]
Осложнения дисплазии шейки матки
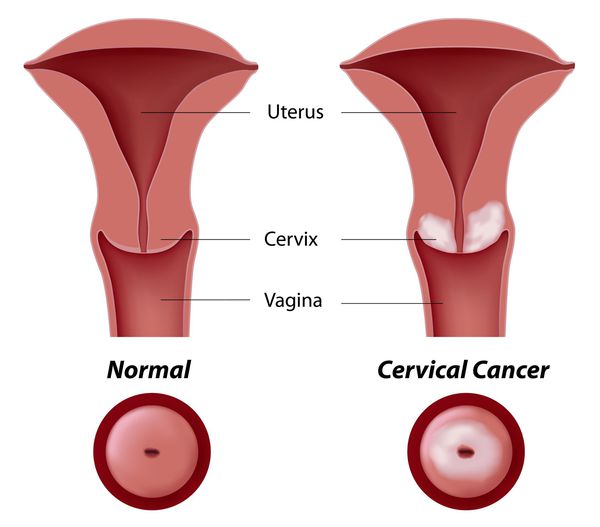
Основное и самое опасное осложнение цервикальной интраэпителиальной неоплазии заключается в развитии рака шейки матки, любой случай развития которого — результат упущенных возможностей диагностики и лечения дисплазии шейки матки. [7]
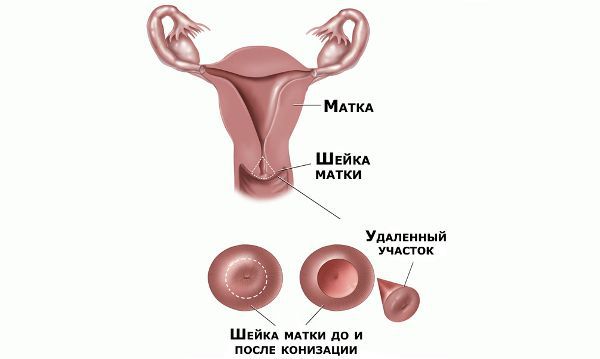
Проводились длительные, систематические исследования риска рака шейки матки у женщин с диагнозом цервикальной интраэпителиальной неоплазии 3 степени (CIN3) по сравнению с женщинами, у которых были нормальные цитологические результаты. Согласно полученным данным, долгосрочный относительный риск развития рака шейки матки зависит от различных гистологических типов CIN3 и выше всего он для аденокарциномы in situ. Даже через 25 и более лет после конизации (хирургического иссечения патологических тканей шейки матки) риск злокачественного перерождения клеток был значительным. [4]
Диагностика дисплазии шейки матки
Для ранней диагностики предраковых поражений шейки матки во многих странах мира существует система цервикального скрининга.
В России данная система включает последовательность действий:
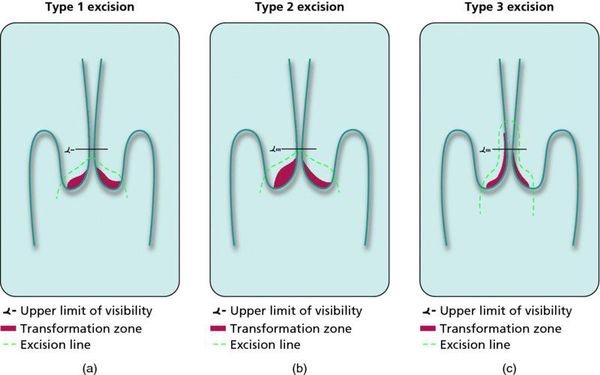
При кольпоскопии должна быть тщательно оценена зона трансформации (переходная зона стыка двух видов покровного эпителия шейки матки).
Влагалищная часть шейки матки (экзоцервикс) покрыта многослойным плоским эпителием. В канале шейки матки (цервикальном канале, эндоцервиксе) — цилиндрический эпителий. Место перехода цилиндрического эпителия цервикального канала в многослойный плоский эпителий поверхности шейки матки носит название зоны трансформации. Эта область имеет большое клиническое значение, поскольку именно в ней возникает более 80% случаев дисплазии и рака шейки матки.
Лечение дисплазии шейки матки
Динамическому наблюдению подлежат молодые пациентки (до 35 лет) с LSIL (ВПЧ, ЦИН 1, ЦИН 2, если при биопсии не обнаружен белок р16, являющийся признаком проникновения ВПЧ высокого риска в геном и трансформации опухолевых клеток под действием вируса). Наблюдать возможно пациенток только с 1 и 2 кольпоскопическим типом зоны трансформации.
Контрольные осмотры, цитологическое и ВПЧ-тестирование показаны через 6 и 12 месяцев после первичного обнаружения патологии. При выявлении HSIL (ЦИН 2 c обнаружением белка р16 при биопсии, ЦИН 3) неизбежно хирургическое лечение в виде абляции («прижигания») или эксцизии (удаления) поврежденной ткани. Для абляции используют электро-/радио-, крио- и лазерные воздействия. Эксцизия возможна электро-/радиоволновая или ножевая.
Немаловажно, что при выявлении по кольпоскопии 3 типа зоны трансформации на фоне положительного РАР-теста гинеколог обязан провести выскабливание слизистой канала шейки матки и/или широкую эксцизионную биопсию (конизацию шейки матки) для исключения опухолевого процесса, потенциально располагающегося вне зоны кольпоскопического обзора. Немаловажно наблюдение после операции через 6 и 12 месяцев с выполнением цитологического соскоба и ВПЧ-теста.
Следует отметить, что процедура хирургического иссечения патологических тканей на шейке матки увеличивает риск преждевременных родов. А сама по себе цервикальная интраэпителиальная неоплазия первой степени на течении беременности и родов никак не отражается и зачастую опасности не представляет. [12]
Средний возраст женщин, когда может потребоваться хирургическая коррекция цервикальной внутриэпителиальной неоплазии — около 30 лет. Хирургическое лечение нередко ассоциировано с неблагоприятным течением последующей беременности. Частота и тяжесть неблагоприятных осложнений возрастают с увеличением глубины иссекаемых тканей. [13]
Прогноз. Профилактика
При своевременном выявлении и лечении дисплазии шейки матки прогноз благоприятный. Основным фактором развития и прогрессирования дисплазии шейки матки является длительное инфицирование канцерогенными типами ВПЧ. Для предупреждения заражения ВПЧ существуют профилактические вакцины «Церварикс» (защита от 16, 18 типов ВПЧ), «Гардасил» (профилактика инфицирования 6, 11, 16, 18 типами вируса), в декабре 2014 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов одобрило использование вакцины «Гардасил9», защищающей от инфицирования 9 типами ВПЧ (6, 11, 16, 18, 31, 33, 45, 52, 58). Однако на российском рынке данный продукт ещё не доступен. «Церварикс» зарегистрирована для вакцинации женщин от 10 до 25 лет; «Гардасил» показана к применению детям и подросткам в возрасте от 9 до 15 лет и женщинам от 16 до 45 лет.
Дополнительными факторами риска прогрессирования ПВИ с формированием предраковой патологии являются:
Устранение и профилактика данных факторов способны снизить вероятность развития предраковой патологии шейки матки.
Рак шейки матки поражает преимущественно женщин репродуктивного возраста. Скрининг является важной стратегией вторичной профилактики. Длительный процесс канцерогенной трансформации от появления в организме вируса папилломы человека (ВПЧ) до инвазивного рака дает широкие возможности для выявления заболевания на стадии, когда лечение высокоэффективно. Подходящими скрининговыми тестами в мире признаны цитологическое исследование, визуальный осмотр после применения уксусной кислоты и тесты на выявление ВПЧ. Всемирная организация здравоохранения рекомендует проводить скрининг женщин по крайней мере один раз в жизни в возрасте от 30 до 49 лет. [14]
Согласно приказу Министерства здравоохранения РФ от 03.02.2015. N36ан «Об утверждении порядка проведения диспансеризации определенных групп взрослого населения», осмотр со взятием мазка (соскоба) с поверхности шейки матки и цервикального канала на цитологическое исследование производится 1 раза в 3 года для женщин в возрасте от 21 года до 69 лет включительно.
Лечение и профилактика прогрессирования заболеваний шейки матки, ассоциированных с вирусом папилломы человека
Приведены основные профилактические мероприятия, направленные на раннее выявление и преодоление прогрессирования ВПЧ-ассоциированной патологии шейки матки. Применение препарата инозин пранобекс повышает эффективность терапии заболеваний шейки матки, ассоц
Main preventive measures directed to early diagnostics and liquidation of development of HPV-associated cervical pathology. Use of inozin pranobex medication increases efficiency of therapy of cervical diseases associated with HPV infection.
Основными проблемами в тактике ведения женщин с заболеваниями шейки матки, ассоциированными с вирусом папилломы человека (ВПЧ), являются несвоевременная и некачественная диагностика, отсутствие четких алгоритмов при принятии решения, а также недостаточная приверженность пациенток к лечению, в основном связанная с полным или частичным невыполнением рекомендаций врача.
По оценкам Центров по контролю заболеваемости (англ. Centers for Disease Control and Prevention, CDC) в США ВПЧ инфицируются до 5,5 млн человек в год [1]. В Европе в год регистрируется 554 000 случаев заболеваний, вызванных этими вирусами, в том числе: цервикальных внутриэпителиальных (интраэпителиалъных) неоплазий (cervical intraepithelial neoplasia — CIN) легкой степени (CIN I), генитальных бородавок, CIN средней и тяжелой степени (CIN II и III), рака шейки матки (РШМ). Несмотря на современные методы диагностики и лечения предраковых заболеваний шейки матки, ежегодно в мире фиксируют 470 тыс. новых случаев РШМ, из которых 233 тыс. заканчиваются смертельным исходом [2]. По данным российских ученых папилломавирусная инфекция (ПВИ) гениталий встречается у 44,3% женщин, обращающихся в гинекологические клиники [3], а заболевания шейки матки, ассоциированные с ВПЧ, встречаются у 50–80% населения и 99,7% случаев подтвержденного РШМ.
Течение ВПЧ-инфекции зависит от состояния иммунной системы и может быть транзиторным, латентным и персистирующим [4–8]. Возможно самоизлечение латентных и начальных субклинических форм ПВИ, для чего важен врожденный компонент иммунной системы. Главное значение имеют клеточные, рецепторные и молекулярные механизмы защиты. Наиболее неблагоприятное течение — персистирующее. При этом ВПЧ «обманывает» иммунную систему макроорганизма, что позволяет ему длительно персистировать ввиду своих эволюционно приобретенных особенностей — репликационный цикл ограничен эпителием, нет виремии и цитолиза, имеется локальная иммуносупрессия за счет вирусных белков [9–11]. Длительная персистенция высокоонкогенных типов ВПЧ более двух лет является наиболее опасным фактором прогрессии предрака шейки матки [12]. При персистенции ВПЧ 16-го типа риск развития CIN составляет 40–50%, 26-го типа — 30–40%, 31-го, 58-го, 82-го типов — по 20–30%, 18-го, 33-го, 35-го, 51-го, 52-го типов — по 10–20% [12]. При обследовании молодых женщин с ПВИ персистенция ВПЧ через 1 год выявлялась у 30%, через 2 года — у 9%, в то время как у женщин старшего возраста — у 50% [13].
В мировой практике используются различные классификации ПВИ и ассоциированных с ней заболеваний. Ориентировочная классификация ПВИ представлена J. Handley и соавт. [14]:
Аногенитальная ВПЧ-инфекция и ассоциированные с ВПЧ заболевания
ВПЧ-инфекция
1. Клинические формы (видимые невооруженным глазом или невидимые, но при наличии соответствующей симптоматики):
2. Субклинические формы (невидимые невооруженным глазом и бессимптомные, выявляемые только при кольпоскопии и/или цитологическом или гистологическом исследовании):
3. Латентные формы (отсутствие морфологических или гистологических изменений при обнаружении ДНК ВПЧ).
Заболевания, ассоциированные с ВПЧ
Клинические и субклинические формы:
Кроме этого, в литературе при описании поражений шейки матки, ассоциированных с ВПЧ, применяют классификацию по Папаниколау — в зависимости от степени изменений в мазках выделяют 5 классов. ВОЗ рекомендует использовать терминологическую систему Бетесда (The Bethesda System — TBS) — норма, ASCUS (Atypical squamous cells of undertermined significance (атипичные клетки плоского эпителия неясного значения)), LSIL (Low grade squamous intraepithelial lesion (интраэпителиальное плоскоклеточное поражение низкой степени тяжести)), HSIL (High grade squamous intraepithelial lesion (интраэпителиальное плоскоклеточное поражение высокой степени тяжести)), карцинома. Однако TBS не исключает использование терминов CIN и «дисплазия».
Согласно существующим принципам по ведению больных с клиническими проявлениями, связанными с ВПЧ, лечение аногенитальных ВПЧ-поражений направлено на разрушение тем или иным методом папилломатозных очагов, возникающих на месте внедрения вируса. Именно такой подход приведен во всех основных рекомендациях по ведению больных с ВПЧ-инфекцией (CDC, Европейских рекомендациях, рекомендациях ВОЗ). Такой подход представлен и в рекомендациях Российского общества дерматовенерологов и косметологов.
Как для лечения клинических проявлений ВПЧ-инфекции, так и ассоциированных с ней заболеваний (в первую очередь это касается CIN II и CIN III), применяют деструктивные методы — хирургические, физические (крио-, электро- или лазеротерапия, радиоволновая хирургия) и химические.
При CIN I тактика может различаться в зависимости от величины поражения шейки матки, наличия другой патологии и возможностей самой пациентки [15]. Также в этом вопросе нет единогласия и ввиду возможности регресса данного заболевания. Общеизвестно, что хирургическое лечение может повлечь за собой до 40% осложнений (шеечное кровотечение, стриктуры цервикального канала, экстравазаты и субэпителиальные гематомы, истмико-цервикальную недостаточность, эндометриоз и др.), поэтому однозначность такого подхода при CIN I у женщин, зачастую еще не реализовавших репродуктивный потенциал, подлежит сомнению [16]. Установили, что прогностическими критериями течения CIN I могут служить анамнестические данные (возраст пациенток, возраст начала половой жизни, интервал между возрастом менархе и возрастом начала половой жизни) и данные клинико-лабораторных методов исследования — уровни вирусной нагрузки ВПЧ 16/18, клинико-кольпоскопического и иммуногистохимического индекса p16ink4a [16].
Одним из главных методов, позволяющих снизить заболеваемость РШМ, являются профилактические осмотры с проведением активного скрининга, направленного на выявление патологии шейки матки.
В ходе профилактического осмотра основными диагностическими методиками являются цитологическое исследование, кольпоскопия и определение ВПЧ.
С введения государственных программ ранней диагностики РШМ накоплен большой опыт по цитологическому скринингу, изложенный во множестве публикаций [17]. Одним из критериев оценки эффективности скрининга является изменение структуры патологии шейки матки за счет увеличения количества ранних предраковых состояний эпителия. Анализ литературы показывает, что при хорошо организованном цитологическом скрининге с широким охватом населения эффективность его очень высока и популяция женщин, прошедших обследование, имеет низкий риск развития РШМ. У них в 5 раз снижена вероятность обнаружения рака и в 10 раз — смертность по сравнению с группой необследованных женщин [18]. При этом вероятность пропуска заболевания на его начальном этапе составляет 1–2%, что связывают с недостаточной чувствительностью цитологических исследований [18]. Неправильный забор материала или недостаточная квалификация врача-цитолога могут приводить к большому количеству ложноотрицательных ответов, требующих дополнительных уточняющих методик. Накопленный опыт в нашей стране показал наилучшие результаты обследований в системах ведомственных лечебных учреждений, где охват прикрепленного контингента женщин достигает 100%, что в результате приводит к отсутствию случаев инвазивного РШМ в течение 2–5 лет [17].
Следующим после цитологического исследования важным диагностическим методом профилактического осмотра женщин является кольпоскопия. Среди задач, поставленных Министерством здравоохранения РФ на ближайшие годы, по внедрению стандартов диагностики и лечения в повседневную клиническую практику кольпоскопическое исследование является обязательным для первичных пациенток женских консультаций с ненормальными цитологическими мазками, женщин с патологией шейки матки и любыми заболеваниями влагалища, вульвы, шейки (код кольпоскопии А03.20.001) [17]. Таким образом, кольпоскопия является одним из ведущих методов обследования женщин, дополняющих цитологическое исследование.
Поскольку основная роль в генезе заболеваний шейки матки принадлежит ВПЧ, то тестирование на этот вирус является также важнейшим инструментом профилактических мероприятий. Особую озабоченность представляют пациентки с длительной персистенцией высокоонкогенных типов ВПЧ в сочетании с ASCUS. Женщинам, инфицированным ВПЧ, особенно типами высокого онкологического риска, требуется более активная диагностическая и терапевтическая тактика, соблюдение курсов терапии, строгий комплаенс.
При активном выявлении заболеваний шейки матки в ходе профилактических осмотров, а также при их ранней диагностике у женщин, самостоятельно обратившихся к гинекологу, чрезвычайно важным является выделение группы пациенток с минимальными субклиническими формами болезни для своевременного лечения и диспансерного наблюдения в женских консультациях [17]. В этой связи важное значение приобретает необходимость длительного контроля и фармакотерапии, направленной на подавление вируса, а также готовность пациентки следовать рекомендованному лечению.
Ранняя диагностика и принципы лечения начальных проявлений CIN остаются одной из дискутабельных проблем в акушерско-гинекологической практике. При небольшом поражении чаще рекомендуют оставить женщину под наблюдением и периодически выполнять обследования — тесты на ВПЧ, кольпоскопию, цитологию. Очень важно при этом диагностировать и лечить воспалительные, дисгормональные и другие заболевания урогенитального тракта. Большую роль в определении тактики ведения больных в этих случаях имеет желание пациентки и ее возможность регулярного посещения врача для проведения обследования и желание следовать рекомендациям врача в выборе медикаментозной терапии. Выжидательная тактика при ПВИ часто связана с тем, что носительство и персистенция свидетельствуют не о предраковом процессе как таковом, а о многократно повышенном риске возникновения последнего, усугубляющегося при дополнительных факторах риска у ряда пациенток [25]. Так, G. Но и соавт. [10] показали, что персистенция ВПЧ более 6 мес встречалась с увеличением возраста женщины и обусловлена типом ВПЧ.
Появление патологических изменений в цитологических мазках возрастает по мере персистенции ВПЧ высокого канцерогенного риска у большинства женщин. Согласно данным литературы после инфицирования ВПЧ CIN II–III развивается уже через 3 года у 27% женщин. При анализе исходов CIN, ассоциированных с ВПЧ, было показано, что при CIN I регрессия наблюдается в 57%, персистенция — в 32%, прогрессия — 11%, а развитие инвазивного рака — только в 1% случаев. При CIN II регрессия наблюдается в 43%, персистенция — в 35%, прогрессия — в 22%, а развитие инвазивного рака — в 5% случаев. В то же время при CIN III малигнизация происходит более чем в 12% случаев, а регрессия — лишь в 32% [26, 27].
В связи с вышесказанным, другим подходом в тактике ведения пациенток с начальными проявлениями CIN может быть назначение противовирусной терапии и контроль со стороны врача за четким выполнением рекомендаций и схем медикаментозной терапии.
Этиопатогенез минимальных изменений эпителия (легкая дисплазия или атипические изменения неясной причины) связан с ВПЧ, который на этой стадии заболевания еще находится в клетке в эписомальном состоянии и не повреждает ее геном. Следовательно, именно на этом этапе развития системный и местный иммунитет будет играть ведущую роль в прогнозе развития болезни. По данным биопсий шейки матки латентные формы инфекции выявляются у 8,1% женщин, а субклинические у 40–60% [25, 28]. Именно поэтому медикаментозная терапия при начальных формах поражения эпителия должна быть направлена на подавление вируса при соблюдении комплаенса, понимании пациенткой необходимости завершения курса для повышения эффективности лечения.
В своем исследовании R. Richard и B. Barron [29] показали, что среднее время для развития карциномы in situ составляет примерно 5 лет для больных со слабой дисплазией, 3 года — с умеренной и 1 год — с выраженной дисплазией. Это позволило предположить, что 66% всех дисплазий будет прогрессировать до карциномы, но достаточно длительное время, которое необходимо использовать для раннего выявления и лечения. В клинической ситуации, несмотря на то, что имеется достаточный период безопасного времени для динамического наблюдения, многие врачи и пациентки после информирования о диагнозе не хотят длительно наблюдаться даже с начальной патологией эпителия. Женщины хотят быть излеченными сразу, что часто предопределяет активную тактику ведения больных, включая деструкцию активной зоны трансформации и иммуно/противовирусную терапию [29–33].
Таким образом, у пациенток с «минимальным» повреждением эпителия шейки матки, например ASCUS, с наличием цитоплазматического эффекта ВПЧ (койлоцитоз при цитологическом исследовании) и положительном ВПЧ-тесте и его высоком титре, может оказаться актуальным применение препарата с двойным противовирусным действием — инозин пранобекс (Изопринозин).
Это один из немногих иммунотропных и противовирусных препаратов, в инструкции по применению которого указана терапия заболеваний, вызванных ВПЧ. Он также входит в Европейскую классификацию методов лечения аногенитальных бородавок [34]. В настоящее время накоплен огромный опыт применения Изопринозина, так как используется он с 1970-х гг. и зарегистрирован в большинстве стран Европы.
Изопринозин — иммуномодулятор, стимулирующий противовирусную защиту организма. Помимо иммунотропного, Изопринозин обладает прямым противовирусным действием, угнетая синтез вирусов путем встраивания инозин-оротовой кислоты в полирибосомы пораженной вирусом клетки и нарушая присоединение адениловой кислоты к вирусной РНК.
Таким образом, обладая противовирусным действием и оказывая влияние на противовирусный иммунитет, Изопринозин прямо и косвенно способен подавлять репликацию ВПЧ и образование вирусных белков. Эти эффекты могут изменять механизм взаимодействия ВПЧ и макроорганизма, препятствуя переходу вируса из транзиторной в персистирующую форму, а также влияя на клиническую манифестацию инфекции.
Одним из показаний применения препарата являются инфекции, вызванные вирусом папилломы человека: остроконечные кондиломы, ПВИ вульвы, вагины и шейки матки (в составе комплексной терапии).
При инфекциях, вызванных ВПЧ, Изопринозин назначают по 3 г/сут (2 таблетки 3 раза в сутки) как дополнение к местной терапии или хирургическому вмешательству в течение 14–28 дней или 5 дней в неделю последовательно в течение 1–2 недель в месяц в течение 3 месяцев. При дисплазии шейки матки, ассоциированной с ВПЧ: по 2 таблетки (1000 мг) 3 раза в сутки в течение 10 дней, далее 2–3 курса с интервалом 10–14 дней.
Улучшение морфологической картины эпителия вульвы показано в исследовании Sun Kuie Tay [32]. Инозин пранобекс назначали по 1 г 3 раза в сутки в течение 6 недель. Положительный эффект был достигнут у 63,5% больных, а в группе, принимавшей плацебо, — у 16,7%.
В другом исследовании при монотерапии Изопринозином по 3 г в сутки у 44 женщин с CIN I (длительность лечения 10 дней) и CIN II (длительность лечения 21 день) установлено, что выраженный клинический эффект наблюдался у 88,6% пациенток — полностью исчезало поражение эпителия экзоцервикса, что подтверждалось кольпоскопически и гистологически [35].
В работе Т. В. Клинышковой и соавт. [36] показана высокая частота регресса CIN I (70%) и прекращения выделения ВПЧ (83,3%) при использовании Изопринозина в режиме монотерапии и комбинированного лечения в сочетании с деструкцией у пациенток с ВПЧ-ассоциированными поражениями шейки матки. Изопринозин назначали по 3 г в сутки двумя 10-дневными курсами — за 1 месяц до деструкции и с 1-го дня деструкции при четком контроле за выполнением курса лечения.
В. Н. Прилепская сообщает о прекращении выделения ВПЧ у 65,6% больных после комбинированной терапии (Изопринозин + деструкция очагов) CIN низкой степени [3]. При использовании только деструкции очагов этот результат был достигнут у 46,9% больных. Изопринозин назначали по 1 г 3 раза в сутки в течение 5 дней за 7–10 дней до проведения деструкции.
Похожие результаты — прекращение выделения ВПЧ у 77% больных — показаны в исследовании И. В. Шевниной (2009 г.) при комбинированной терапии женщин с CIN и аногенитальными бородавками. Изопринозин назначали по 1 г 3 раза в сутки в течение 10 дней, затем по 0,5 грамма 3 раза в сутки в течение 20 дней.
В другом исследовании Изопринозин назначали женщинам с патологией шейки матки, ассоциированной с ВПЧ [37]. Препарат назначали после проведения обследования и противовоспалительной терапии по 3 г в сутки в течение 10 дней. Элиминация ВПЧ достигнута у 95,3% пациенток.
Есть и другие исследования, в которых показано прекращение выделения ВПЧ из очагов поражения у 69,6–97,8% женщин, принимавших Изопринозин [30, 38, 39].
Представленные данные свидетельствуют о возможной эффективности монотерапии Изопринозином при бессимптомном вирусовыделении, когда применение деструктивных методик не показано.
Сравнительная оценка лечения с применением Изопринозина и без него показала преимущество дополнительной лекарственной терапии вне зависимости от степени онкологического риска. Так, в группе женщин с начальными изменениями эпителия самостоятельное улучшение после санации влагалища достигнуто в 64,9% наблюдений, а при применении Изопринозина в 80,4% случаев [17]. У пациенток с изменениями легкой степени тяжести, выявленными при кольпоскопическом или цитологическом исследованиях, даже в случаях отсутствия самостоятельных улучшений более 3 мес Изопринозин был эффективен почти в 85% наблюдений [17].
Результаты исследования, проведенного в ФГБУ НЦАГиП им. акад. В. И. Кулакова [40, 41], показали, что инозин пранобекс подавляет репликацию высокоонкогенных типов ВПЧ и способствует исчезновению койлоцитарной атипии у 94% пациенток с поражением эпителия шейки матки.
При использовании Изопринозина в режиме монотерапии и в комбинации с деструкцией у пациенток с ВПЧ-ассоцированными поражениями низкой степени получена высокая частота регресса CIN I, прекращение выделения ВПЧ, снижение вирусной нагрузки, активация интерферонового ответа в сравнении с традиционными подходами [16]. Через 4 мес у пациенток, принимавших Изопринозин, в 2 раза снизилась частота экспрессии онкобелка Е7 по сравнению с контрольной группой. Кроме этого были отмечены и другие значимые позитивные изменения в отличие от контрольной группы, где имелась лишь тенденция к этому. Выявленные различия позволяют расценивать их как патогенетические предпосылки неполного клинического эффекта и отдаленного рецидивирования заболевания у пациенток контрольной группы. Эффективность лечения в группе пациенток, принимавших Изопринозин, по окончании лечения была в 1,4 раза выше, чем при традиционном лечении.
Заключение
Таким образом, основными профилактическими мероприятиями, направленными на раннее выявление и преодоление прогрессирования ВПЧ-ассоциированной патологии шейки матки, могут быть:
Многочисленные исследования, проведенные во многих странах мира, в том числе и в России, показали, что при применении Изопринозина (в комбинации с деструкцией или в виде монотерапии), благодаря его двойному противовирусному и иммуномодулирующему действию, подавляющему репликацию ВПЧ, повышается эффективность терапии заболеваний шейки матки, ассоциированных с ПВИ.
Для достижения этих результатов важным является соблюдение дозировок и продолжительности лечения. Как было указано выше, наиболее опасной с точки зрения прогрессирования дисплазии является персистенция ВПЧ, при которой вирус встраивается в геном эпителиальной клетки. Противовирусное действие при этом должно продолжаться несколько месяцев, чтобы захватить несколько циклов полного обновления эпителия. Именно поэтому для консервативной терапии дисплазий предлагается длительное многокурсовое лечение — два-три 10-дневных курса с интервалом 10–14 дней. Такие курсы, как показали результаты многочисленных исследований, приведенные в данной работе, позволяют достичь высокой эффективности лечения. Чем ниже уровень выполнения пациентками предписаний врача, тем ниже уровень эффективности лечения и выше риск рецидивирования и прогрессирования патологии.
Литература
А. М. Соловьев*, кандидат медицинских наук
Д. В. Логвинова**
*ГБОУ ВПО МГМСУ им. А. И. Евдокимова МЗ РФ, Москва
**НПЦДК ДЗМ, Москва