Лечу хеликобактер антибиотиками начался понос что делать
Значение дисбиотических нарушений толстой кишки в патогенезе Helicobacter pylori- ассоциированных заболеваний гастродуоденальной зоны. Роль пребиотико
Изучено влияние пребиотического комплекса на результаты эрадикационной антихеликобактерной терапии и показана его эффективность по предупреждению развития антибиотикоассоциированной диареи у пациентов, имеющих прогностические факторы неблагоприятного тече
Influence of prebiotic complex on the results of eradication anti-helicobacter therapy was studied, and its efficiency in prevention of antibiotic-associated diarrhea in patients having forecasting factors of adverse clinical course of early post-eradication period was shown.
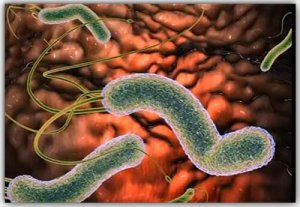
Инфекция Helicobacter pylori (Н. pylori) является ведущей причиной хронических заболеваний желудка и двенадцатиперстной кишки. Эрадикация Н. pylori является основным стандартом лечения хеликобактер-ассоциированных заболеваний гастродуоденальной зоны, что отражено в международных соглашениях (Маастрихтские соглашения 1–3, соответственно 1996, 2000 и 2005 гг.) [1].
Следует иметь в виду, что хеликобактериоз проявляется не только местными эрозивно-язвенными поражениями гастродуоденальной зоны, но и оказывает системное влияние на организм человека. Инфицирование макроорганизма и длительное персистирование H. pylori нарушает микроэкологию пищеварительного тракта и может рассматриваться в качестве фактора, инициирующего и усугубляющего нарушения микробиоценоза толстой кишки [2, 3]. При H. pylori-позитивной язвенной болезни дисбиоз кишечника выявляется у 92% пациентов (НИИ питания РАМН), выраженность дисбиотических изменений достоверно связана со степенью обсемененности H. pylori [4]. Антихеликобактерная терапия, включающая применение антибиотиков, также приводит к угнетению облигатной микрофлоры и последующей колонизации слизистой оболочки желудочно-кишечного тракта патогенной и условно-патогенной микрофлорой [5].
Дисбиоз толстой кишки может стать причиной развития вторичного иммунодефицита (местного и общего), что в свою очередь вызывает снижение защитных сил организма и является важным фактором в патогенезе H. pylori-ассоциированной патологии. При этом важно, что сопутствующие дисбиотические изменения кишечника могут достигать определенного критического уровня и превращаться в самостоятельный фактор агрессии. В этих условиях прогредиентно нарастает выраженность клинических симптомов воспалительных заболеваний гастродуоденальной области, удлиняются сроки их существования, утяжеляется общее состояние, ухудшаются показатели результатов лечения и качество жизни пациентов, клиническое течение приобретает часто рецидивирующий характер [6, 7].
Иммуногенная функция нормофлоры заключается в стимуляции синтеза иммуноглобулинов, интерферона, цитокинов; в активировании созревания системы фагоцитирующих мононуклеаров; в повышении содержания комплемента и пропердина, активности лизоцима; выработке бактериальных модулинов. В качестве медиаторов действия бактериальных метаболитов выступают гистамин, серотонин, простагландины, лейкотриены, короткоцепочные жирные кислоты. Воздействие микробных метаболитов и медиаторов их действия направлено на модуляцию пролиферации, дифференцировки, апоптоза и метаболических реакций эукариотических клеток. Нормофлора способна воздействовать на дифференцировку Т-хелперов и таким образом влиять на соотношение про- и противовоспалительных цитокинов. S. Roos, C. Johnson (2003 г.) показали, что некоторые штаммы лактобактерий обладают кислотоустойчивостью и антагонизмом к H. pylori in vivo и in vitro. Lactobacilli spp., как и Bifidobacterium spp., выделяют бактериоцины, способные ингибировать рост H. pylori и нарушать адгезию микроба к эпителиальным клеткам желудка [8–10].
Исследования последних лет показали, что препараты, улучшающие микробиоценоз кишечника, не только повышают эффективность эрадикационной терапии, но и предупреждают развитие и позволяют в значительной степени снизить побочные эффекты антибиотиков, входящих в стандартные схемы антихеликобактерной терапии, такие как антибиотикоассоциированная диарея, тошнота, неприятный привкус в ротовой полости и т. п. [10–14].
Независимо от индивидуальных различий в составе кишечной микрофлоры, кишечный микробиоценоз у каждого человека функционирует как единая экосистема и целостный метаболический орган, который обеспечивает необходимое количество и профиль конечных метаболитов, среди которых наиболее важную роль играют короткоцепочечные жирные кислоты (КЦЖК). КЦЖК — основной продукт микробной ферментации анаэробными бактериями углеводов, жиров и белков. К ним относятся уксусная (С2), пропионовая (С3), изомасляная, масляная (С4), изовалериановая, валериановая (С5), изокапроновая и капроновая (С6) кислоты [7, 15, 16].
Неразветвленные КЦЖК — уксусная, пропионовая и масляная — образуются при анаэробном брожении углеводов, тогда как метаболизм белков ведет к образованию разветвленных кислот — изомасляной (из валина) и изовалериановой (из лейцина). В течение суток синтезируется более 300 ммоль/л КЦЖК. Максимальная концентрация КЦЖК достигается в проксимальных отделах толстой кишки 70–140 ммоль/л — самом мощном биокорректорном участке желудочно-кишечного тракта. В дистальной части содержание КЦЖК снижается до 20–70 ммоль/л [16].
КЦЖК участвуют в регуляции большинства физиологических эффектов облигатной микрофлоры толстой кишки. Так, они являются основным источником питания для колоноцитов, обеспечивая их энергией (на 70%), стимулируют регенерацию эпителия, обладают антибактериальной активностью, обеспечивают баланс микробной экосистемы, препятствуя ее контаминации патогенной микрофлорой, поддерживают детоксицирующую функцию печени за счет участия в энтерогепатической циркуляции желчных кислот, обладают антиканцерогенным и антивирусным действием, оказывают влияние на экспрессию генов в колоноцитах, являются активным модулятором иммунной системы, регулируют моторную функцию кишечника (табл. 1) [16–18].
КЦЖК выступают в роли триггера и запускают множество физиологических и клинических эффектов на разном удалении от места их синтеза. Такие молекулы принято относить к химическим сигнальным веществам. На слизистой оболочке ЖКТ, в том числе и в гастродуоденальной зоне располагаются рецепторы, которые «распознают язык» химического сигнала КЦЖК. Многообразное действие КЦЖК и клинические проявления этого действия позволяют относить молекулы КЦЖК к классу универсальных сигнальных химических носителей и передатчиков информации в организме человека. Несмотря на то, что все КЦЖК участвуют в обеспечении основных функций иммунитета, в роли особенно активного иммуномодулятора выступает масляная кислота. Масляная кислота обладает рядом иммуномодулирующих эффектов:
Основными продуцентами бутирата являются не бифидо- и лактобактерии, а эубактерии, пептококки, фузобактерии и клостридии (поэтому большинство пробиотиков не влияют на синтез масляной кислоты). Эта КЦЖК активно абсорбируется в цитоплазму колоноцита, где в митохондриях из нее образуется АТФ. 70% энергии идет на обеспечение локальных процессов в толстой кишке, а оставшиеся 30% этой энергии расходуются на нужды целого организма. Рецептор-опосредованным путем масляная кислота инициирует активацию и/или ингибирование локальных и системных иммунных реакций [16].
В России с 2011 г. для лечения различных заболеваний ЖКТ применяется препарат Закофальк®. В состав препарата входит масляная кислота и инулин в дозе 250 мг, которые помещены в полимерную мультиматриксную капсулу NMX. В отличие от ранее известных про- и пребиотиков, которые стимулируют рост нормофлоры толстой кишки, что опосредованно приводит к образованию КЦЖК, в первую очередь ацетата и пропионата, Закофальк® напрямую доставляет масляную кислоту и инулин в толстую кишку в заданном количестве. Пребиотический комплекс Закофальк® обеспечивает возможность реализации сложного каскада иммунобиологических, метаболических и других свойств, присущих нормально функционирующему микробно-тканевому комплексу кишечника.
Инулин, (C6H10O5)n, органическое вещество из группы полисахаридов (фруктанов), полимер D-фруктозы, построенный из остатков D-фруктофуранозы, связанных 2,1-бета связями.
Что касается медицинской классификации инулина, в большинстве публикаций его относят к группе растворимых пищевых волокон (не целлюлозный полисахарид). Кроме того, способность инулина избирательно стимулировать бифидо- и лактобактерии, являющиеся представителями нормальной микрофлоры кишечника, позволяет назвать данное вещество истинным пребиотиком.
При попадании в пищеварительный тракт инулин проходит в неизмененном виде в желудок и тонкую кишку. В толстой кишке фруктоолигосахариды являются питательным субстратом исключительно для бифидобактерий и отдельных видов лактобацилл, которые обладают ферментной системой бета-фруктозидаз, позволяющей им расщеплять фруктоолигосахариды до масляной кислоты. Таким образом, инулин выступает не только как селективный пребиотический фактор для микрофлоры толстой кишки, но и как промоутер синтеза эндогенной масляной кислоты.
Растительные волокна инулина, будучи нерастворимыми в тонкой кишке, в толстой кишке создают дополнительные площади (помимо поверхности слизистой оболочки), к которым фиксируются сахаролитические бактерии. Благодаря этому в просвете толстой кишки во много раз возрастает число мест для адгезии и формирования микроколоний лакто- и бифидобактерий, что приводит к значительному увеличению количества присутствующих на единицу объема кишки микроорганизмов, и, как следствие этого, резко возрастает метаболическая активность кишечного содержимого с образованием различных важных для организма энергетических и пластических субстанций. Lactobacilli spp., как и Bifidobacterium spp., выделяют бактериоцины, способные ингибировать рост Н. pylori и нарушать адгезию микроба к эпителиальным клеткам желудка.
Масляная кислоты С3Н7СООН является органической кислотой, вырабатывающейся в просвете толстой кишки в процессе бактериальной ферментации неперевариваемых пищевых углеводородов. Бутират используется организмом в качестве энергетического субстрата для обеспечения процессов пролиферации и дифференцировки колоноцитов, для энергообеспечения ферментативных процессов индигенной флоры. Именно эта кислота контролирует механизмы, инициирующие апоптоз ненужных в функциональном отношении колоноцитов и раковых клеток, модулирует экспрессию генов, регулирующих клеточный цикл, нивелирует действие супероксидных радикалов. Масляная кислота играет основную роль в обеспечении локальных и системных иммунных механизмов: путем активации локальных макрофагов для увеличения презентации антигенов B-лимфоцитам и увеличения производства секреторного иммуноглобулина А местно и системно, модулирования цитокиновых профилей и активации синтеза интерферона. Масляная кислота, являясь универсальным сигнальным химическим носителем передачи информации в организме человека, регулирует адаптивные реакции не только на уровне микробиоценоза толстой кишки (предупреждает развитие кишечного дисбиоза), но и оказывает общее иммуномодулирующее действие.
Клинически манифестной формой кишечного дисбиоза при проведении эрадикационной терапии является антибиотикоассоциированная диарея. На базе городских поликлиник г. Москвы было проведено открытое сравнительное рандомизированное многоцентровое исследование по изучению влияния препарата Закофальк® на эффективность и переносимость эрадикационной терапии.
Целью настоящего исследования было изучение влияния пребиотического комплекса Закофальк® на результаты эрадикационной терапии и его эффективности по предупреждению развития антибиотикоассоциированной диареи при проведении антихеликобактерной терапии у пациентов, имеющих прогностические факторы неблагоприятного течения раннего постэрадикационного периода.
Материал и методы исследования
В рамках сравнительного открытого рандомизированного исследования было обследовано 115 человек (мужчин — 52, женщин — 63), средний возраст 42,5 лет (20–65 лет).
Критерии включения: больные язвенной болезнью, ассоциированной с Н. pylori, в стадии обострения с наличием язвенного дефекта в желудке или в двенадцатиперстной кишке; наличие не менее двух факторов риска развития антибиотикоассоциированной диареи (постинфекционный синдром раздраженного кишечника, сахарный диабет 2-го типа, указание в анамнезе на проведение антибактериальной терапии вне связи с основным заболеванием в течение ближайших 6 месяцев, хронические заболевания гепатобилиарной системы и поджелудочной железы, длительный прием гормональных или химиотерапевтических препаратов, синдром короткой тонкой кишки, дивертикулярная болезнь толстой кишки, онкологические заболевания толстой кишки в анамнезе).
Обследование включало: клиническое наблюдение в динамике, проведение эзофагогастродуоденоскопии с взятием гастробиоптатов слизистой оболочки края язвы с последующей их гистобактериоскопией и проведением уреазного теста (до и через 4 недели от окончания эрадикационной терапии). В ходе исследования анализировались результаты исследования состава кишечной микрофлоры. Исследование иммунного статуса включало определение в сыворотке крови IgG, IgM, IgA, IgE.
После включения в исследование больные были рандомизированы на две группы. Пациенты основной группы (60 человек) помимо препаратов эрадикационной терапии (Нексиум 20 мг 2 раза + кларитромицин 500 мг 2 раза + амоксициллин 1000 мг × 2 раза 14 дней) получали Закофальк® 3 таблетки в сутки, а больные группы сравнения (55 человек) — ту же терапию, но без применения препарата Закофальк®. До начала терапии нарушений кишечной моторики (поносов либо запоров) ни у кого не было.
Результаты и их обсуждение
Через 7 дней от включения в исследование при повторном опросе и осмотре синдром кишечной диспепсии, индуцированный проведением эрадикационной терапии, был отмечен у 34 (68%) пациентов группы сравнения: вздутие — 25, урчание — 28; жидкий стул до 3 раз в сутки — 25, жидкий стул более 3 раз в день — 9. Девять пациентов этой группы (18%) в течение первой недели лечения отказались от дальнейшего приема антибиотиков. При этом в основной группе, пациенты которой получали Закофальк®, не было зафиксировано возникновение диареи, а вздутие или урчание живота было отмечено лишь у 14 пациентов (23,3%). По завершении антибиотикотерапии на 14-й день лечения 41 (82%) пациент группы сравнения отмечал послабления стула от 3 до 5–7 раз в сутки. У 7 (11,7%) пациентов основной группы отмечалось учащение дефекаций до 5 раз в сутки. Таким образом, включение препарата Закофальк® в схему эрадикационной терапии улучшает переносимость лечения антибиотиками даже у пациентов с высоким риском антибиотикоассоциированной диареи (табл. 2).
Исходный уровень сывороточных иммуноглобулинов не имел значимых отличий в основной группе и группе сравнения, средние его значения были незначительно снижены. Уровень IgE был повышен только у больных язвенной болезнью двенадцатиперстной кишки с наличием участков лимфоидной гиперплазии в антральном отделе желудка, средний его уровень в основной группе составил 64,25 ± 11 кЕ/л и 55 ± 12 кЕ/л в группе сравнения. После проведения эрадикационной схемы лечения с включением препарата Закофальк® у пациентов основной группы наблюдалась небольшая тенденция к повышению уровня IgA до 3,0 ± 0,5 г/л (исходный 0,65 ± 0,2 г/л) и значительное снижение IgE до 43 ± 11 кЕ/л. У пациентов группы сравнения такой тенденции не наблюдалось. Повышение сывороточного IgA может отражать повышение секреторного IgA на слизистой оболочке желудка, что свидетельствует об усилении реакций местного иммунитета. Снижение уровня IgE, по-видимому, связано с усилением протективной и детоксицирующей функций эндосимбиотных бактерий. Повышение сывороточных IgA и снижение IgE после лечения препаратом Закофальк® сочеталось со стабильным исчезновением клинических признаков обострения и эндоскопически подтвержденным рубцеванием язв у всех пациентов основной группы (табл. 3).
При микробиологическом исследовании фекалий в исходном периоде достаточно выраженные изменения соотношения представителей кишечной микрофлоры выявлены у большинства обследованных больных в обеих группах, в первую очередь отмечалось снижение уровня бифидо- и лактобактерий. После курса эрадикационной терапии у пациентов, принимавших Закофальк®, выявлено достоверное увеличение количества бифидобактерий и лактобактерий, а также достоверное уменьшение количества патогенных и условно-патогенных бактерий. В группе сравнения обращает внимание угнетение микробного роста представителей нормальной кишечной микрофлоры и увеличение степени дисбиоза кишечника. Таким образом, полученные данные в очередной раз подтверждают отрицательное влияние стандартной эрадикационной терапии на микробный состав кишечника, что имеет особое значение для пациентов с сопутствующими заболеваниями ЖКТ, увеличивающими риск развития кишечного дисбиоза и его клиническое проявление — антибиотикоассоциированной диареи (табл. 4, 5).
Достижение эрадикации H. pylori было зафиксировано у 52 (86,7%) пациентов основной группы и у 17 (31%) из группы сравнения, что может зависеть от более четкого соблюдения комплаентности терапии, а также способности препарата Закофальк® потенцировать противовоспалительный эффект антибиотиков.
Проводилась морфологическая оценка из краев язвенных дефектов до начала антихеликобактерной терапии и по ее завершении. Полученные данные свидетельствуют, что включение в терапию препарата Закофальк® приводит к улучшению клеточного состава слизистой оболочки в краях язвы. Так, значительно уменьшается нейтрофильная и лимфоцитарная и плазмоцитарная инфильтрация, что свидетельствует об уменьшении воспалительного и иммуно-воспалительных процессов (табл. 6, 7).
Выводы
Результаты исследования показывают несомненное преимущество комплексного лечения язвенной болезни, ассоциированной с H. pylori, с включением пребиотика Закофальк® по сравнению со стандартной эрадикационной схемой.
На основании полученных данных можно сделать следующие выводы:
Литература
Л. И. Буторова*, кандидат медицинских наук
Т. А. Плавник**
Н. Г. Кадникова***
С. Р. Рекель****
* ГИУВ МО РФ; ГБУЗ ГП № 209 ДЗМ, Москва
** ГБУЗ ГП № 195 ДЗМ, Москва
*** ПК № 230 ДЗМ, Зеленоград
**** ФГБУ ПК № 2 УДП РФ, Москва
Победим хеликобактер: лечение антибиотиками
Заболевания ЖКТ часто вызывают ощущение дискомфорта в животе, тошноту, неприятную отрыжку и другие симптомы, кроме того, есть несколько факторов, которые могут вызвать плохое самочувствие, и один из них – хеликобактер пилори.
Хеликобактер пилори – инфекционное бактериальное заболевание, которое развивается в полости желудка и двенадцатиперстной кишки. Инфекция способна вызвать осложнения в виде гастрита, язв и других заболеваний, которые даже опасны для жизни человека.
По каким причинам в организме появляется бактерия?
Бактерия хорошо выживает в кислотной среде, поэтому она беспрепятственно попадает в желудок и его слизистую, начиная разрушать все здоровые ткани.
Вследствие заражения данной бактерией, у человека могут возникнуть эрозии, гастрит и заканчивается все язвой, и если не обнаружить заболевание на раннем сроке и не начать лечение, может развиться рак желудка.
Заражению подвержены люди, которые не следят за личной гигиеной, ведут грязный образ жизни и т.п. Также в группе риска те, кто живет в общежитиях, интернатах, в детдомах, и работники медицины.
Далее вы узнаете о симптомах данного заболевания, о том, как диагностируют и собственно лечат хеликобактериоз.
Симптоматика
Хеликобактер: лечение антибиотиками
Попадая в организм, бактерия начинает свое развитие, что вызывает плохое общее состояние организма, и чаще всего симптоматика хеликобактериоза проявляется следующим образом.
Спустя неделю после заражения, человек страдает от блей в брюшной области, ощущение дурноты, отрыжку. Но такие симптомы можно перепутать с воспалением ЖКТ, и данные ухудшения в состоянии здоровья проходят буквально спустя несколько дней, что и позволяет человеку не обращать внимание и не думать о чем-то серьезном.
Но бактерии остаются в организме больного, но они могут бездействовать на протяжении нескольких лет, а могут начать свои разрушительные действия сразу. Часто активность данных бактерий вызывают определенные факторы, к таким относят:
С симптомами хеликобактериоза вас ознакомит видеосюжет:
Чтобы поставить окончательный диагноз – хеликобактериоз, врачами назначаются следующие исследования организма больного:
Данные исследования являются не дорогими и быстрыми, касательно получения результата. Но тут следует отметить то, что неинвазивные тесты часто показывают ложноположительные результаты.
Как лечиться от хеликобактер пилори?
Диагностика хеликобактер: анализ крови
Бактерия хеликобактер пилори является очень живущим микроорганизмом, который способен выжить в кислотных условиях, отвратительно влияет на иммунную систему человека, а именно блокирует возможность уничтожения белыми кровяными тельцами (лейкоцитами) вредных живых организмов. И для того чтобы излечиться от данного паразита, необходимо пройти курс антибактериальной терапии.
Процесс уничтожения в организме данных бактерий носит свое отдельное название – « эрадикация », и состоит из нескольких схем. Во время лечения назначаются разные лекарственные препараты, относящиеся к разным группам действия. А антибактериальное лечение имеет три линии, о которых мы вам и расскажем.
Это последний вариант терапии из первой линии, он применяется к тем людям, которые не хотят принимать антибиотики или у них к ним нетерпимость. Данный вариант основан на приеме ИИП и раствора прополиса (30%) в течении 14 дней. Препараты необходимо пить натощак по 2 раза в день.
Вторая линия лечения от хеликобактериоза применяется тогда, когда первые схемы лечения не приносят положительных результатов. Вторая линия эрадикации также имеет несколько вариантов, а точнее, 3 варианта терапии:
В течении 14 дней больному прописывают прием препаратов с содержанием соли висмута и антисекреторные лекарства. Также назначают антибиотики « Метронидазол » или «Тетрациклин».
Третья линия заключается в дополнительных исследованиях, в том случае, если две предыдущие схемы были безрезультативными.
На данном этапе проводят исследования, которые позволяют определить чувствительность микроорганизмов, и определяются те антибиотики, которые должны повлиять на бактерии.
Анализы во время третьей линии терапии являются необходимыми из-за того, что данная бактерия очень устойчива к большому количеству антибиотиков.
Медицинскими учеными было выявлено антибиотики, к которым у бактерии есть наибольший иммунитет – « Метронидазол » и « Кларитромицин ». Данные антибактериальные препараты назначаются лишь в том случае, когда с помощью анализов на чувствительной бактерии было выявлено, что она подвергается данным антибиотикам.
К чему может привести игнорирование данного заболевания?
Антибактериальные препараты — против хеликобактер
В первую очередь стоит упомянуть о том, что заниматься самостоятельным лечением от хеликобактериоза категорически нельзя!
Лекарственные препараты, дозирование и длительность курса лечения определяется исключительно по результатам анализов и исследований, и исключительно квалифицированным врачом.
Но стоит отметить, что в запущенных случаях, даже самый высококвалифицированный и опытный врач может не помочь, а особенно, если болезнь была запущенна до того, что развилось онкологическое заболевание.
Поэтому, если у вас наблюдаются симптомы, связанные с заболеванием ЖКТ обращайтесь к врачу, проходите специальные обследования и при наличии в организме хеликобактер пилори начинайте лечение.
Врачами было доказан тот факт, что если один член семьи был заражен, вероятность того, что другие члены семьи также больны – 95%.
Профилактические действия
Часто заражены все члены семьи
Думаем, что многих заинтересовал вопрос о том, как же уберечь себя, от столь неприятного заболевания. Так вот, если у кого-то из ваших близких людей обнаружили данную бактерию, вам также необходимо обследоваться.
Чтобы уберечься от бактерии следите за личной гигиеной, питайтесь правильной и здоровой пищей, соблюдайте режим, повышайте иммунную систему.
Чтобы не было рецидива заболевания, врачами назначаются контрольные анализы по истечении 2-6 недель после выздоровления. Особенное внимание получают пациенты, которые страдают от осложнений инфекции (кровотечения, перфорация слизистой), для таких больных рецидив хеликобактериоза является очень опасным и может привести к смерти.
.gif)
_575.gif)
_575.gif)
.gif)