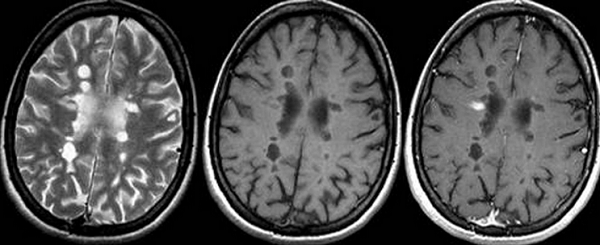
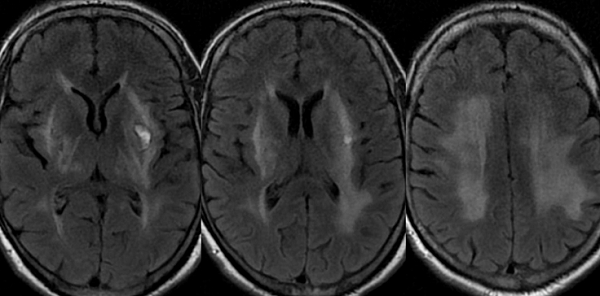
Лейкопатия головного мозга что это такое
Прогрессирующая сосудистая лейкоэнцефалопатия (I67.3)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Примечание. Из данной подрубрики исключена «Субкортикальная сосудистая деменция (F01.2).
Этиология и патогенез
Описаны семейные случаи заболевания с началом до 40 лет, без артериальной гипертензии. Более чем в 80% случаев болезнь дебютирует в возрастном промежутке от 50 до 70 лет.
Страдают также и более крупные артерии диаметром до 500 мкм, и все микроциркуляторное русло.
Эпидемиология
Болезнь (энцефалопатия) Бинсвангера встречается довольно часто. По данным клинико-компьютерно-томографического исследования, она составляет около 1/3 всех случаев сосудистой деменции.
Возраст. Более чем в 80% случаев болезнь дебютирует в возрастном промежутке от 50 до 70 лет.
Факторы и группы риска
Клиническая картина
Cимптомы, течение
Клиническая картина болезни Бинсвангера характеризуется прогрессирующими когнитивными нарушениями, нарушениями функции ходьбы и тазовыми расстройствами. На последнем этапе заболевания клиническая картина представлена слабоумием, полной беспомощностью больных (не ходят, не обслуживают себя, не контролируют функцию тазовых органов).
Картина слабоумия может значительно варьироваться по степени тяжести и особенностям симптоматики.
В целом для болезни Бинсвангера характерно неуклонно-прогредиентное течение, но возможны и периоды длительной стабилизации. Причинами слабоумия в этих случаях считаются разобщение корково-подкорковых связей, наступающее в результате поражения подкоркового белого вещества, а также дисфункция базальных ганглиев и таламуса.
Изменение походки на начальных стадиях болезни Бинсвангера заключаются в следующем: походка шаркающая или семенящая, мелкими шажками, «магнитная» (ноги как бы прилипают к полу). На следующей стадии она становится «осторожной», увеличивается опорная площадь стояния, распадается автоматизм ходьбы (диспраксия или апраксия ходьбы) и все более включается произвольный контроль за ходьбой – походка такого больного напоминает походку здорового человека, оказавшегося на ледяном поле.
Основные характеристики лобной диспраксии ходьбы, связанной с дезавтоматизацией ходьбы, следующие:
• замедление ходьбы;
• укорочение шага;
• затруднение в начале ходьбы (инициация ходьбы);
• неустойчивость при поворотах (постуральная дисфункция);
• расширение базы опоры;
• снижение длины шагов.
Для нарушения тазовых функций при болезни Бинсвангера характерно развитие «гиперактивности» («гиперрефлекторности») мочевого пузыря, что проявляется повышенной сократительной активностью детрузора. Гиперактивность мочевого пузыря характеризуется: учащенным мочеиспусканием; императивными позывами на мочеиспускание, которые по мере прогрессирования заболевания переходят в случаи императивного недержания мочи.
Двигательные нарушения могут также характеризоваться (помимо нарушения ходьбы): другой экстрапирамидной патологией в виде паркинсоноподобной симптоматики, а также легкими или умеренными центральными моно- или гемипарезами, часто быстро регрессирующими (регресс очаговой двигательной симптоматики становится неполным по мере прогрессирования заболевания). Характерен псевдобульбарный синдром.
Эмоционально-волевые нарушения представлены астеническим, неврозоподобным или астено-депрессивным синдром. По мере прогрессирования заболевания на первый план выходят не астения и депрессия, а нарастание эмоционального оскудения, сужение круга интересов и спонтанности.
В критериях подчеркивается, что у пациента должны отсутствовать множественные или двухсторонние корковые очаги по данным КТ и МРТ, и тяжелая деменция.
Диагностика
Осложнения
Транзиторные ишемические атаки (ТИА, преходящие нарушения мозгового кровообращения) характеризуются кратковременными симптомами локальной ишемии мозга.
ТИА обычно связаны с гемодинамической недостаточностью, возникающей при выраженном атеросклеротическом стенозе сонных или позвоночных артерий в их дистальных ветвях или артериальной эмболией.
В большинстве случаев транзиторные ишемические атаки разрешаются в течение 5-20 минут.
Клиническое значение ТИА состоит в том, что они служат предвестниками не только инсульта, но и инфаркта миокарда и представляют собой сигналы опасности, требующие от врача быстрых действий. Больных с ТИА необходимо госпитализировать в инсультное отделение для наблюдения, всестороннего обследования и проведения профилактики ишемического инсульта.
ТИА часто проявляются при снижении АД, физической нагрузке, натуживании, приеме пищи; при этом очаговые неврологические симптомы нередко проявляются на фоне предобморочного состояния, иногда по нескольку раз в день. Больные часто жалуются на предобморочное состояние, головокружение, нарушения зрения, слабость в конечностях, тошноту и рвоту, нарушения памяти, шум в ушах, нарушения чувствительности, неожиданную утрату равновесия.
Ишемический инсульт возникает в результате критического снижения или прекращения кровоснабжения участка мозга с последующим развитием очага некроза мозговой ткани.
Внутримозговое кровоизлияние возникает в результате разрыва патологически измененных сосудов мозга, приводящего к кровоизлияниям.
Прогрессирующая многоочаговая лейкоэнцефалопатия
Прогрессирующая многоочаговая лейкоэнцефалопатия (син.: прогрессирующая субкортикальная энцефалопатия, PML) является демиелинизирующей болезнью ЦНС, вызванной реактивацией вируса JC (JCV) у иммуннологически скомпрометированных пациентов, включая пациентов после трансплантации, со злокачественными новообразованиями системы кроветворения или СПИДом. С созданием и совершенствованием высокоактивной антиретровирусной терапии (ВААРТ) заболеваемость и распространенность прогрессирующей многоочаговой лейкоэнцефалопатии уменьшились в несколько раз. Тем не менее патология продолжает встречаться и должна рассматриваться в качестве одного из дифференциальных диагнозов при симптомах поражения ЦНС у ВИЧ инфицированных пациентов.
Недавно, о развитии прогрессирующей многоочаговой лейкоэнцефалопатии сообщалось у пациентов с аутоиммуннными болезнями, у которых проводилась иммуносупрессивная терапия. Несмотря на прекращение иммуносупрессии.
Патогенез (что происходит?) во время Прогрессирующей многоочаговой лейкоэнцефалопатии:
В полушариях большого мозга, мозговом стволе и мозжечке обнаруживают множественные очаги демиелинизации с максимальной плотностью на границе между белым и серым веществом. В основном поражаются олигодендроглиоциты.
Симптомы Прогрессирующей многоочаговой лейкоэнцефалопатии:
Течение и прогноз
Обычно трудно установить момент начала заболевания, особенно если оно развивается на фоне тяжёлого соматического недуга. Течение прогрессирующее, заканчивается летальным исходом. Может протекать остро, приводя к смерти в течение 1 мес.
Диагностика Прогрессирующей многоочаговой лейкоэнцефалопатии:
При ЭЭГ практически всегда выявляется локальное или генерализованное замедление ритма, иногда еще до появления изменений при КТ.
Спинномозговая жидкость чаще не изменена, иногда слегка повышена концентрация белка или IgG, менее чем у четверти больных выявляется цитоз, преимущественно лимфоцитарный и не превышающий 25 в мкл.
При обнаружении олигоклональных иммуноглобулинов, выраженного цитоза, наличия нейтрофилов либо эритроцитов в С спинномозговой жидкости необходимо исключить рассеянный склероз, острый геморрагический лейкоэнцефалит, СПИД-дементный синдром и ВИЧ-миелопатию, менингоэнцефалит, вызванный вирусом varicella-zoster, постинфекционный и поствакцинальный энцефаломиелит.
Окончательный диагноз ставится на основании биопсии или аутопсии. В ткани мозга можно выявить антигены вируса JC (иммуноцитохимически) и ДНК вируса (методами флюоресцентной гибридизации in situ или ПЦР), но они обнаруживаются в ткани мозга и у здоровых людей. Около 80-90% людей среднего возраста имеют антитела к вирусу JC. Он может находиться в мозге или других тканях в латентном состоянии и реактивироваться при ослаблении иммунитета. С другой стороны, возможно развитие прогрессирующей многоочаговой лейкоэнцефалопатии у лиц с ослабленным иммунитетом при первом контакте с вирусом; об этом свидетельствует тот факт, что 10-20% больных на момент установления диагноза серонегативны.
Новые данные в этом отношении могут быть получены при широком применении ПЦР.
Лечение Прогрессирующей многоочаговой лейкоэнцефалопатии:
Общее согласие относительно терапии прогрессирующей многоочаговой лейкоэнцефалопатии пока еще не достигнуто.
Появлялись отдельные сообщения о стабилизации и даже улучшении состояния при лечении цитарабином в/в или интратекально в комбинации с интерфероном а либо без него. Однако проведенное Национальным институтом здоровья кооперированное испытание не подтвердило эффективности цитарабина в сочетании с антиретровирусными препаратами (по сравнению с лечением только антиретровирусными препаратами) при прогрессирующей мультифокальной лейкоэнцефалопатии на фоне ВИЧ-инфекции.
Цидофовир, обладающей анти-JCV активностью in vitro, является наиболее эффективной терапией полиомавирусной болезни у мышей. Несколько сообщений предположили его потенциальную терапевтическую выгоду, принимая во внимание, что другие сообщения не показали клинической эффективности.
Поскольку прогрессирующая многоочаговая лейкоэнцефалопатия скорее является последствием реактивации JCV, чем острой инфекции, в идеале, лекарственное средство должно предотвращать повторную инфекцию глиальных клеток. Недавно, Atwood с коллегами продемонстрировали, что JCV использует серотониновый рецептор 5HT2A, чтобы инфицировать глиальные клетки человека. Антидепрессант миртазапин, который является антагонистом 5HT2A, способен пересекать гематоэнцефалический барьер, связывать существенное количество рецепторов 5HT2A и блокировать репликацию JCV in vitro.
К каким докторам следует обращаться если у Вас Прогрессирующая многоочаговая лейкоэнцефалопатия:
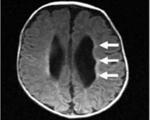
Перивентрикулярная лейкомаляция
Перивентрикулярная лейкомаляция — это гипоксически-ишемическая энцефалопатия, характеризующаяся поражением белого вещества головного мозга новорожденных. Состояние чаще возникает у недоношенных, провоцируется патологиями течения беременности и родов, неадекватной респираторной поддержкой в постнатальном периоде. Заболевание проявляется мышечной дистонией, судорожным синдромом, задержкой психомоторного развития. Для диагностики болезни назначается КТ или МРТ мозга, ЭЭГ, допплерография церебральных сосудов. Лечение лейкомаляции включает медикаменты (нейропротекторы, инфузионные растворы, антиконвульсанты), индивидуальный комплекс физиотерапии, массажа, ЛФК.
МКБ-10
Общие сведения
По разным данным, перивентрикулярная лейкомаляция (ПВЛ) встречается у 4,8-9% младенцев, причем среди больных преобладают недоношенные новорожденные (78%). Наибольшая вероятность появления болезни у детей, родившихся на сроке 27-32 недели. По данным аутопсии умерших младенцев, признаки ПВЛ регистрируются чаще — у 50-75%. Заболевание имеет большую значимость в детской неврологии, поскольку может вызывать тяжелые отдаленные последствия, считается ведущей причиной ДЦП.
Причины
Основной этиологический фактор перивентрикулярной лейкомаляции — внутриутробная гипоксия, которая выступает следствием осложнений протекания беременности, материнских факторов риска либо негативного экзогенного воздействия. Также состояние может возникать при перинатальной гипоксии, которая развивается во время родов, в первые дни жизни младенца (при синдроме дыхательных расстройств, врожденных аномалиях сердца и легких, неонатальном сепсисе).
В группе риска наибольшую по численности категорию составляют недоношенные младенцы. Зачастую лейкомаляция выявляется у детей, которое были рождены от матерей с сахарным диабетом, хронической анемией, гипертиреозом либо страдавших от преэклампсии и эклампсии. Состояние возникает при выполнении экстренного кесарева сечения, неадекватном родовспоможении (травмирующие акушерские пособия). Высокая частота лейкомаляции (до 22%) отмечается при сочетании длительного безводного периода с хориоамнионитом у матери.
Патогенез
Поражение головного мозга связано со снижением кровотока в церебральных сосудах, недостаточным поступлением кислорода и питательных ингредиентов. Перивентрикулярная область наиболее чувствительна к этим изменениям, что обусловлено особенностями кровоснабжения, несовершенством процессов ауторегуляции, нейроонтогенетическими особенностями головного мозга у младенцев.
Недоношенные намного чаще страдают лейкомаляцией, поскольку у них на фоне гипоксии не увеличивается церебральный кровоток, как это бывает у рожденных в срок младенцев. В результате этого резко уменьшается кровоток в зоне между вентрикулофугальными и вентрикулопетальными артериями, быстро формируется гиперкапния и ацидоз. Расстройства микроциркуляции проявляются стазом, тромбозом, вне- и внутриклеточным отеком белого вещества.
При перивентрикулярной лейкомаляции в конечном итоге происходит некроз отельных участков мозгового вещества, образование кист, избыточное накопление медиаторов воспаления. Поскольку на 28-32 неделях в норме происходит активная миелинизация белого вещества, а в условиях гипоксии этот процесс не может происходить, недоношенные новорожденные впоследствии имеют серьезные органические поражения ЦНС.
Формирование ПВЛ возможно не только при недостатке кислорода, но и при гипероксии — при проведении ИВЛ, оказании других видов респираторной поддержки. При избыточном поступлении кислорода повышается рН крови в мозговой ткани, что вызывает рефлекторный спазм сосудов, затруднение венозного оттока. Также кислород активизирует процессы свободнорадикального церебрального повреждения.
Симптомы
Как правило, перивентрикулярная лейкомаляция формируется антенатально или на протяжении первых часов после рождения ребенка, поэтому начальные признаки заметны уже в родильном доме, особенно если младенец рожден недоношенным. При обширном повреждении белого вещества происходят нарушения сознания по типу летаргии или комы, однако возможна обратная симптоматика — повышенная возбудимость, оживление безусловных рефлексов, судорожный синдром.
Типичным проявлением патологии являются изменения тонуса мышц. На первом месяце жизни преобладает слабость мускулатуры ног в сочетании с нормальным формированием мышц верхних конечностей. У недоношенных новорожденных часто отмечается тотальная мышечная гипотония. Такие нарушения сохраняются в среднем до 6 месяцев, после чего они сменяются спастическими явлениями — повышением тонуса мускулатуры нижних конечностей, оживлением коленных рефлексов.
Течение перивентрикулярной лейкомаляции имеет неравномерный характер: периоды обострения симптоматики сменяются «мнимым благополучием», когда ребенок развивается относительно нормально. Затем происходит задержка формирования моторных навыков, развиваются различные сенсорные нарушения, дизартрия. 66% детей, особенно недоношенные, страдают от снижения остроты зрения вплоть до полной слепоты вследствие атрофии зрительных нервов.
Осложнения
Перивентрикулярные поражения белого вещества — крайне тяжелое состояние. Недоношенные дети с ПВЛ умирают в 50% случаев еще в период новорожденности, у выживших обычно наступает инвалидность с полной дезадаптацией. Пациенты с длительно сохраняющимся судорожными приступами в 85% случаев имеют грубую задержку психомоторного развития. У перенесших ПВЛ в будущем в 1,5 раза чаще встречаются фебрильные судороги, в 27 раз чаще формируется эпилепсия.
При множественных кистах в перивентрикулярной зоне у 80-97% больных (чаще — недоношенных) возникает детский церебральный паралич (ДЦП), который сопровождается глубоким психоречевым отставанием. Развитие заболевания связано с повреждением центральной части внутренней капсулы, средне- и заднелобных сегментов белого вещества полушарий. Также лейкомаляция вызывает микроцефалию (у 42% пациентов), нейросенсорную тугоухость (у 28% больных).
Диагностика
Постановка правильного диагноза в неонатальном периоде затруднена, что объясняется полиморфностью клинической картины, отсутствием патогномоничных симптомов. При физикальном осмотре выявляется асимметрия мышечного тонуса, патологическое усиление рефлексов, на более поздних этапах — спастическая диплегия. Особую настороженность следует проявлять в отношении детей, родившихся недоношенными. В план обследования новорожденных с подозрением на ПВЛ включаются:
Лечение перивентрикулярной лейкомаляции
Терапия перивентрикулярной лейкомаляции представляет собой сложную задачу, учитывая необратимый характер повреждений белого вещества, частое сочетание гипоксически-ишемической энцефалопатии с поражениями других систем организма у недоношенных. Медикаментозное лечение подбирается на основе ведущих синдромов болезни и включает следующие группы препаратов:
Учитывая высокую частоту резидуальных неврологических явлений, рекомендовано восстановительное лечение. Чтобы улучшить двигательные способности, назначаются курсы массажа, физиотерапии, лечебной физкультуры. Для развития речевых навыков требуются коррекционные занятия у логопеда, дефектолога. Детям с поражением органов чувств нужна помощь тифлопедагога, сурдопедагога. Пациентам с ДЦП необходимы специальные ходунки, костыли, инвалидные коляски.
Прогноз и профилактика
В большинстве случаев лейкомаляция отличается неблагоприятным течением, отличается высоким уровнем смертности во время младенчества. Для выживших детей прогноз напрямую зависит от тяжести органического дефекта перивентрикулярной зоны, своевременности и полноты проведенного лечения. Профилактика ПВЛ включает рациональное ведение беременности, предупреждение родового травматизма, соблюдение протоколов при респираторной поддержке в роддоме, усиленный контроль за развитием недоношенных.
Лейкоареоз при МРТ головного мозга
Патологические процессы, затрагивающие центральную нервную систему (ЦНС), влияют на работоспособность всего организма. Морфологические изменения зачастую носят необратимый характер, снижая функциональность поврежденных отделов.
Органические поражения головного мозга часто развиваются на фоне нарушения кровоснабжения интракраниального (внутричерепного) пространства. Следствием длительной ишемии нервных тканей может стать лейкоареоз – структурные изменения белого церебрального вещества.
Признаки сосудистого поражения головного мозга
Своевременная диагностика заболевания позволяет стабилизировать работу брахиоцефальных артерий, снизить риск развития опасных осложнений. Эффективным методом исследования головного мозга является магнитно-резонансная томография.
МРТ предполагает использование силового поля, безвредного для здоровья человека. В ответ на направленный электромагнитный импульс наблюдается резонанс заряженных частиц в клетках организма. Атомы водорода в молекулах воды совершают колебательные движения, которые можно зарегистрировать при помощи чувствительных детекторов.
Информативность МР-сканирования зависит от насыщенности жидкостью изучаемых структур. Ткани головного и спинного мозга содержат большой объем воды, поэтому магнитно-резонансная томография позволяет визуализировать малейшие изменения в состоянии ЦНС.
Что такое лейкоареоз?
Причиной развития патологических процессов в области церебрального вещества служит хроническая ишемия головного мозга. При нарушении интракраниального кровообращения возникают очаги некроза нервной ткани. Структурные трансформации сопровождаются уменьшением плотности белого вещества, разрушением миелиновой оболочки нейронов. Процесс передачи нервных импульсов прекращается, снижается функциональность пораженного участка ЦНС.
В зависимости от локализации патологических явлений различают две формы лейкоареоза:
перивентрикулярный – дегенеративные процессы протекают в боковых желудочках головного мозга, возможны очаговые или диффузные изменения паренхимы;
субкортикальный – затрагивает белое вещество под корковым слоем.
Перивентрикулярный лейкоареоз как самостоятельное заболевание встречается редко, чаще данное явление служит симптомом другой патологии головного мозга. Причинами деструктивных процессов считают:
Характерным признаком перечисленных патологий является нарушение мозгового кровообращения, приводящее к демиелинизации и дегенерации церебральных структур.
Перивентрикулярный процесс на снимках МРТ
К негативным факторам, повышающим риск развития лейкоареоза, относят:
употребление наркотических средств;
заболевания сердечно-сосудистой системы;
повышенную свертываемость крови;
Перивентрикулярный процесс часто развивается вследствие отека головного мозга, сопровождающегося нарушением функционирования ликвора боковых желудочков. Крупные очаги появляются при лакунарном инфаркте или инсульте.
Симптомы лейкоареоза
Деструкция белого вещества характеризуется нарушением мозговых функций. Клинические проявления зависят от локализации и стадии патологического процесса. Степень поражения нервной ткани определяют с помощью инструментальных исследований. При проведении МРТ возможна диагностика лейкоареоза на начальном этапе.
Для клинической картины деструкции головного мозга характерны:
расстройство психо-эмоционального фона;
Первая стадия лейкоареоза сопровождается незначительными головокружениями, быстрой утомляемостью, слабостью. Пациент отмечает:
снижение концентрации внимания;
общее депрессивное состояние.
Возможны речевые нарушения, ослабление памяти. При осмотре выявляют повышение сухожильных рефлексов.
Вторая стадия протекает со значительным снижением функциональности организма. Отмечают:
нарушение координации движений;
потерю равновесия при ходьбе;
замедление психомоторных функций;
частичную или полную утрату речи;
снижение памяти и внимания.
Пациент перестает контролировать свои действия. Заметны апатия, раздражительность, депрессия. Возможны учащенное мочеиспускание, ночной диурез.
Третья стадия сопровождается усилением перечисленных признаков. Наблюдаются:
выраженные поведенческие нарушения;
падения при ходьбе;
утрата речи, памяти;
Пациент не способен к самообслуживанию.
Лейкоареоз на снимках МРТ
Деструкция белого вещества в области лобной доли характеризуется снижением интеллектуальных способностей на фоне удовлетворительной моторной функции.
МРТ головного мозга покажет лейкоареоз?
Магнитно-резонансную томографию считают одним из наиболее информативных способов исследования церебральных структур. В результате МРТ получают послойные изображения с шагом от 1 мм.
Сканирование проводят в трех взаимно перпендикулярных проекциях, при необходимости врач реконструирует 3D-модель рассматриваемой области. Томограммы визуализируют строение, форму, размеры интракраниальных структур. Трехмерная проекция помогает оценить локализацию и распространенность патологического процесса.
Изменения, характерные для лейкоареоза, хорошо видны при МРТ головного мозга. Метод позволяет оценить состояние белого вещества, показывает нарушение целостности миелинового слоя нейронов. Для визуализации кровеносной системы назначают МР-ангиографию.
Исследование церебральных сосудов проводят с использованием контрастного препарата. После внутривенной инъекции раствор заполняет кровеносное русло и межклеточное пространство. Томограммы дают возможность оценить просвет, наполненность, состояние стенок сосудов. В результате ангиографии выявляют патологии церебральных вен и артерий, последствия нарушений мозгового кровообращения (ишемию и пр.)
Сканирование применяют для дифференциальной диагностики дегенеративно-дистрофических, воспалительных, демиелинизирующих процессов, следствием которых может стать деструкция белого вещества. МРТ показывает структурные изменения тканей головного мозга, помогая выявлять пораженные очаги диаметром от 3 мм.
Магнитно-резонансная томография позволяет определить лейкоареоз на начальном этапе, уточнить патогенез заболевания и выбрать результативный метод лечения. Эффективность терапевтических и хирургических мер во многом зависит от этиологии деструктивного процесса.
Признаки легкого перивентрикулярного лейкоареоза на МРТ
Заболевание развивается на фоне увеличения количества жидкости вокруг боковых желудочков головного мозга. Расширение периваскулярной щели сопровождается образованием патологических очагов вследствие инсульта или инфаркта. Наблюдается нарушение кровотока церебральных артерий.
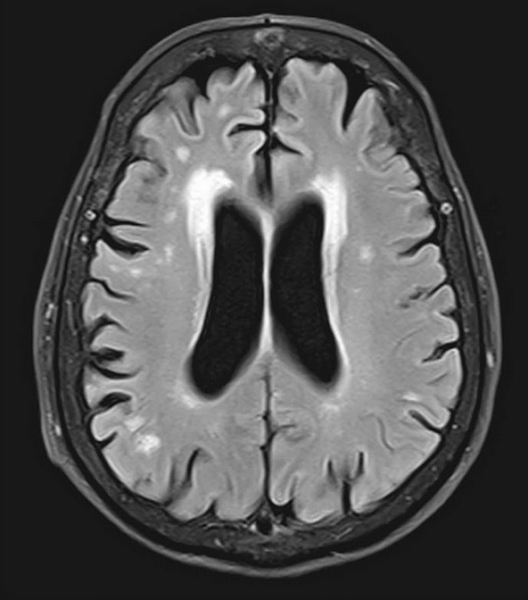
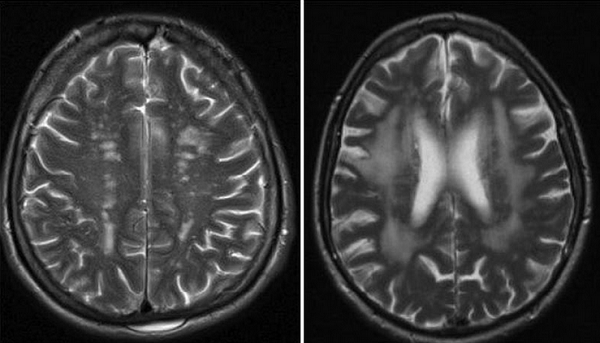
При проведении МРТ выявляют следующие признаки лейкоареоза:
вдоль перивентрикулярного пространства заметна равномерная полоса;
над полюсом бокового желудочка образуется «шапочка», соответствующая пораженному участку белого вещества.
На Т2-взвешенных изображениях патологические очаги имеют гиперинтенсивный сигнал.
Изменения в области боковых желудочков при перивентрикулярном лейкоарезе
Клиника «Магнит» в Санкт-Петербурге проводит МРТ головного мозга на закрытом томографе фирмы Siemens. Устройство генерирует силовое поле напряженностью 1,5 Тл, обеспечивая высокое качество снимков. Записаться на исследование можно по телефону +7 (812) 407-32-31 или на сайте клиники.