Диагностика и оценка риска развития преэклампсии (sFlt-1/PlGF)
Расчет соотношения концентраций растворимой фмс-подобной тирозинкиназы-1 (sFlt-1) и плацентарного фактора роста (PlGF), которое используется для оценки риска развития и степени тяжести преэклампсии.
Растворимая фмс-подобная тирозинкиназа-1 / Плацентарный фактор роста.
Solublefms-like tyrosinekinase-1 / Placental Growth Factor.
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Диагноз «преэклампсия» чаще всего ставится на основании достаточно неспецифических симптомов и признаков, главным образом – гипертензии и протеинурии. Следует, однако, отметить, что анализы на белок в моче могут быть неточными, и что осложнения преэклампсии часто возникают до того, как протеинурия становится выраженной. Кроме того, клиническая картина преэклампсии может значительно варьировать от мягкой поздней формы до тяжелой и быстро прогрессирующей ранней преэклампсии, требующей немедленного родоразрешения. Эти особенности свидетельствуют о том, что «классическое» определение преэклампсии (гипертензия более 140/90 мм рт. ст. и протеинурия 0,3 г в суточной моче) не достаточно для того, чтобы полностью охватить все компоненты этого синдрома. Учитывая это, последние рекомендации допускают диагностику преэклампсии на основании гипертензии и признаков нарушения функции органов беременной женщины, а не протеинурии. Также большое внимание уделяется новым методам диагностики и оценки риска преэклапсии. Одним из таких методов является соотношение sFlt-1/PlGF.
sFlt-1/PlGF – это соотношение концентраций в крови двух белков: растворимой fms-подобной тирозинкиназы-1 (sFlt) и плацентарного фактора роста (PlGF). Оба белка вырабатываются плацентой. PlGF обладает ангиогенными свойствами. Считается, что он необходим для нормального развития сосудистой системы плаценты. В норме концентрация PlGF постепенно возрастает к 30 неделе беременности. sFlt обладает антиангиогенными свойствами. Считается, что он связывает и нейтрализует PlGF и другие ангиогенные факторы. При нормально протекающей беременности уровень sFlt-1 остается стабильно низким вплоть до 33-36 недели беременности, после чего он незначительно возрастает вплоть до родов. При преэклампсии наблюдают обратные изменения: снижение концентрации PlGF и увеличение концентрации sFlt-1. Вероятно, изменение соотношения sFlt-1/PlGF является одной из причин развития преэклампсии. С практической точки зрения, это соотношение исследуют для оценки риска развития и степени тяжести этого заболевания.
Применение соотношения sFlt-1/PlGF у женщин с симптомами и признаками, подозрительными на преэклампсию:
В эту группу пациентов относятся женщины, у которых преэклампсия подозревается на основании таких признаков, как нарушение зрения, снижение количества тромбоцитов и других, но отсутствуют классические критерии заболевания «гипертензии плюс протеинурия».
Такие женщины должны быть госпитализированы и находиться под очень тщательным наблюдением. Очень высокое значение соотношения sFlt-1/PlGF>655 (при ранней форме) или >201(при поздней форме) ассоциировано с необходимостью родоразрешить в течение следующих 48 часов.
Повторное исследование соотношенияsFlt-1/PlGF через 2-4 дня может помочь оценить степень риска развития преэклампсии. У женщин с относительно стабильным результатом при повторном анализе вероятность быстрого ухудшения состояния пациентки маленькая. В этом случае, тест может быть повторен еще раз через 2 недели. С другой стороны, если при повторном анализе соотношениеsFlt-1/PlGF нарастает, это указывает на прогрессирование состояния.
Применение соотношения sFlt-1/PlGF у бессимптомных женщин из группы высокого риска развития преэклампсии:
В эту группу относятся женщины с факторами риска преэклампсии (ожирение, осложненный по преэклампсии семейный и личный анамнез, антифисфолипидный синдром, инсулинзависимый сахарный диабет, многоплодная беременность, отсутствие родов в анамнезе, артериальная гипертензия до беременности, болезнь почек до беременности) и женщины с нарушениями маточно-плацентарного кровотока по данным допплеровского исследования.
Исследование проводят на 24-26 неделе беременности. У пациенток с нормальным результатом соотношения sFlt-1/PlGF диагноз «преэклампсия» исключен, по крайней мере в течение 1 недели, но не на протяжении всей беременности. В этой группе может быть показано повторное исследование. Напротив, у пациенток с высоким значением sFlt-1/PlGF подозревается преэклампсия, и они должны быть направлены под более тщательное наблюдение.
Применение соотношения sFlt-1/PlGF у женщин подтвержденным диагнозом преэклампсии:
У женщин с подтвержденным диагнозом преэклампсии (гипертензии и протеинурия) соотношение sFlt-1/PlGF не добавляет никакой новой диагностической информации, но может быть использовано для оценки прогноза: более высокое значение sFlt-1/PlGF говорят о тяжелой степени заболевания.
Необходимо помнить следующие ограничения применения соотношения sFlt-1/PlGF:
Результаты анализа интерпретируют с учетом всех значимых анамнестических, клинических, других лабораторных и инструментальных данных.
Для чего используется анализ?
Когда назначается анализ?
Что означают результаты?
Референсные значения: менее 38.
Соотношение sFlt-1/PlGF:
Риск преэклампсии
Что может влиять на результат?
Кто назначает исследование?
Акушер-гинеколог, врач общей практики.
Литература
Подписка на новости
Оставьте ваш E-mail и получайте новости, а также эксклюзивные предложения от лаборатории KDLmed
Маркеры преэклампсии что это
Placental Growth Factor, PlGF.
Электрохемилюминесцентный иммуноанализ (ECLIA).
Пг/мл (пикограмм на миллилитр).
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Преэклампсия – это осложнение беременности, родов и послеродового периода, проявляющееся в виде повышения артериального давления и уровня белка в моче. По определению Международного общества по изучению гипертензии у беременных (ISSHP), о преэклампсии говорят при повышении АД более 140/90 мм рт. ст., выявленном при двух измерениях с интервалом более 4 часов, и наличии протеинурии более 0,3 г в суточной моче (или более 30 мг/ммоль при использовании протеин/креатининового соотношения), которые возникают denovo после 20-й недели беременности и полностью разрешаются к 6-й неделе послеродового периода. Преэклампсия осложняет 2-8% беременностей. Хотя тяжесть клинических проявлений сильно варьируется, прогноз обычно благоприятный при развитии легкой преэклампсии после 36-й недели. Напротив, угроза здоровью матери или плода серьезно возрастает, если преэклампсия развивается рано (до 33-й недели) или на любом сроке при наличии сопутствующих заболеваний.
Считается, что преэклампсия развивается в результате нарушения процесса дифференцировки и инвазии трофобласта на ранних сроках беременности. Это приводит к целому ряду патологических изменений в организме беременной женщины, наиболее важными из которых являются (1) стимуляция оксидативного стресса и системного воспалительного ответа и (2) дисфункция эндотелия сосудов плаценты и системная артериальная гипертензия. Выявлено несколько факторов риска преэклампсии: возраст старше 40 лет, ожирение, осложненный по преэклампсии семейный и личный анамнез, антифосфолипидный синдром, инсулинзависимый сахарный диабет, многоплодная беременность и первые роды, а также предсуществующая артериальная гипертензия и болезнь почек.
Раннее выявление преэклампсии – это основной этап лечения этого состояния. В последнее время появились новые лабораторные тесты, с помощью которых можно заподозрить преэклампсию на стадиях, предшествующих появлению белка в моче и повышению АД («пре-преэклампсия»). Одним из таких тестов является тест на плацентарный фактор роста.
Плацентарный фактор роста (ПФР) – один из белков семейства факторов роста эндотелия сосудов (VEGF, от англ. vascular endothelial growth factor). ПФР вырабатывается трофобластом и обладает выраженным ангиогенным потенциалом. Ангиогенез – ключевой процесс в развитии сосудистой системы плаценты. В норме концентрация ПФР постепенно возрастает к 30-й неделе беременности. Напротив, для преэклампсии характерна низкая концентрация ПФР. Более того, выявлено, что снижение концентрации ПФР предшествует появлению клинических признаков преэклампсии. В одном из исследований было показано, что низкий уровень ПФР на сроке 20-35 недель – это чувствительный маркер развития преэклампсии в последующие 2 недели. Считается, что изменения концентрации ПФР не являются причиной патологических изменений в плаценте, а возникают вторично в ответ на развивающуюся плацентарную недостаточность.
Некоторые факторы оказывают значительное влияние на результат исследования ПФР: срок беременности, вес и возраст матери, ее этническая принадлежность, курение, зачатие с помощью ЭКО, отсутствие родов в анамнезе и предсуществующий сахарный диабет. Поэтому, прежде чем сравнивать результат исследования с нормой, концентрацию ПФР «корректируют» с учетом этих факторов и выражают в единицах MoM (от. англ. multiple of the mean). MoM – это отношение концентрации диагностического маркера (например, ПФР) данной пациентки к средней концентрации этого маркера в соответствующей группе женщин (например, женщины на том же сроке беременности, что и испытуемая). Такой же подход используется при оценке результата альфа-фетопротеина (АФП) при диагностике аномалий плода.
Исследование на ПФР может быть дополнено анализами на другие маркеры преэклампсии, например растворимую fms-подобную тирозинкиназу-1 (sFlt-1) и ассоциированный с беременностью протеин А плазмы (PAPP-A).
Для чего используется исследование?
Когда назначается исследование?
Что такое преэклампсия (гестоз)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Дубового А. А., акушера со стажем в 13 лет.
Определение болезни. Причины заболевания
Преэклампсия — это осложнение беременности, при котором из-за увеличения проницаемости стенки сосудов развиваются нарушения в виде артериальной гипертензии, сочетающейся с потерей белка с мочой (протеинурией), отеками и полиорганной недостаточностью. [1]
Сроки развития преэклампсии
Причины преэклампсии
По сути, причина преэклампсии — беременность, именно при ней возникают патологические события, в конечном счете приводящие к клинике преэклампсии. У небеременных преэклампсии не бывает.
В научной литературе описывается более 40 теорий происхождения и патогенеза преэклампсии, а это указывает на отсутствие единых взглядов на причины ее возникновения.
Факторы риска
Установлено, что преэклампсии чаще подвержены молодые и нерожавшие женщины (от 3 до 10%). [2] У беременных с планируемыми вторыми родами риск ее возникновения составляет 1,4-4%. [3]
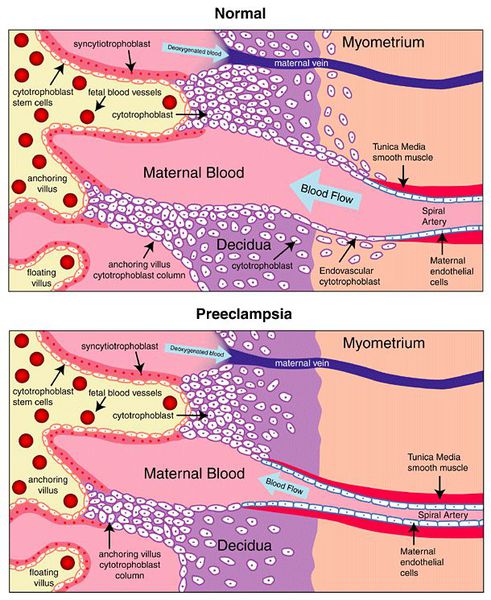
Пусковым моментом в развитии преэклампсии в современном акушерстве считается нарушение плацентации. Если беременность протекает нормально, с 7 по 16 неделю эндотелий (внутренняя оболочка сосуда), внутренний эластичный слой и мышечные пластинки участка спиральных артерий, вытесняется трофобластом и фибриносодержащим аморфным матриксом (составляющие предшественника плаценты — хориона). Из-за этого понижается давление в сосудистом русле и создается дополнительный приток крови для обеспечения потребностей плода и плаценты. Преэклампсия связана с отсутствием или неполным вторжением трофобласта в область спиральных артерий, что приводит к сохранению участков сосудистой стенки, имеющей нормальное строение. В дальнейшем воздействие на эти сосуды веществ, вызывающих вазоспазм, ведет к сужению их просвета до 40% от нормы и последующему развитию плацентарной ишемии. При нормальном течении беременности до 96% из 100-150 спиральных артерий матки претерпевают физиологические изменения, при преэклампсии же — всего 10%. Исследования подтверждают, что наружный диаметр спиральных артерий при патологической плацентации вдвое меньше, чем должно быть в норме. [4] [5]
Симптомы преэклампсии
Раньше в отечественном акушерстве то, что сейчас называется термином «преэклампсия», называлось «поздний гестоз», а непосредственно под преэклампсией при беременности понимали тяжелую степень позднего гестоза. Сегодня в большинстве регионов России перешли на классификацию, принятую ВОЗ. Ранее говорили о так называемом ОПГ-гестозе (отеки, протеинурия и гипертензия).
1. Артериальная гипертензия
Преэклампсия характеризуется систолическим АД>140 мм рт. ст. и/или диастолическим АД>90 мм рт. ст., измеряется дважды с интервалом 6 часов. По меньшей мере два повышенных значения АД являются основанием для диагностики АГ во время беременности. Если есть сомнения, рекомендуется провести суточное мониторирование АД (СМАД).
2. Протеинурия
Чтобы диагностировать протеинурию, необходимо выявить количественное определение белка в суточной порции (в норме при беременности — 0,3 г/л). Клинически значимая протеинурия во время беременности определена как наличие белка в моче ≥ 0,3 г/л в суточной пробе (24 часа) либо в двух пробах, взятых с интервалом в 6 часов; при использовании тест-полоски (белок в моче) — показатель ≥ «1+».
Умеренная протеинурия — это уровень белка > 0,3 г/24 часа или > 0,3 г/л, определяемый в двух порциях мочи, взятой с интервалом в 6 часов, или значение «1+» по тест-полоске.
Выраженная протеинурия — это уровень белка > 5 г/24 часа или > 3 г/л в двух порциях мочи, взятой с интервалом в 6 часов, или значение «3+» по тест-полоске.
Чтобы оценить истинный уровень протеинурии, нужно исключить наличие инфекции мочевыделительной системы, а патологическая протеинурия у беременных является первым признаком полиорганных поражений. [1]
3. Отечный синдром
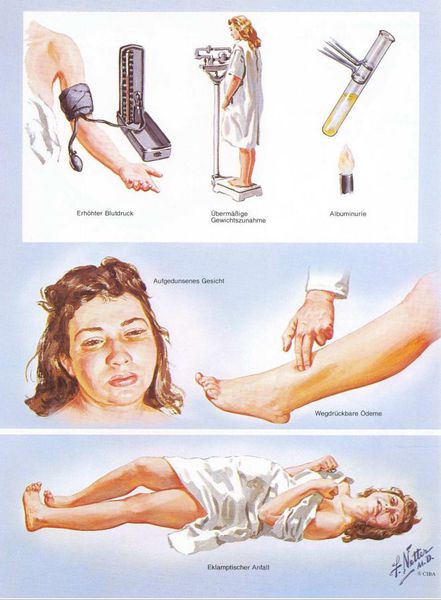
Триада признаков преэклампсии, описанная Вильгельмом Цангемейстером в 1912 г. (ОПГ-гестоз), сегодня встречается лишь в 25-39%. Наличие отеков в современном акушерстве не считается диагностическим критерием преэклампсии, но важно, когда нужно оценить степень ее тяжести. Когда беременность протекает нормально, отеки встречаются в 50-80% случаев, амбулаторное ведение безопасно для лёгкого отечного симптома. Однако генерализованные, рецидивирующие отеки зачастую являются признаком сочетанной преэклампсии (нередко на фоне патологии почек). [6]
Американский врач-хирург и художник-иллюстратор Фрэнк Генри Неттер, которого справедливо прозвали «Микеланджело медицины», очень наглядно изобразил основные проявления преэклампсии. [7]
Патогенез преэклампсии
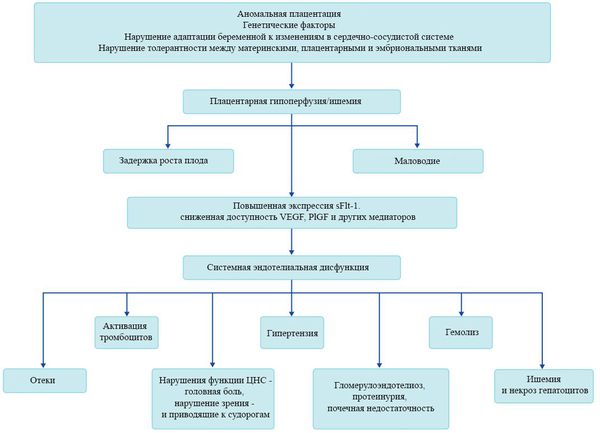
В ответ на ишемию при нарушении имплантации (см. рисунок) начинают активно вырабатываться плацентарные, в том числе антиангиогенные факторы и медиаторы воспаления, повреждающие клетки эндотелия. [8] Когда компенсаторные механизмы кровообращения на исходе, плацента с помощью прессорных агентов активно «подстраивает» под себя артериальное давление беременной, при этом временно усиливая кровообращение. В итоге этого конфликта возникает дисфункция эндотелия. [9]
При развитии плацентарной ишемии активируется большое количество механизмов, ведущих к повреждению эндотелиальных клеток во всем организме, если процесс генерализуется. В результате системной эндотелиальной дисфункции нарушаются функции жизненно важных органов и систем, и в итоге мы имеем клинические проявления преэклампсии.
Нарушение плацентарной перфузии из-за патологии плаценты и спазма сосудов повышает риск гибели плода, задержки внутриутробного развития, рождения детей малых для срока и перинатальной смертности. [10] Кроме того, состояние матери нередко становится причиной прерывания беременности на раннем этапе — именно поэтому дети, родившиеся от матерей с преэклампсией, имеют более высокий показатель заболеваемости респираторным дистресс-синдромом. Отслойка плаценты очень распространена среди больных преэклампсией и связана с высокой перинатальной смертностью.
Классификация и стадии развития преэклампсии
В Международной классификации болезней (МКБ-10) преэкслампсия кодируется как О14. Выделяют умеренную и тяжёлую форму заболевания.
Эклампсия – состояние, при котором в клинических проявлениях преэклампсии преобладают поражения головного мозга, сопровождаемые судорожным синдромом, который не может быть объяснен другими причинами, и следующим после него периодом разрешения. Эклампсия может развиться на фоне преэклампсии любой степени тяжести, а не является проявлением максимальной тяжести преэклампсии.
Осложнения преэклампсии
Основные осложнения при преэклампсии у беременных:
Диагностика преэклампсии
Диагностика преэклампсии заключается прежде всего в установлении наличия указанных выше симптомов. В ряде случаев представляет сложность дифференциальная диагностика преэклампсии и существовавшая до беременности артериальная гипертензия.
Дифференциальная диагностика гипертензивных осложнений беременности
| Клинические признаки | Хроническая гипертензия | Преэклампсия |
|---|---|---|
| Возраст | часто возрастные (более 30 лет) | часто молодые ( [1] |
2. Антигипертензивная терапия
Цель лечения — поддерживать АД в пределах, которые сохраняют на нормальном уровне показатели маточно-плодового кровотока и снижают риск развития эклампсии.
Антигипертензивную терапию следует проводить, постоянно контролируя состояние плода, потому что снижение плацентарного кровотока провоцирует у него прогрессирование функциональных нарушений. Критерием начала антигипертензивной терапии является АД ≥ 140/90 мм рт. ст.
Основные лекарственные средства, используемые для лечения АГ в период беременности:
3. Профилактика и лечение судорог
Для профилактики и лечения судорог основным препаратом является сульфат магния (MgSO4). Показанием для противосудорожной профилактики является тяжелая преэклампсия, если есть риск развития эклампсии. При умеренной преэклампсии — в отдельных случаях решает консилиум, потому что при этом повышается риск кесарева сечения и есть ряд побочных эффектов. Механизм действия магния объясняется нарушением тока ионов кальция в гладкомышечную клетку.
Кроме того, необходимо контролировать водный баланс, уделять внимание лечению олигурии и отека легких при их возникновении, нормализации функции ЦНС, реологических свойств крови, улучшение плодового кровотока.
Прогноз. Профилактика
Сегодня до 64% смертей от преэклампсии предотвратимы.
Основные факторы качественной и своевременной помощи:
К сожалению, сегодня нет достаточно чувствительных и специфичных тестов, которые бы обеспечивали раннюю диагностику/выявление риска развития преэклампсии.
Факторы риска развития преэклампсии: [2]
1. антифосфолипидный синдром;
2. заболевания почек;
3. преэклампсия в анамнезе;
4. предстоящие первые роды;
5. хроническая гипертензия;
7. жительницы высокогорных районов;
8. многоплодная беременность;
9. сердечно-сосудистые заболевания в семье (инсульты/инфаркты у близких родственников);
10. системные заболевания;
12. преэклампсия в анамнезе у матери пациентки;
13. возраст 40 лет и старше;
14. прибавка массы тела при беременности свыше 16 кг.
Установлено, что для преэклампсии характерен недостаточный ангиогенез — процесс образования сосудов. [11] В нем участвуют около 20 стимулирующих и 30 ингибирующих ангиогенез факторов, их список постоянно пополняется. Наиболее изучен и представляют особый интерес с точки зрения исследования патогенеза преэклампсии два проангиогенных фактора: сосудисто-эндотелиальный фактор роста (VEGF) и плацентарный фактор роста (PlGF), антиангиогенный фактор — Fms-подобная тирозинкиназа (Flt-1) и ее растворимая форма (sFlt-1).
Повышение содержания этого sFlt-1 с одновременным снижением VEGF и PlGF начинается за 5-6 недель до клинических проявлений преэклампсии. [12] Данный факт позволяет прогнозировать развитие преэклампсии у женщин из группы риска в первом триместре беременности. Однако другими исследователями отмечено, что несмотря на высокую чувствительность теста (96%), изолированное определение sFlt-1 не может быть использовано при диагностике преэклампсии из-за низкой специфичности. Таким образом, обнаружение изменений в соотношении уровня PlGF и sFlt-1 в течение беременности может сыграть важную вспомогательную роль для подтверждения диагноза преэклампсии.
Сегодня существуют коммерческие наборы, которые позволяют проводить иммуноферментное исследование, чтобы определить вероятность развития преэклампсии, на основании определения содержания PlGF (DELFIA Xpress PlGF kit, PerkinElmer; США), предложены скрининговые тесты для прогнозирования и ранней диагностики преэклампсии, основанные на определении соотношения sFlt-1 и PlGF (Elecsys sFlt-1/PlGF, Roche, Швейцария).
Из-за нарушения инвазии трофобласта увеличивается сосудистое сопротивление в маточной артерии и снижается перфузия плаценты. Повышение пульсационного индекса и систолодиастолического отношения в маточной артерии в 11-13 недель беременности является лучшим предиктором преэклампсии, и его настоятельно рекомендуется использовать в клинической практике у беременных из группы риска.
Профилактика преэклампсии
Из-за того, что исчерпывающая информация об этиологии и патофизиологии преэклампсии отсутствует, разработка эффективных профилактических мер представляет определенные трудности.
Сегодня доказан прием только 2 групп препаратов для профилактики преэклампсии: [1] [2]
• Аспирин в низких дозах (75 мг в день), начиная с 12 недель до родоразрешения. При этом необходимо брать письменное информированное согласие пациентки, поскольку согласно инструкции по применению, прием аспирина противопоказан в первом триместре.
• Беременным с низким потреблением кальция (
Циркулирующие прогностические биомаркеры преэклампсии
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Патофизиология преэклампсии остается малоизученной. Тем не менее известно, что продуцируемые плацентой в результате окислительного стресса и вызывающие чрезмерный системный воспалительный ответ факторы [1] приводят к дисфункции эндотелия женщины, оказывая влияние на клинические особенности преэклампсии [9]. Неправильная плацентация с аномальным вторжением цитотрофобласта и неполным ремоделированием спиральных артерий, снабжающих плаценту, предположительно вызывает изменения циркуляции и последующий окислительный стресс в плаценте, а также связанный с ним выброс факторов эндотелиальной дисфункции в систему кровообращения [9, 10]. По результатам изучения патогенеза преэклампсии были выявлены новые биомаркеры (вещества, используемые в качестве индикаторов биологического состояния; данное понятие применяется для характеристики маркеров, пригодных для прогнозирования биологического состояния, например преэклампсии [11]) для раннего обнаружения и предотвращения данной патологии. Усилия ученых сосредоточены на выявлении плацентарных белков (РР), коррелирующих с патофизиологическими изменениями, наблюдаемыми при раннем дефективном вторжении трофобластов [4].
Что касается преэклампсии, то принадлежность к негроидной расе является таким же значительным фактором, если даже не большим, чем возраст первородящей или присутствие болезни в семейном анамнезе. Материнские и отцовские генотипы вносят значимый вклад в развитие преэклампсии [3]. Удивительно, но курение уменьшает риск возникновения преэклампсии на 50% в зависимости от дозы, если продолжать его в течение всей беременности. Точный механизм этого не известен, но есть доказательства, что табачный дым может влиять на кровеносные сосуды и эндотелиальную функцию, снижая проявления преэклампсии. Тем не менее ученые не выступают в поддержку курения других его вредоносных влияний на мать и плод [12].
В настоящее время абсолютно эффективного метода лечения или профилактики преэклампсии нет. Роды и последующее удаление плаценты — своеобразное «лечение», часто с рождением недоношенного ребенка. Поэтому конечная цель изучения биомаркеров преэклампсии — пополнение знаний о патофизиологии данного состояния для определения новых терапевтических мишеней и, соответственно, улучшения состояния здоровья матери и плода. Важно, чтобы в распоряжении врача было несколько биомаркеров, способных помочь в принятии решения о безопасности продления беременности при раннем начале развития преэклампсии с целью уменьшения осложнений, связанных с недоношенностью. В глобальной перспективе тест должен быть предпочтительно простым и быстрым для выполнения, дешевым и по возможности неинвазивным. Он должен обладать 100% чувствительностью и 100% специфичностью [13]. В настоящее время такого теста не существует. Низкая чувствительность теста будет иметь более серьезные последствия, чем низкая специфичность, поскольку печальных последствий от ложноотрицательных результатов гораздо больше, чем от ложноположительных в связи с потенциальной высокой смертностью и заболеваемостью матери и ребенка, связанных с преэклампсией.
В последние десятилетия было выявлено, что дисбаланс проангиогенных и антиангиогенных факторов, вовлеченных в процесс формирования плаценты и имплантации, вызывает эндотелиальную дисфункцию во время беременности. Эти факторы могут оказаться хорошими кандидатами на право быть биомаркерами преэклампсии. Проангиогенные факторы включают сосудистые эндотелиальный фактор роста (VEGF) и фактор роста плаценты (PIGF), антиангиогенные представлены растворимым рецептором тирозинкиназы 1 (sFlt1) и эндоглином (sEng). Еще до развития клинических проявлений преэклампсии отмечаются значительные изменения уровней PIGF, sFlt1 и sEng [3, 14–16].
Ассоциированный с беременностью
Ассоциированный с беременностью () — высокогликозилированный белок, который вырабатывается в большом количестве в развивающемся трофобласте. модулирует активность инсулиноподобных факторов роста путем расщепления белков, связывающих такие факторы. Предполагается, что играет важную роль в имплантации, а в повседневной практике используется в качестве биомаркера синдрома Дауна. Повышение уровня в материнской сыворотке при клинической преэклампсии было установлено исследователями еще 40 лет назад, а более поздние исследования выявили данный показатель в III триместре ( нед.) — еще до развития преэклампсии [1]. Кроме того, может быть маркером задержки внутриутробного развития плода (ЗВУР) [17]. В сочетании с допплеровским индексом резистентности маточных артерий он повышает уровень прогнозирования преэклампсии [18], но чувствительность этого теста остается слишком низкой, чтобы быть полезной в качестве скринингового биомаркера преэклампсии.
Ингибин, А и активин A
Ингибин, А и активин, А являются гликопротеидными гормонами из β-группы трансформирующих факторов роста. Плацента — это основной источник данных циркулирующих белков, их концентрация увеличивается в III триместре при неосложненных беременностях. Часто встречается одновременное увеличение концентрации активина, А и ингибина, А, возможно, того, что активин, А стимулирует секрецию хорионического гонадотропина человека (ХГЧ), в то время как ХГЧ, в свою очередь, стимулирует продукцию ингибина, А [1]. По сравнению с группой с нормальным АД у женщин с преэклампсией повышается концентрация ингибина, А и/или активина, А в материнской сыворотке [19–22].
Чем выше показатели α-фетопротеина, ХГЧ и ингибина, тем больше вероятность развития преэклампсии, причем раннего начала заболевания. Данные методы обследования могут способствовать выявлению пациенток с более высоким риском неблагоприятных исходов, требующих тщательного мониторирования. Одним из возможных объяснений полученных данных может быть то убеждение, что раннее и позднее начало преэклампсии могут быть разными, отличающимися заболеваниями со сложным взаимодействием между плацентарными факторами, материнским организмом и беременностью как сосудистой и иммунологической адаптацией, приводящей к различным синдромам. Это подтверждается растущим числом литературных данных [4].
— это еще один маркер, прогнозирующий развитие не только преэклампсии, но и ЗВУР. является членом семейства галектинов, представляет собой димерный белок, в большом количестве секретируемый в плаценте. Роль его неясна, но было высказано предположение, что может быть вовлечен в процесс имплантации плаценты и ремоделирования материнских сосудов [23]. У пациенток с преэклампсией после родов в плаценте отмечено снижение выброса цитоплазматического белка трофобласта по сравнению с женщинами с неосложненной беременностью [24]. Однако в сыворотке крови пациенток при развитии преэклампсии концентрация увеличивается, несмотря на уменьшение его экскреции плацентой. Возможно, сброс в материнскую кровь происходит расширенной синцитиотрофобластической мембраны [24].
Наличие низкой концентрации в материнской сыворотке в I триместре позволяет прогнозировать преэклампсию [25] у женщин как с умеренным и низким уровнем риска [26], так и с высоким риском [27]. В целом низкий уровень в I триместре может быть прогностическим маркером раннего начала и тяжелого течения преэклампсии [27]. Как правило, при оценке тяжести преэклампсии применяется с другими маркерами. Из них и допплерометрия маточных артерий кажутся одними из самых многообещающих в отношении прогнозирования.
Ангиогенные факторы
Ангиогенный белок sFlt1, также называемый « фактора роста эндотелия сосудов» (), был предложен в 2003 г. в качестве возможного повреждающего эндотелий фактора при преэклампсии [1]. Повышение уровня sFlt1 во II триместре прогнозирует развитие преэклампсии [29, 30], он является лучшим предиктором ранней преэклампсии. Низкая концентрация sFlt1 в I триместре, прогнозирующая раннее начало преэклампсии, была подтверждена в исследованиях [31] и O. Erez [32] с учетом индекса массы тела (ИМТ), возраста и отсутствия родов в анамнезе.
Повышенный уровень sEng обнаруживается примерно за 2–3 мес. до появления клинических признаков преэклампсии [14]. Тем не менее не доказано, что в I триместре sEng способен прогнозировать преэклампсию [32].
Обнаружено, что у женщин с преэклампсией выявляется больше последовательных изменений уровней sFlt1 и sEng в I и II триместрах, несмотря на одинаковые уровни вначале [15]. Эти результаты были подтверждены длительными исследованиями, включавшими более 1600 пациенток, в которых было выявлено, что хотя индивидуальные уровни sEng, PIGF и sFlt1 не прогнозируют преэклампсию достаточно точно, соотношение PIGF/sEng обладает 100% чувствительностью, а специфичность варьирует от 98 до 99% [31].
еt al. показали, что уровни sFlt1 повысились за 5–6 нед. до клинических проявлений преэклампсии, с другой стороны, уровни sEng выросли за 2–3 мес. [14]. Интересно отметить, что повышение уровня sEng связано либо с тяжелой формой преэклампсии, либо с эклампсией [33]. Уровни PIGF и sFlt1 одновременно изменяются при преэклампсии, и поэтому соотношение sFlt1/PIGF считается лучшим прогностическим фактором развития преэклампсии, чем другие факторы [34].
В большинстве исследований было показано, что наличие низкой концентрации PIGF во II триместре позволяет прогнозировать позднее развитие преэклампсии [35–37], но в других работах эта связь не была подтверждена [38].
Измерение концентрации PIGF в моче как скринингового маркера для определения группы риска, возможно, будет еще одним показателем, поскольку его уровень снижается во II триместре беременности у женщин с поздним развитием преэклампсии [39].
Эмбриональные эритробласты и ДНК в материнской крови
Еще до развития клинических проявлений преэклампсии выявляется увеличение количества фетальных эритробластов в материнской крови [1]. В 1999 г. et al. отмечено повышение уровня фетальной ДНК в материнской крови при преэклампсии [40]. Позже было предложено использование фетальной ДНК вне хромосомы Y для оценки риска развития преэклампсии у женщин, имеющих плод женского пола [1]. Неудобство метода заключается в его сложности и высокой стоимости.
Подоциты
Отмечается растущий интерес к использованию подоцитов как возможных прогностических маркеров преэклампсии. Когда одну аллель VEGF удаляли в подоцитах у мышей, в почках развивались патологические процессы, характерные для преэклампсии [3]. et al., продолжив изучение на людях, продемонстрировали, что при биопсии почек у пациенток с преэклампсией экспрессия специфического для подоцитов белка снижена [41]. Кроме того, они могут быть выделены в моче у таких пациенток [42]. Описано наличие подоцитурии у 15 женщин с преэклампсией или (гемолиз, повышение уровня ферментов печени, тромбоцитопения) и 16 пациенток контрольной группы. Авторы культивировали подоциты в моче, определяя их с использованием подоцина, нефрина, подокалексина и синаптоподина как белков. Чувствительность и специфичность клеток достигали 100%, а вот чувствительность и специфичность других белков были низкими [42]. Впоследствии К. Aita et al. обнаружили подоцитурию у пациенток с преэклампсией на нед. беременности и на день после родов, но не на мес. после родов. По мнению авторов, этот срок предполагает полное восстановление почек после повреждений, вызванных преэклампсией. Интересно отметить, что даже у 9 из 45 нормотензивных женщин на день после родов выявлена подоцитурия, что означает либо то, что она не является специфической для преэклампсии, либо то, что она может определяться и у здоровых женщин [43, 44]. Несмотря на первоначальный энтузиазм по поводу использования подоцитов как возможных прогностических маркеров, этот метод остается слабым диагностическим критерием, учитывая трудную изоляцию, частую контаминацию точного определения верного подоцита.
Существует нехватка метаанализов оценки прогнозирующих биомаркеров преэклампсии, исследования отдельных биомаркеров сложно сравнивать, гестационный возраст на момент проведения проб и другие параметры часто меняются. Несколько авторов показали, что комбинация маркеров повышает точность тестов в прогнозировании преэклампсии. Например, сочетание найденной патологии маточных артерий при допплеровском исследовании и изменений циркулирующих ангиогенных факторов во II триместре показали лучшую прогностическую ценность в отношении преэклампсии, чем отдельный допплеровский тест или только ангиогенные факторы [45, 46].
F. Crispi et al. предложили тесты с 90% чувствительностью и 95% специфичностью для идентификации раннего начала преэклампсии или синдрома ЗВУР путем объединения исследования во II триместре уровня PIGF в сыворотке и среднего пульсационного индекса маточной артерии. В то же время чувствительность этого теста в отношении позднего начала преэклампсии или ЗВУР была очень низкой (ниже 11%) [47]. Исследование во II триместре уровней sFlt1 и PIGF и нарушения маточной перфузии при допплеровской велосиметрии повысило точность прогнозирования преэклампсии [46]. B подгруппе беременных с патологическими показателями при допплеровском исследовании артерий матки во II триместре (23 нед.) уровень sFlt1 был повышенным. Уровень PIGF у женщин с развивающейся преэклампсией или ЗВУР (без АГ) был ниже, чем у женщин с неосложненной беременностью. Данные показатели были особенно выраженными у женщин с показаниями к родоразрешению до 34 нед. [46]. Есть мнение, что определение уровней sFlt1 и sEng во II триместре может предсказать раннее начало преэклампсии у женщин с аномальными результатами допплерометрии маточных артерий со 100% чувствительностью и 93% специфичностью [48]. R. Akolekar et al. выявили, что определение уровня PIGF в сыворотке у женщин на нед. беременности и пульсационного индекса маточных артерий дает уровень прогнозирования преэклампсии в 90% (с ложноположительным результатом 10%) [49].
Скрининговое исследование плацент было использовано в качестве средства для поиска новых биомаркеров преэклампсии. За начальным скринингом экспрессии плацентарных генов проводилось исследование концентрации белка в крови матери для выявления дизрегуляции генов [50]. Новые технологии, которые могут помочь в поиске новых скрининговых биомаркеров, включают безгелевые протеомиксы с методом для определения глобальных изменений концентрации белка в плазме [51]. Кроме того, другие исследования обнаружили, что ранняя и поздняя преэклампсия возникают при наличии различных гемодинамических состояний. Поздняя преэклампсия наблюдается чаще у пациенток с высоким ИМТ, высоким сердечным выбросом и низким общим сосудистым сопротивлением. При ранних формах имеются меньший ИМТ, повышенное сосудистое сопротивление маточной артерии [52].
Многообещающим исследованием с целью прогнозирования преэклампсии может быть определение биомаркеров в моче. Однако молекулы sFlt1 слишком большие (
100 kDа), чтобы быть отфильтрованными в моче при отсутствии повреждений почек, в то время как более мелкие молекулы PIGF и VEGF (30 и 45 kDа) могут пройти барьер клубочковой фильтрации [39]. Поскольку VEGF выделяется локально, он не будет, скорее всего, отражать циркулирующий ангиогенный статус. Несколько исследований показали более низкие концентрации PIGF в моче женщин с установленной преэклампсией, а также низкие концентрации PIGF во II триместре как предвестники преэклампсии [39, 53, 54].
Популяция пациенток, у которых выполняется забор образцов для биологического тестирования маркеров, имеет решающее значение для интерпретации результатов. Несколько биобанков были использованы или планируется использовать для изучения биомаркеров прогнозирования преэклампсии. Большую роль играют также правильный забор и условия хранения биологических образцов.
В заключение следует сказать, что маркеры, определяемые в сыворотке материнской крови, сильнее всего связаны с ранними и более тяжелыми вариантами преэклампсии. В то же время они не имеют достаточной чувствительности или специфичности, чтобы самостоятельно быть клинически полезными.
Профилактических мер для предупреждения преэклампсии не хватает, хотя есть некоторые данные, что использование таких препаратов, как ацетилсалициловая кислота или низкомолекулярный гепарин может помочь снизить вероятность развития данной патологии. Например, использование низких доз ацетилсалициловой кислоты у женщин с высоким ХГЧ и аномальными показателями при допплеровском исследовании маточных артерий позволило увеличить вес младенца при рождении и снизить заболеваемость гестационной АГ [55].
Тем не менее есть надежда, что с помощью более глубокого изучения природы ранней и поздней преэклампсии возможно создание лучших прогностических моделей, которые касаются различных проявлений этого болезненного состояния, и выявление женщин с высоким риском для проспективного клинического испытания и одновременной разработки лучших профилактических стратегий. В настоящее время, несмотря на сотни изученных маркеров, ни один из них не соответствует определению ВОЗ по отбору биомаркеров, которые либо прогнозируют, либо диагностируют преэклампсию. За основу берутся традиционные факторы риска, согласующиеся с клиническими параметрами и лабораторными и ультразвуковыми исследованиями. До сих пор не разработана и эффективная терапия, хотя контрольные исследования эффективного и в конечном счете пролонгирующего беременность удаления sFlt1 экстракорпоральным аферезом у пациенток с тяжелой формой преэклампсии представляются весьма перспективными [56].
Применение новых технологий, разработанных для открытия биомаркеров, зачастую ограничено их высокой стоимостью. Из этого следует, что предстоит еще многое сделать, чтобы снизить частоту развития и тяжесть преэклампсии [3].
Только для зарегистрированных пользователей