Лимфогистиоцитоз гемофагоцитарный что это
Гемофагоцитарный лимфогистиоцитоз у детей. Клинические рекомендации.
Гемофагоцитарный лимфогистиоцитоз у детей
Оглавление
Ключевые слова
Трансплантация гемопоэтических стволовых клеток
Всего 10-15 ключевых слов
Список сокращений
ГЛГ – гемофагоцитарный лимфогистиоцитоз
ВГЛГ – вторичный гемофагоцитарный лимфогистиоцитоз
ТГСК – трансплантация гемопоэтических стволовых клеток
НК – натуральные киллеры
АЛТ- аланиновая аминотрансфераза
АСТ – аспарагиновая аминотрансфераза
КТ – компьютерная томография
МРТ – магнитно-резонансная томография
УЗИ – ультразвуковое исследование
ВИЧ – вирус иммунодефицита человека
ПЦР – полимеразная цепная реакция
ЭБВ – вирус Эпштейн-Барр
Термины и определения
Гемофагоцитарный лимфогистиоцитоз – врожденное или приобретенное заболевание, проявляющееся лихорадкой, спленомегалией, панцитопенией, коагулопатией и неврологическим дефицитом вследствие системного воспалительного ответа и повреждения органов активированными макрофагами и цитотоксическими Т лимфоцитами.
Гемофагоцитоз – феномен фагоцитоза форменных элементов крови макрофагами, выявляемый при цитоморфологическом или гистологическом исследовании образцов тканей или биологических жидкостей
Первичный гемофагоцитарный лимфогистиоцитоз (ПГЛГ) – форма ГЛГ, обусловленная наследуемым генетическим дефектом механизмов клеточной цитотоксичности и иных механизмов негативной регуляции иммунного ответа
Вторичный гемофагоцитарный лимфогистиоцитоз (ВГЛГ) – форма ГЛГ, обусловленная нарушением регуляции иммунного ответа в контексте верифицированного онкологического, аутоиммунного или инфекцинонного процесса, и не имеющая в основе наследуемого генетического дефекта
1. Краткая информация
1.1 Определение
Гемофагоцитарный лимфогистиоцитоз – заболевание, обусловленное дефицитом негативной регуляции иммунного ответа, сопровождающееся неконтролируемой активацией цитотоксических Т-лимфоцитов и макрофагов, аккумуляцией их в пораженных органах и развитием системного воспалительного ответа.
1.2 Этиология и патогенез
Вторичный гемофагоцитарный синдром развивается вследствие нарушения регуляции иммунного ответа, развивающегося в контексте аутоиммунных, онкологических и инфекционных заболеваний. Независимо от пусковых механизмов, общим патологическим механизмом первичного и вторичного гемофагоцитарного синдрома является гиперпродукция провоспалительных цитокинов, активация моноцитов/макрофагов и мультиорганное воспалительное повреждение [1]
1.3 Эпидемиология
Данные о заболеваемости и распространенности ПГЛГ в России ограничены, экстраполяция международных данных дает заболеваемость 1 на 106 детского населения в год. Достоверных оценок заболеваемости и распространенности ВГЛГ нет.
1.4 Кодирование по МКБ-10
D76.1 – гемофагоцитарный лимфогистиоцитоз
D76.2 – гемофагоцитарный синдром, связанный с инфекцией
D76.3 – другие гистиоцитозные синдромы
1.5 Классификация
Гемофагоцитарный лимфогистиоцитоз отнесен к группе “H” в современной классификации гистиоцитозов. Выделяют первичные формы гемофагоцитарного лимфогистиоцитоза, обусловленные известным генетическим дефектом, и вторичные, не связанные с наследуемым генетическим дефектом. Полная классификация гемофагоцитарного лимфогистиоцитоза в соответствии с приведена ниже [2].
Первичный гемофагоцитарный лимфогистиоцитоз: наследственные заболевания, ведущие к развитию ГЛГ
ГЛГ, ассоциированный с дефектами цитотоксичности лимфоцитов
Синдром Грисселли типа (RAB27A)
Синдром Чедиак-Хигаши (LYST)
ГЛГ, ассоциированный с аномалиями активации инфламмасомы
ГЛГ, ассоциированный с наследственными болезнями, влияющими на воспаление
Лизинурия/интолерантность к белку (SLC7A7)
Семейные формы ГЛГ с неустановленным генетическим дефектом
Вторичный гемофагоцитарный лоимфогистиоцитоз
Ассоциированный с инфекцией
ГЛГ, ассоциированный с бактериальной инфекцией
ГЛГ, ассоциированный с грибковой инфекцией
ГЛГ, ассоциированный с паразитарной инфекцией
Ассоциированный со злокачественными новообразованиями
ГЛГ, ассоциированный с химиотерапией (не связанный с первичной презентацией опухоли)
Ассоциированный с ревматологическими заболеваниями
ГЛГ, ассоциированный с трансплантацией
ГЛГ, ассоциированный с иатрогенной активацией иммунной системы
ГЛГ, ассоциированный с иатрогенной иммуносупрессией
2. Диагностика
2.1 Жалобы и анамнез
Увеличение объёма живота
Ребенок раннего возраста
Беременность и роды без патологии
Смерть сиблингов со сходной клинической презентацией
Указания на Х-сцепленную патологию в семейном анамнезе
2.2 Физикальное обследование
Геморрагии на слизистых
2.3 Лабораторная диагностика
Пациентам с гемофагоцитарным лимфогистиоцитозом рекомендовано выполнение:
Автоматического анализа крови с лейкоцитарной формулой
Биохимического анализа крови
Исследования спинномозговой жидкости
Иммунофенотипирование лимфоцитов периферической крови
Определение экспрессии белков перфорин, SAP и XIAP в НК-клетках и Т-лимфоцитах
Исследования концентрации иммуноглобулинов сыворотки
Детекции вирусных геномов методом ПЦР в крови (цитомегаловирус, вирус Эпштейн-Барр, ВИЧ, герпес симплекс 1 и 2 типа, парвовирус В19)
Исследования концентрации растворимого sCD25;
Тканевого типирования пациента и потенциальных доноров
Микробиологического исследования крови (гемокультура)
Микробиологического исследования ликвора
Молекулярно-генетического исследования – прямое секвенирование генов PRF1, UNC13D, STX11, STXBP, SH2D1A, RAB27
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
2.4 Инструментальная диагностика
Пациентам с гемофагоцитарным лимфогистиоцитозом рекомендовано проведение:
2.4.1 МРТ головного мозга Т1, Т2, FLAIR, c контрастированием гадолинием
2.4.2 УЗИ брюшной полости
2.4.3 Рентгенографии грудной клетки
2.4.4 КТ легких
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
2.5 Иная диагностика
Пациентам с гемофагоцитарным лимфогистиоцитозом рекомендовано проведение:
2.5.1 Биопсии лимфатического узла с морфологическим и иммуногистохимическим исследованием
2.5.2 Биопсии кожи с морфологическим и иммуногистохимическим исследованием
2.5.3 Биопсии печени с морфологическим и иммуногистохимическим исследованием
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Комментарии: Диагностика ГЛГ включает два этапа: 1) установление диагноза ГЛГ и 2) верификация природы ГЛГ (первичный или вторичный).
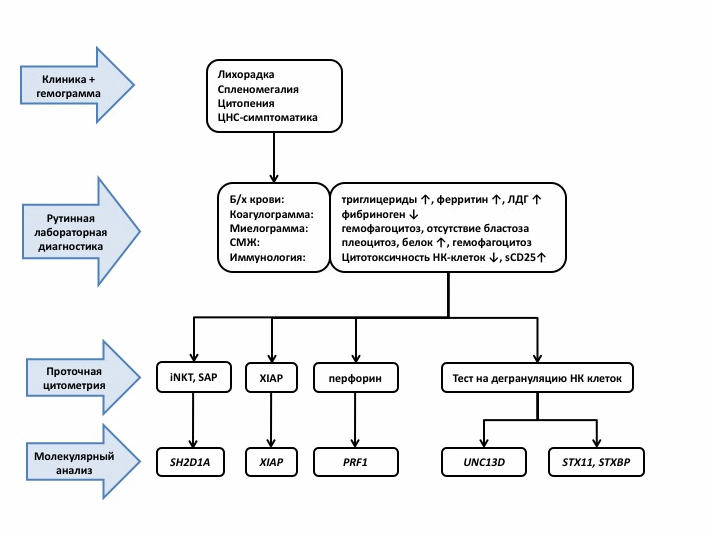
На первом этапе диагноз ГЛГ устанавливается на основании набора диагностических критериев:
лихорадка > 38оС > 7 дней
спленомегалия > 3 см из-под реберной дуги
Снижение цитотоксичности НК?клеток (или )
Гемофагоцитоз (в костном мозге, ликворе, лимфатических узлах, ином субстрате)
Клинический диагноз ГЛГ устанавливается при выполнении 5 из 8 критериев и отсутствии морфологических признаков злокачественной опухоли в исследуемом субстрате. Диагностические критерии могут выявляться асинхронно.
Второй этап – дифференциальный диагноз между первичными и вторичными формами ГЛГ. Диагноз ПГЛГ устанавливается при 1) выявлении биаллельной мутации в одном из известных генов ГЛГ; 2) при семейном анамнезе, подтверждающем наследственный характер заболевания; 3) при сохранении дефекта клеточной цитотоксичности НК клеток после остановки терапии в ремиссии заболевания. Диагноз ВГЛГ устанавливают при отсутствии признаков ПГЛГ и подтверждают установлением основного диагноза в соответствии с принципами диагностики соответствующей нозологии.
3. Лечение
3.1 Консервативное лечение
Цель консервативного лечения – подавление системного воспалительного ответа, восстановление функции органов и (при ПГЛГ) подготовка и выполнение трансплантации гемопоэтических стволовых клеток. ТГСК – единственный куративный метод лечения при ПГЛГ. Терапия ГЛГ осуществляется в соответствии со следующими принципами: 1) при установлении клинического диагноза ГЛГ назначается программная иммуносупрессивная химиотерапия (состав приведен ниже); 2) при верификации первичной формы ГЛГ пациенту показано выполнение трансплантации гемопоэтических стволовых клеток от аллогенного донора; 3) на всех этапах назначается многокомпонентная сопроводительная терапия, направленная на профилактику и лечение оппортунистических инфекций, замещение функции костного мозга (компонентная гемотерапия) и контроль осложнений иммуносупрессивной химиотерапии. Порядок назначения препаратов в программе иммуносупрессивной химиотерапии:
Пациентам с гемофагоцитарным лимфогистиоцитозом рекомендовано:
Фазу инициальной терапии рекомендовано проводить по схеме:
3.1.1 Этопозид в дозе 150 мг/м2 внутривенно капельно в дни 1,4,8,12,15,22,29,36,43,50,57
3.1.2 Дексаметазон в дозе 10 мг/м2 внутрь или внутривенно в дни 1-14, в дозе 5 мг/м2 в дни 15-28, в дозе 2,5 мг/м2 в дни 29-42, в дозе 1,25 мг/м2 в дни 43-56.
3.1.3 Циклоспорин А в стартовой дозе 5 мг/кг внутрь с дня 14 постоянно, целевая концентрация То-100-150 нг/мл.
3.1.4 Метотрексат (интратекально) в возрастной дозе (см. комментарий); вводится в дни 15,22,29,36 только при сохранении плеоцитоза или прогрессии неврологической симптоматики после двух недель системной терапии.
3.1.5 Преднизолон (интратекально) в возрастной дозе (см. комментарий); вводится в дни 15,22,29,36 только при сохранении плеоцитоза или прогрессии неврологической симптоматики после двух недель системной терапии.
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
фазу поддерживающей терапии рекомендовано проводить по схеме:
3.1.6 Этопозид в дозе 150 мг/м2 внутривенно капельно 1 раз в две недели в альтернирующем режиме с дексаметазоном
3.1.7 Дексаметазон в дозе 10 мг/м2 внутрь или внутривенно в течение трех дней с интервалом в две недели в альтернирующем режиме с этопозидом
3.1.8 Циклоспорин А в стартовой дозе 5 мг/кг внутрь с дня 14 постоянно, целевая концентрация То-100-150 нг/мл.
терапия второй линии
3.1.9 Антитимоцитарный глобулин (кроличий) в курсовой дозе 25 мг/кг
3.1.10 Метилпреднизолон в дозе 5 мг/кг/сутки в течение 5 дней
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Комментарий: Возрастная доза метотрексата для интратекального введения: 3 лет – 12 мг; Возрастная доза преднизолона для интратекального введения: 3 лет – 10 мг. При ПГЛГ поддерживающая терапия продолжается до выполнения ТГСК.
3.3 Хирургическое лечение
Хирургическое пособие не применяется в терапии ГЛГ
3.4 Иное лечение
Сопроводительная антимикробная и трансфузионная терапия проводятся в соответствии с действующими клиническими рекомендациями
4. Реабилитация
Реабилитация и диспансерное наблюдение пациентов с ПГЛГ осуществляются в соответствии с принципами, принятыми для реципиентов аллогенной трансплантации гемопоэтических стволовых клеток.
5. Профилактика и диспансерное наблюдение
Пациентам с гемофагоцитарным лимфогистиоцитозом рекомендовано:
5.1 Пренатальная диагностика и репродуктивное планирование, включая прерывание беременности по медицинским показаниям, на основании установления диагноза у плода
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
5.2 Выполнение ТГСК у пациентов с верифицированным генетическим диагнозом ПГЛГ до клинической манифестации заболевания
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
6. Дополнительная информация, влияющая на течение и исход заболевания
6.1 Выбор донора для выполнения ТГСК от аллогенного донора (в порядке приоритета)
полностью совместимый сиблинг (включая пуповинную кровь)
полностью совместимый неродственный донор
частично совместимый (гаплоидентичный) родственный донор
неродственная пуповинная кровь
6.2 Срок выполнения ТГСК
ТГСК при ПГЛГ должна быть выполнена в наиболее ранний срок, до 6 месяцев от манифестации заболевания
поиск неродственного донора должен быть инициирован в момент верификации генетической природы ПГЛГ
При выполнении трансплантации от совместимого сиблинга необходимо исключить ПГЛГ у донора на основании генетического или, при неустановленном генетическом дефекте, функционального тестирования.
Критерии оценки качества медицинской помощи
Критерии качества
Уровень достоверности доказательств
Уровень убедительности рекомендаций
Выполнено определение концентрации ферритина, фибриногена, триглицеридов при подозрении на ГЛГ
Выполнена пункция костного мозга с подсчетом миелограммы при подозрении на ГЛГ
Выполнено молекулярно-генетическое исследование при установлении клинического диагноза ГЛГ
Проведена иммуносупрессивная химиотерапия (с началом терапии не позднее 24 часов от установления диагноза ГЛГ)
Направление документов пациента в центр трансплантации костного мозга в течение 7 дней от верификации первичной формы ГЛГ
Список литературы
Приложение А1. Состав рабочей группы
Конфликт интересов отсутствует
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций:
Педиатрия 31.08.19
Таблица П1 – Уровни достоверности доказательств
Уровень достоверности
Источник доказательств
Проспективные рандомизированные контролируемые исследования
Достаточное количество исследований с достаточной мощностью, с участием большого количества пациентов и получением большого количества данных
Как минимум одно хорошо организованное рандомизированное контролируемое исследование
Репрезентативная выборка пациентов
II (2)
Проспективные с рандомизацией или без исследования с ограниченным количеством данных
Несколько исследований с небольшим количеством пациентов
Хорошо организованное проспективное исследование когорты
Мета-анализы ограничены, но проведены на хорошем уровне
Результаты не презентативны в отношении целевой популяции
Хорошо организованные исследования «случай-контроль»
III (3)
Нерандомизированные контролируемые исследования
Исследования с недостаточным контролем
Рандомизированные клинические исследования с как минимум 1 значительной или как минимум 3 незначительными методологическими ошибками
Ретроспективные или наблюдательные исследования
Серия клинических наблюдений
Противоречивые данные, не позволяющие сформировать окончательную рекомендацию
IV (4)
Мнение эксперта/данные из отчета экспертной комиссии, экспериментально подтвержденные и теоретически обоснованные
Таблица П2 – Уровни убедительности рекомендаций
Уровень убедительности
Описание
Расшифровка
Рекомендация основана на высоком уровне доказательности (как минимум 1 убедительная публикация I уровня доказательности, показывающая значительное превосходство пользы над риском)
Метод/терапия первой линии; либо в сочетании со стандартной методикой/терапией
Рекомендация основана на среднем уровне доказательности (как минимум 1 убедительная публикация II уровня доказательности, показывающая значительное превосходство пользы над риском)
Метод/терапия второй линии; либо при отказе, противопоказании, или неэффективности стандартной методики/терапии. Рекомендуется мониторирование побочных явлений
Рекомендация основана на слабом уровне доказательности (но как минимум 1 убедительная публикация III уровня доказательности, показывающая значительное превосходство пользы над риском) или
нет убедительных данных ни о пользе, ни о риске)
Нет возражений против данного метода/терапии или нет возражений против продолжения данного метода/терапии
Рекомендовано при отказе, противопоказании, или неэффективности стандартной методики/терапии, при условии отсутствия побочных эффектов
Отсутствие убедительных публикаций I, II или III уровня доказательности, показывающих значительное превосходство пользы над риском, либо убедительные публикации I, II или III уровня доказательности, показывающие значительное превосходство риска над пользой
Порядок обновления клинических рекомендаций – пересмотр 1 раз в год.
Приложение Б. Алгоритмы ведения пациента
Алгоритм клинической и лабораторной диагностики гемофагоцитарного лимфогистиоцитоза
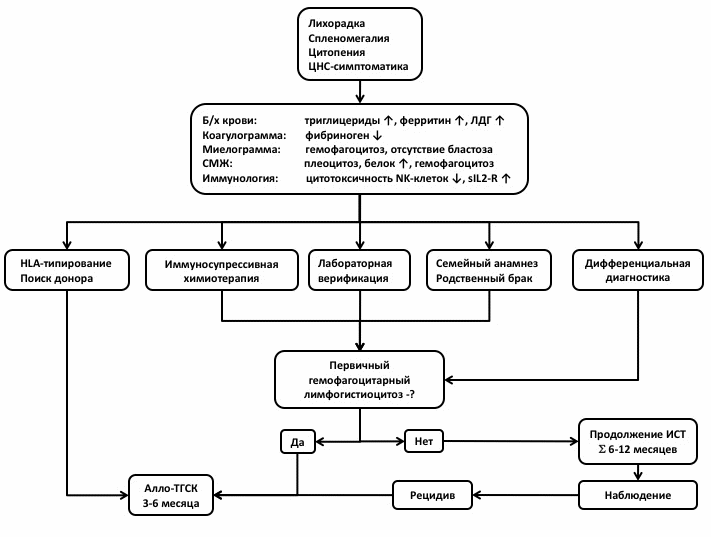
Алгоритм ведения пациентов с гемофагоцитарным лимфогистиоцитозом
Приложение В. Информация для пациентов
Гемофагоцитарный лимфогистиоцитоз – редкое заболевание, причиной которого является нарушение в работе иммунной системы. В результате этого нарушения происходит избыточная активация и размножение некоторых видов лейкоцитов, которые в результате вызывают тяжелое повреждение органов. Наиболее часто нарушается работа костного мозга, печени, селезенки и головного мозга.
Основными проявлениями заболевания являются высокая температура, увеличение размеров печени и селезенки, изменения в анализах крови в виде снижения основных показателей – гемоглобина, лейкоцитов, тромбоцитов и свертываемости, а также нарушения сознания и поведения, обусловленные повреждением головного мозга.
Причиной заболевания может быть наследственный (генетический) дефект в работе иммунной системы, в этом случае говорят о первичном гемофагоцитарном лимфогистиоцитозе, или сбой, обусловленный другим тяжелым заболеванием, в этом случае говорят о вторичном гемофагоцитарном лимфогистиоцитозе. Наиболее часто вторичный гемофагоцитарный лимфогистиоцитоз встречается при ревматических заболеваниях, опухолях и инфекциях, вызванных вирусами семейства герпес-вирусов.
Для установления диагноза необходимо выполнение большого количества исследований крови, а также пункции костного мозга и спинномозговой жидкости. При подозрении на гемофагоцитарный лимфогистиоцитоз обследование должно быть проведено быстро, в течении нескольких дней. Для подтверждения диагноза наследственной формы гемофагоцитарного лимфогистиоцитоза необходимо выполнение молекулярно-генетического исследования.
Гемофагоцитарный лимфогистиоцитоз – тяжелое заболевание, которое, при отсутствии лечения, приводит к смерти пациента.
Лечение гемофагоцитарного лимфогистиоцитоза состоит из двух этапов. На первом этапе назначают химиотерапию, подавляющую функцию иммунной системы. Эта терапия состоит из трех основных препаратов: этопозид, дексаметазон и циклоспорин А. Некоторым пациентам для контроля поражения головного мозга необходимо введение химиопрепаратов в спинномозговой канал. Целью иммуносупрессивной терапии является установление контроля над активацией иммунной системы и нормализация работы пораженных органов. Интенсивная фаза лечения длится два месяци и, как правило, требует пребывания в стационаре. Для лечения необходимо установить центральный венозный катетер, через который вводят лекарства и делают забор крови на исследование.
Для пациентов с первичным гемофагоцитарным лимфогистиоцитозом вторым этапом лечения является трансплантация гемопоэтических стволовых клеток. Трансплантация является необходимым этапом терапии, без которого излечение пациента с гемофагоцитарным лимфогистиоцитозом невозможно. Трансплантация гемопоэтических стволовых клеток (костного мозга) – сложная медицинская процедура, состоящая из нескольких этапов. Трансплантацию проводят в специализированном отделении. Очено важно выполнить трансплантацию вовремя, через 2-6 месяцев от начала иммуносупрессивной терапии. Для того, чтобы выполнение трансплантации стало возможным, вскоре после установления диагноза необходимо начать поиск донора. Донором может быть полностью или частично совместимый родственник (брат, сестра, мать, отец) или полностью совместимый неродственный донор. Выбор донора зависит от множества дополнительных показателей и осуществляется в центре трансплантации.
Гемофагоцитарный лимфогистиоцитоз у детей
Общая информация
Краткое описание
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «07» декабря 2017 года
Протокол № 34
Гемофагоцитарный лимфогистиоцитоз – редкое наследственное или приобретенное заболевание, характеризующееся неконтролируемой активацией макрофагов, и, как следствие, нерегулируемым фагоцитозом клеток крови и их предшественников [1].
Код(ы) МКБ-10:
| МКБ-10 | |
| Код | Название |
| D76.1 | Гемофагоцитарный лимфогистиоцитоз |
| D76.2 | Гемофагоцитарный синдром, связанный с инфекцией |
Дата разработки/пересмотра протокола: 2017 год.
Пользователи протокола: врачи-педиатры, ВОП, онкологи/гематологи, ревматологи.
Категория пациентов: дети.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+), результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
| GPP | Наилучшая клиническая практика |
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
К ГФС относятся два различных состояния, которые по начальным клиническим симптомам трудно отличить друг от друга [1].
Семейно-наследственный (первичный) гемофагоцитарный лимфогистиоцитоз – аутосомно-рецессивное заболевание, в генезе которого важную роль играет мутация в гене перфорина, которая встречается в 20–40% случаев СГЛГ.
Вторичный гемофагоцитарный лимфогистиоцитоз – синдром макрофагальной активации с гемофагоцитозом, который развивается в результате иммуной активации системы мононуклеарных фагоцитов.
Вторичные гемофагоцигарные синдромы развиваются как осложнение основного заболевания при широком круге патологических процессов [1,2,3]. В зависимости от природы основного заболевания принято выделять гемофагоцитарный синдром, связанный с [3]:
· инфекцией;
· опухолью;
· первичным иммунодефицитом;
· системной аутоиммунной патологией;
· наследственными дефектами метаболизма.
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Диагностические критерии
Физикальное обследование [3,4]:
Осмотр больного: необходимо обратить внимание на температуру тела, рост, вес, окружность головы, сыпь на коже головы и туловища, геморрагические элементы на коже, активные кровотечения, желтушность, бледность, альбинизм, лимфаденопатию, тонзиллит, пороки развития скелета, одышку, тахипноэ, размеры печени, селезенки, периферические отеки, неврологическую симптоматику (парезы/параличи черепных нервов, уровень сознания, менингеальные знаки).
Клиническая симптоматика [2]:
· упорная лихорадка более 38,5°С в течение 7 суток и более, рефрактерная к антимикробной терапии;
· спленомегалия более 3 с, из-под реберной дуги.
Лабораторные исследования 3:
· ОАК + лейкоформула ручным методом: анемия (Hb 9 ), нейтропения ( 9 ), ускорение СОЭ. Возможны 2-х или 3-х ростковые цитопении
· Биохимический анализ крови: повышение уровня триглицеридов (уровень триглицеридов натощак ³2,0 ммоль/л или ³3,0 стандартных отклонения от средней возрастной нормы), ферритина (>500 мкграмм/л), возможны гипопротеинемия, повышение трансаминаз
· Коагулограмма: гипофибриногенемия (£1,5 г/л или 3,0 стандартные отклонения), снижение протромбинового времени (ПВ) и протромбинового комплекса (ПТИ), удлинение международного нормализованного времени (МНО)
· цитологическое исследование миелограммы или морфологическое исследование биоптата лимфоузла или селезенки: наличие гемофагоцитирующих макрофагов. При стандартном окрашивании пунктата костного мозга выявляется инфильтрация активированными моноцитами/макрофагами, не несущими признаков злокачественного перерождения. Моноцитарный компонент сопровождается, как правило, инфильтратом из малых лимфоцитов. Часто удается обнаружить феномен гемофагоцитоза, т.е. макрофаги с явлением фагоцитоза клеточных элементов: эритроцитов, реже тромбоцитов и лейкоцитов. На поздних этапах отмечается выраженное обеднение костного мозга с формированием картины аплазии кроветворения.
· Иммунограмма: низкая или полное отсутствие активности натуральных киллеров (NK-клеток), повышен уровень растворимого рецептора интерлейкина-2 (IL-2) CD25 >2400 U/ml. Исследование дегрануляции НК-клеток на основе экспрессии CD 107а на активированных НК-клетках. Исследование экспрессии перфорина, SAP, XIAP в НК и Т-клетках методом проточной цитометрии.
· Молекулярно-генетическое исследование для дифференциации СЛГЛ и ЛГЛ: мутации гена перфорина (10q21).
· HLA типирование пациента и его семьи
Диагноз ГЛГ является правомочным при наличии мутации гена порфирина при молекулярно-генетическом исследовании и/или при выполнении 5 из 8 условий [2]:
1) лихорадка
2) спленомегалия
3) 2-х или 3-х ростковая цитопения
4) гипертриглицеридемия и/или гипофибриногенемия
5) гемофагоцитоз в пунктате костного мозга или в биопсийном материале лимфоузла или селезенки
6) гиперферритинемия
7) снижение или полное отсутствие активности NK- клеток
8) увеличение уровня растворимого рецептора IL-2 CD25
Инструментальные исследования [3,6]:
· УЗИ органов брюшной полости и забрюшинного пространства – позволяет оценить размеры печени, селезенки, и увеличение лимфоузлов брюшной полости, наличие свободной жидкости в брюшной полости.
· МРТ головного мозга в режиме Т1и, Т2, FLAIR, с контрастированием гадолинием.
Диагностический алгоритм: (схема 1)
Дифференциальный диагноз
| Диагноз | Обоснование для дифференциальной диагностики | Обследования | Критерии исключения диагноза |
| Острый лейкоз | Гиперпластический, анемический, геморрагический синдромы, лихорадка и другие симптомы интоксикации | Исследование миелограммы | Наличие бластной метаплазии в костном мозге более 25% |
| Миелодиспластический синдром | Гиперпластический, анемический, геморрагический синдромы, лихорадка и другие симптомы интоксикации | Исследование миелограммы | Как правило, гиперклеточный костный мозг, дисплазия ростков кроветворения, наличие бластной метаплазии |
| Приобретенная апластическая анемия | Симптомы интоксикации, лихорадка, 2-х или 3-х ростковая цитопения | Исследование миелограммы | костный мозг малоклеточный, ростки кроветворения угнетены, костный мозг полиморфный, бластные клетки |
| Инфекционный мононуклеоз | Лимфопролиферативный синдром, лимфоцитоз, моноцитоз, возможны позитивные IgM, IgG, DNA-EBV | Исследование миелограммы. | Отсутствует гемофагоцитозвмиелограмме |
| Сепсис | Упорная лихорадка, выраженные симптомы интоксикации, возможны 2-х и 3-х ростковые цитопении, коагулопатия | Исследование миелограммы, уровня прокальцитонина | В миелограмме раздражение или угнетение костного мозга, без признаков гемофагоцитоза. Уровень прокальцитонина резко повышен. |
| Синдром Вискотта-Олдрича | Геморрагический синдром, инфекционные осложнения, тромбоцитопения | Сбор анамнеза, Исследование иммунного статуса, миелограмма. Молекулярно-генетические исследования | Сочетание иммунодефицита, тромбоцитопении и атопического дерматита. В миелограмме отсутствует гемофагоцитоз7 Мутация в WASP |
Лечение
Препараты (действующие вещества), применяющиеся при лечении
| Азитромицин (Azithromycin) |
| Амикацин (Amikacin) |
| Ампициллин (Ampicillin) |
| Амфотерицин B (Amphotericin B) |
| Ацикловир (Acyclovir) |
| Валацикловир (Valacyclovir) |
| Ванкомицин (Vancomycin) |
| Вориконазол (Voriconazole) |
| Ганцикловир (Ganciclovir) |
| Гентамицин (Gentamicin) |
| Дексаметазон (Dexamethasone) |
| Декстроза (Dextrose) |
| Имипенем (Imipenem) |
| Иммуноглобулин G человеческий нормальный (Immunoglobulin G human normal) |
| Каспофунгин (Caspofungin) |
| Кларитромицин (Clarithromycin) |
| Левофлоксацин (Levofloxacin) |
| Линезолид (Linezolid) |
| Меропенем (Meropenem) |
| Метотрексат (Methotrexate) |
| Метронидазол (Metronidazole) |
| Микафунгин (Micafungin) |
| Натрия хлорид (Sodium chloride) |
| Нистатин (Nystatin) |
| Омепразол (Omeprazole) |
| Офлоксацин (Ofloxacin) |
| Преднизолон (Prednisolone) |
| Ранитидин (Ranitidine) |
| Сульбактам (Sulbactam) |
| Сульфаметоксазол (Sulphamethoxazole) |
| Триметоприм (Trimethoprim) |
| Флуконазол (Fluconazole) |
| Цефепим (Cefepime) |
| Цефоперазон (Cefoperazone) |
| Цефтазидим (Ceftazidime) |
| Цефтриаксон (Ceftriaxone) |
| Цефуроксим (Cefuroxime) |
| Циклоспорин (Cyclosporine) |
| Ципрофлоксацин (Ciprofloxacin) |
| Эртапенем (Ertapenem) |
| Этопозид (Etoposide) |
Группы препаратов согласно АТХ, применяющиеся при лечении
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ
посиндромная терапия с целью обеспечения транспортабельности больного в специализированное отделение.
Немедикаментозное лечение [3,6,7]: режим и диета зависит от тяжести состояния пациента.
· Режим – палатный.
· Диета – Стол №11, стол №1Б, стол №5П (с исключением острых, жирных, жареных блюд, обогащенная белком).
Медикаментозное лечение.
Терапия на догоспитальном этапе зависит от наличия того или иного синдрома, имеющего место у больного:
· анемический синдром требует заместительной терапии одногруппной лейкофильтрованной эритроцитарной взвесью при снижении Нв ниже 80г/л;
· геморрагический синдром – остановка кровотечение, заместительная терапия одногруппнымлейкофильтрованным, вирусинактивированнымтромбоконцентратом. При дефиците плазменных факторов свертывания и ДВС синдроме трансфузия СЗП;
· симптоматическая терапия – адекватная антибактериальная, противогрибковая терапия.
Перечень основных лекарственных средств: нет
Перечень дополнительных лекарственных средств
Хирургическое вмешательство: нет.
Дальнейшее ведение:
Профилактические мероприятия: своевременная терапия инфекционно-септических осложнений в случае вторичного ЛГЛ, медико-генетическая консультация в случае СГЛГ.
Мониторинг состояния пациента:
· контроль основных витальных функций – АД, пульс, частота дыхания, степени сознания;
· контроль показателей гемограммы – эритроциты, Нв, лейкоциты, тромбоциты ежедневно;
· контроль коагулограммы ежедневно.
Индикаторы эффективности лечения
· Ясное сознание;
· Стабильная гемодинамика;
· Отсутствие кровотечения;
· стабильные показатели гемограммы (Нв>80г/л, тромбоциты ³30´10 9 /л);
· сохранный диурез.
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ
Карта наблюдения пациента, маршрутизация пациента
Тактика лечения программная химиотерапия, иммуносупрессивная терапия с последующей трансплантацией гемопоэтических стволовых клеток [2,3,7,8,9,10].
Немедикаментозное лечение:
· Режим: пациенты в изолированные (боксированные) палаты:
— ламинарный поток воздуха,
— изоляция инфекционных больных в палаты с отрицательным давлением;
— личная гигиена и правильная обработка рук (согласно «Руководство ВОЗ по гигиене рук в медико-санитарной помощи”, Женева, 2006 г.) [8];
— при агранулоцитозе туалет полости рта поролоновыми щетками, полоскания антисептиками;
· Диета – низко бактериальная пища, усиленное питание – высококалорийная диета с полуторным по сравнению с возрастными нормами количеством белков, витаминизированная, богатая минеральными веществами. Для детей с различными нарушениями питания включение в питание различных лечебных смесей.
· обеспечение венозного доступа с установкой центрального венозного катетера (из тефлона). Смена катетера по леске запрещается. Применение катетеров из полиэтилена запрещается. Уход за центральным катетером осуществляется обученным медицинским персоналом.;
Медикаментозное лечение [2]:
· Терапия состоит из инициального 8-недельного курса комбинированной иммуносупрессивной и химиотерапии, затем продолженная иммуносупрессивная и химиотерапия до подбора донора для ТГСК и проведения ТГСК. Инициальная терапия включает длительную терапию дексаметазоном, циклоспорин и этопозид, а для некоторых пациентов (с поражением ЦНС) – интратекальная терапия метотрексатом и преднизолоном.
· сопроводительная антибактериальная, противогрибковая, противовирусная терапия, заместительная терапия, направленная на профилактику и лечение инфекционных осложнений. Лечение сопутствующих инфекционных и других осложнений осуществляется согласно Протоколам терапии соответствующих нозологий 17.
Схема инициальной терапии (1-8 недели):
· Дексаметазон назначается перорально в 3 приема (при невозможности перорального приема внутривенно). Доза дексаметазона в 1,2 недели 10мг/м 2 /день, в 3,4 недели – 5мг/м 2 /день, в 5,6 недели – 2,5 мг/м 2 /день, в 7,8 недели – 1,25 мг/м 2 /день/
· Этопозид назначается внутривенно капельно 1-3 часа, разводится на 0,9% хлорида натрия или 5% растворе глюкозы из расчета 0,4мг/мл раствора. В случае инициальнойнейтропении (абсолютное количество нейтрофилов
| Возраст | 1-2 года | 2-3 года | >3 лет | |
| Метотрексат | 6 мг | 8 мг | 10 мг | 12 мг |
| Преднизолон | 4 мг | 6 мг | 8 мг | 10 мг |
Схема продолженной терапии(9-24 недели, 25-40 недели): 
· Дексаметазон 10мг/м 2 /день пульс-терапия по 3 дня каждые 2 недели перорально в 3 приема;
· Этопозид 150мг/м 2 внутривенно капельно 1-3 часа, вводится каждые 2 недели, разводится на 0,9% хлорида натрия или 5% растворе глюкозы из расчета 0,4мг/мл раствора;
· Циклоспорин назначается под контролем функции почек внутрь в 2 приема, доза зависит от уровня циклоспорина в сыворотке крови. Необходимый уровень циклоспорина, который рекомендуют поддерживать 200 микрограмм/мл.
Предлагаются 4 стратегии лечения, и лечение может быть редуцировано и остановлено, если нет реактивации:
1) продолжить продолженную терапию до 40 недель;
2) продлить интервал между каждой инфузиейэтопозида и пульс-терапиейдексаметазона от 2 до 4 недель, продолжить терапию циклоспорином как ранее. Таким образом, пациенты получают альтернирующую терапию каждую вторую неделю (не еженедельно) введениями этопозида и пульс-терапиейдексаметазона;
3) исключить из терапии этопозид, продолжить терапию дексаметазоном и циклоспорином А, в дозах и интервалах, рекомендуемых для продолженной терапии на 9-40 неделях;
4) исключить из терапии этопозид, продолжить терапию дексаметазоном или циклоспорином А в монотерапии.
Перечень основных лекарственных средств:
Хирургическое лечение:
Процедура Аллогенной трансплантации гемопоэтических стволовых клеток – является обязательной для первичных форм ЛГЛ, для прогрессирующих и персистирующих форм ЛГЛ, не имеющих генетической верификации. В случае разрешающихся форм ЛГЛ, не имеющих генетической верификации, АллоТГСК проводится при реактивации заболевания после окончания продолженной терапии. В случае отсутствия совместимого донора как альтернатива возможна гаплоидентичная АллоТГСК [21,22] (УДА).
Дальнейшее ведение
· соответствует наблюдению пациентов после АллоТГСК [21].
Индикаторы эффективности лечения [2]:
Клинический ответ (оценивается на 2-4 неделе терапии):
· отсутствие лихорадки;
· редукция размеров селезенки;
· тромбоциты ³100´10 9 /л;
· нормальный уровень фибриногена;
· редукция уровня ферритина (на 25%).
Оценка ответа в решающие точки и в дальнейшем на терапии через 8 недель (резолюция):
Неактивное заболевание:
· нет лихорадки;
· нет спленомегалии;
· нет цитопении (Нв³90г/л, тромбоциты³100´10 9 /л, абсолютное количество нейтрофилов ³0,5´10 9 /л);
· нет гипертриглицеридемии ( 9 /л;
· гипертриглицеридемия (³3 ммоль/л или ³265 мг/дл);
· гипофибриногенемия£1,5 г/л;
· повышение уровня ферритина;
· CD25³2400 U/ml.
· развитие новых ЦНС симптомов достаточно рассматривать как единственный критерий реактивации заболевания
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ
Показания для плановой госпитализации:
· при ранее установленном диагнозе повторная госпитализация на очередной курс терапии.
Показания для экстренной госпитализации:
· при подозрении на ГЛГ для первичной диагностики и лечения, а также в случае реактивации заболевания при уже установленном диагнозе.
Информация
Источники и литература
Информация
| п/о | перорально |
| АллоТГСК | аллогенная трансплантация гемопоэтических стволовых клеток |
| АЧТВ | активированное частично тромбопластиновое время |
| ВИЧ | вирус иммунодефицита человека |
| ВВИГ | внутривенные иммуноглобулины |
| ВОЗ | всемирная организация здравоохранения |
| ВПГ | вирус простого герпеса |
| ГЛГ | Гемофагоцитарный лимфогистиоцитоз |
| ГФС | Гемофагоцитарный синдром |
| ИФА | иммуноферментный анализ |
| ИТ | интратекальная терапия |
| КТ | компьютерная томография |
| ЛДГ | лактатдегидрогеназа |
| МНН | международное непатентованное название |
| МНО | международное нормализованное время |
| МРТ | магнитно-резонансная томография |
| ОАК+тромбоциты | общий анализ крови с подсчетом лейкоформулы и тромбоцитов |
| ОАМ | общий анализ мочи |
| ПЦР | полимеразная цепная реакция |
| ПВ | протромбиновое время |
| ПТИ | протромбиновый индекс |
| ПДФ | продукты деградации фибринолиза |
| РКИ | Рандомизированные клинические исследования |
| РК | Республика Казахстан |
| СГЛГ | семейный гемофагоцитарныйлимфогистиоцитоз |
| СОЭ | скорость оседания эритроцитов |
| ТГСК | трансплантация гемопоэтических стволовых клеток |
| УЗИ | ультразвуковое исследование |
| УД | уровень доказательности |
| ЦНС | центральная нервная система |
| ЦНС | центральная нервная система |
| ЦсА | циклоспорин А |
| ЭБВ | Эбштейн-Барр вирус |
| ЭКГ | электрокардиография |
| ЭхоКГ | эхокардиография |
| Hb | гемоглобин |
| HLA | Human leukocytes antigen (система человеческих лейкоцитарных антигенов) |
| IL | Интерлейкин |
| CD | кластеры дифференцировки (моноклональные антитела) |
| NK | натуральные киллеры |
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ПРОТОКОЛА
Список разработчиков протокола
1) Манжуова Лязат Нурбапаевна –кандидат медицинских наук, заведующий отделением онкогематологии, РГП на ПХВ«Научный центр педиатрии и детской хирургии».
2) Омарова Кулян Омаровна – профессор, доктор медицинских наук, РГП на ПХВ«Научный центр педиатрии и детской хирургии».
3) Булабаева Гульнара Ержановна – заведующая отделением онкогематологии РГП на ПХВ «Научный центр педиатрии и детской хирургии».
4) Нургалиев Даир Жванышевич – доктор медицинских наук, заведующий отделением гематологии АО «Национальный научный центр материнства и детства», г. Астана.
5) Сарсекбаев Ергали Семгалиевич – врач отделения ТГСК РГП на ПХВ«Научный центр педиатрии и детской хирургии».
6) Калиева Шолпан Сабатаевна – кандидат медицинских наук, PHD, доцент, заведующая кафедрой клинической фармакологии и доказательной медицины РГП на ПХВ «Карагандинский государственный медицинский университет».
Указание на отсутствие конфликта интересов:нет.
Список рецензентов:
1) Ташенова Гульнара Талиповна – доктор медицинских наук, заведующий кафедрой детских болезней №2, Казахский научный медицинский университет имени С.А.Асфендиарова.